Az enzimek olyan fehérjemolekulák a sejtekben, amelyek biológiai katalizátorként működnek. Az enzimek felgyorsítják a szervezetben zajló kémiai reakciókat, de nem használódnak el a folyamat során, ezért újra és újra felhasználhatók.
Az élőlényekben szinte minden biokémiai reakcióhoz enzimekre van szükség. Egy enzimmel a kémiai reakciók sokkal gyorsabban mennek végbe, mint az enzim nélkül.p39 Más biokatalizátorok a katalitikus RNS-molekulák, az úgynevezett ribozimek.
A reakció kezdetén lévő anyagokat szubsztrátoknak nevezzük. A reakció végén lévő anyagok a termékek. Az enzimek a szubsztrátokon dolgoznak, és azokat termékké alakítják. Az enzimek tanulmányozását nevezzük enzimológiának.
Az első enzimet 1833-ban Anselme Payen találta meg.
Szerkezet és működés
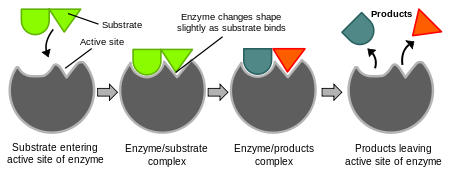
Az enzimek többsége fehérje, amely egyedi háromdimenziós szerkezettel rendelkezik. A működésük kulcsa az aktív hely, az a kis régió az enzim felületén, ahol a szubsztrát kötődik és a kémiai átalakulás lezajlik. Az aktív hely alakja és kémiai tulajdonságai határozzák meg az enzim szubsztrát-specificitását.
Két gyakori modell írja le az enzim–szubsztrát kölcsönhatást:
- Lock-and-key (zár és kulcs) — a szubsztrát pontosan illik az aktív helybe;
- Induced fit (indukált illeszkedés) — az enzim rugalmasan alakot változtat, hogy optimálisan illeszkedjen a szubsztráthoz.
Enzimkinetika röviden
Az enzimsebességet több tényező befolyásolja, és gyakran a Michaelis–Menten modelllel írjuk le. Két fontos fogalom:
- Vmax — az enzim maximális reakciósebessége telített szubsztrátkoncentrációnál;
- Km — a szubsztrátkoncentráció, ahol a reakciósebesség a Vmax feléhez közelít; a kisebb Km nagyobb affinitást jelez az enzim és a szubsztrát között.
A működést befolyásoló tényezők
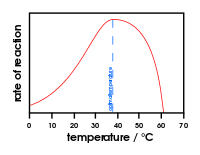
- Hőmérséklet: emelkedő hőmérsékleten általában nő az aktivitás, de túl magas hőmérséklet denaturálhatja a fehérjét és elveszti aktivitását.
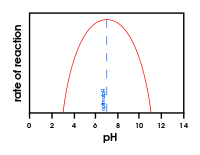
- pH: minden enzimnek van optimális pH-értéke; ettől eltérve az ionizációs állapot megváltozik, és csökkenhet az aktivitás.
- Szubsztrát koncentráció: növekvő koncentráció növeli a sebességet, de telítés esetén eléri a Vmax-ot.
- Inhibiterek: például kompetitív (a szubsztrát kötőhelyet foglalja el), nemkompetitív és unkompetitív inhibiterek csökkentik az aktivitást különböző módon.
- Kofaktorok és koenzimek: sok enzimhez szükség van fémionokra (pl. Mg2+, Zn2+) vagy szerves molekulákra (pl. B-vitaminból származó koenzimek), amelyek segítik a katalízist. Néhány enzimnek állandó, erősen kötődő prostetikus csoportja van.
Szabályozás a sejtekben
A sejtek szigorúan szabályozzák az enzimaktivitást, hogy alkalmazkodjanak a változó körülményekhez:
- Alloszterikus szabályozás: egy molekula az enzim más részéhez kötődve megváltoztatja az aktivitást;
- Kovalens módosítás: például foszforiláció, amely gyorsan be- vagy kikapcsolhat egy enzimet;
- Szabályozott termelés: génszinten történő szabályozás — az enzim mennyisége változhat a termelés és lebontás egyensúlyával;
- Kompartimentalizáció: sok enzim specifikus sejtszervecskékben található (pl. lizozómák, mitokondriumok), ami segít elkülöníteni és szabályozni a reakciókat.
Biológiai szerepek és példák
Az enzimek minden sejtfunkcióban részt vesznek: emésztés, energiaátalakítás, DNS-szintézis és javítás, jelátvitel stb. Néhány ismert példa:
- Amiláz — szénhidrátok lebontása (pl. nyál és hasnyálmirigy);
- Peptidázok (proteázok) — fehérjék bontása;
- Lipázok — zsírok emésztése;
- DNS-polimerázok — DNS másolása;
- ATP-szintáz — ATP termelése a mitokondriumban.
Ipari és orvosi alkalmazások
- Az enzimeket használják élelmiszeriparban (sörfőzés, sajtgyártás), mosószerekben (zsírok és fehérjék lebontása), biotechnológiában (rekombináns fehérjék előállítása) és gyógyszeriparban (enzimgátlók mint gyógyszerek — pl. ACE-gátlók).
- Diagnosztika: specifikus enzimek mérése vérvizsgálatokban fontos kórképek (pl. máj- vagy szívkárosodás) kimutatására.
- Enzimterápia: egyes öröklött anyagcsere-betegségekben hiányzó vagy hibás enzimeket pótolnak.
Ribozimok és nem-protein katalizátorok
Bár a legtöbb enzim fehérje, a biológiai katalízisre képesek bizonyos ribozymek is — speciális RNS-molekulák, amelyek kémiai reakciókat katalizálnak (például rNS-önkatalízis vagy intron kivágás).
Tudományos eszközök és kutatás
Az enzimológia modern módszereket használ: kinetikai mérések, spektroszkópia, kromatográfia, valamint szerkezeti módszerek (röntgenkrisztallográfia, cryo-EM) segítik az enzimek pontos működésének feltárását. Az inhibitorok és aktivátorok kutatása új gyógyszerek alapját adhatja.
Rövid történeti kitekintés
Az első, jól dokumentált enzimet 1833-ban Anselme Payen írta le (diastáz, később amiláz). A "enzim" (enzyme) kifejezést később, a 19. század végén vezették be a biokémiában használt terminusként.
Összefoglalva: az enzimek alapvetőek az élethez — gyorsítják és szabályozzák a kémiai reakciókat, speciálisak, és változatos módokon szabályozhatók, ezért fontosak a sejtek működésében, az iparban és az orvostudományban.