Az elektron egy nagyon kis anyag- és energiadarab. Jelképe e−. 1897-ben J. J. Thomson fedezte fel. Az elektron a modern fizika szerint egy alapvető, nem összetett részecske: tömege a nyugalmi állapotban körülbelül 9,109×10−31 kg (ez a tömeg kevesebb mint 1/1800-a a proton tömegének), töltése −1,602×10−19 coulomb (az ún. elemi töltés nagysága), és nyugalmi energiája ≈0,511 MeV.
Az elektron egy szubatomi részecske. Azért tartják elemi részecskének, mert jelenlegi ismereteink szerint nem bontható kisebb alkotóelemekre. Negatív töltésű, és a kvantummechanika szerint fermion (spinje 1/2), tehát a Pauli-elv szerint nem lehet két elektron ugyanabban a kvantumállapotban ugyanannál az atomnál. Bár az elektron részecskeként viselkedik, hullámtermészetű tulajdonságokkal is rendelkezik (hullám–részecske kettősség), amelyet például diffrakciós kísérletek igazolnak. Az elektronok soha nem érik el a fénysebességet; vákuumban a fénysebességhez c közelítve sem lehet elérniük, de a belső energiájuk és sebességük széles tartományban változhat.
Az elektronok részt vesznek a gravitációs, elektromágneses és gyenge kölcsönhatásokban. (A strong — erős — kölcsönhatásban általában nem vesznek részt, mert nem hordoznak színtöltést.) A televíziókat, motorokat, mobiltelefonokat és sok más dolgot működtető elektromosság valójában sok elektronból áll, amelyek vezetéken vagy más vezetéken keresztül mozognak. Fontos különbség, hogy az elektromos jel terjedési sebessége (a mezőváltozás) közel fénysebességű lehet, míg az egyes töltéses részecskék, azaz az elektronok átlagos vándorlósebessége (driftsebesség) vezetőkben tipikusan nagyon lassú (mm/s–cm/s nagyságrend). Ugyanakkor az elektronoknak a fémekben a Fermi-sebessége rendkívül nagy, ~106 m/s körüli.
Alapvető tulajdonságok
- Töltés: −1 elemi töltés (−1,602×10−19 C).
- Tömeg: nyugalmi tömeg ≈9,109×10−31 kg.
- Spin: 1/2 — fermion, Fermi–Dirac statisztikát követ.
- Stabilitás: az elektron a legtöbb elmélet szerint stabil részecske (alapállapotban nem bomlik fel).
- Antirészecske: a pozitron (e+) az elektron antirészecskéje; találkozáskor annihiláció történik, mely gamma-fotonokat hoz létre.
Elektron az atomokban és a kémiai kötésekben
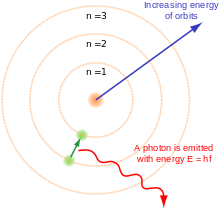
Az elektronok az atomok körül kvantumállapotokban helyezkednek el (atomorbitálok). Az elektronok elrendeződése határozza meg az atom kémiai tulajdonságait és a periódusos rendszer szerkezetét. A vegyértékelektronok (a legkülső héjon lévők) döntenek a kötésképződésről: kötések létrejötte, ionos vagy kovalens viszonyok az elektronok megosztásán vagy átvitelén alapulnak. A Pauli-kizárási elv miatt az anyag térfogata és szilárdsága is fennállhat — az elektronok kvantummechanikai viselkedése biztosítja, hogy a részecskék ne összeomoljanak egyetlen pontba.
Kölcsönhatások és elméletek
A elektronok elektromágneses kölcsönhatásai alapvetőek: Coulomb-taszítás és -vonzás határozza meg az elektromos mezőkkel való kapcsolatot. A kvantumelektrodinamika (QED) az a kvantumtérelmélet, amely pontosan leírja az elektronok és a fotonok kölcsönhatását, és a fizika egyik legjobban kísérletileg alátámasztott elmélete. Elektronok részt vesznek gyenge kölcsönhatásokban is (például béta-bomlásnál keletkező elektron). Gravitációs hatásuk elméletileg létezik, de gyakorlati szempontból elhanyagolható a tömegük kicsinysége miatt.
Előállítás és észlelés
Elektronokat különböző módon lehet előállítani és felgyorsítani:
- Termikus emisszió: felhevített anyagból (katódból) távozó elektronok, használták régebben CRT-kben és vákuumcsövekben.
- Fotonok hatására: fotoelektromos hatás — ha egy fém felszínét fény éri, elektronok szabadulhatnak fel.
- Mezőemisszió: erős elektromos tér hatására kilépő elektronok (field emission).
- Béta-bomlás: radioaktív izotópok közben elektronok (béta-részecskék) keletkeznek.
Az elektronok és mozgásuk detektálására szolgáló eszközök: felhőkamra, buborékkamra, szcintillációs detektorok, félvezető-detektorok, mikrocsövek és modern elektronmikroszkópok (SEM, TEM), valamint részecskegyorsítók és ütköztetők.
Alkalmazások
- Elektronika és áramkörök: az elektronok áramlása adja az elektromos áramot; félvezetőkben és elektronikai eszközökben a töltéshordozók (elektronok és lyukak) működtetik a tranzisztorokat, diódákat és integrált áramköröket.
- Elektronmikroszkópia: nagy felbontású képalkotás elektronnyalábbal (TEM, SEM), anyagtudományban és biológiában alapvető eszköz.
- Röntgen- és sugárforrások: gyors elektronok célba ütközésekor röntgensugárzás keletkezik (röntgencsövek); elektronnyalábokkal dolgozó eszközök ipari hegesztésre, fúváshoz és anyagfeldolgozáshoz is használhatók.
- Gyógyászat: elektron- és fotonsugaras radioterápia daganatok kezelésére; pozitron-emission tomography (PET) a positron–elektron annihiláció gamma-fotonjaira épít.
- Elektron-sugaras litográfia: félvezetőgyártásban használt precíziós mintázatkészítési eljárás.
- Kutatás: részecskegyorsítókban és detektorokban az elektronok segítségével új fizikai jelenségek vizsgálhatók.
Érdekességek
- A pozitron (az elektron antirészecskéje) felfedezése 1932-ben történt (Carl Anderson), és ez megerősítette az antirészecskék létezését.
- Az elektron töltése és tömege meghatározza az elektronvolt (eV) jelentőségét: 1 eV annak az energiának a nagysága, amelyet egy elemi töltés egy volt potenciálkülönbség hatására nyer (≈1,602×10−19 J).
- A mindennapi elektromos jelenségek mögött az elektronok kvantum- és statisztikai viselkedése áll — például a vezetők, félvezetők és szigetelők közötti különbség alapja az elektronok energiasáv-rendszere.
Az elektron tehát egyszerre alapvető építőköve az anyagnak és a modern technológia működésének: megértése és alkalmazása nélkül a 20–21. századi elektronika, orvosi képalkotás, anyagtudomány és részecskefizika elképzelhetetlen lenne.