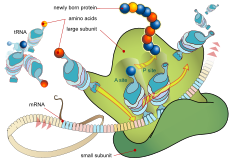
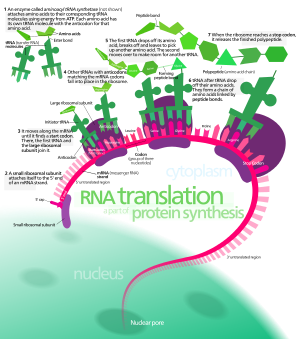
A transzláció (fordítás) a fehérjék bioszintézisének második, a génexpressziós folyamatba illeszkedő lépése: az mRNS-en kódolt nukleotidsorrend alapján polipeptidláncok (fehérjék) szintetizálódnak.
Mielőtt bekövetkezne a transzláció, több előfeldolgozó esemény történik:
- transzkripció, amely az DNS egy szakaszának átírásával hozza létre az elsődleges RNS-molekulát, amelyben intronok és exonok találhatók.
- RNS-splicing a spliceoszómák közreműködésével, amely eltávolítja az intronokat és összekapcsolja az exonokat.
- végül a kifejlődött hírvivő RNS (mRNS) 5' sapkával, 3' poli(A)-farokkal és szükség esetén tovább szerkesztett szekvenciával rendelkezik, amely alkalmassá teszi a riboszómák általi leolvasásra.
A transzláció helye és a riboszóma felépítése
Az eukariótákban a transzláció részben a sejtplazmában (citoplazma) zajlik, részben a durva endoplazmatikus retikulum riboszómáihoz kapcsolódva. A riboszómák két alegységből (kis és nagy) állnak, amelyek együttveszik körül az mRNS-t és biztosítják a kodon–antikodon párosodást, valamint a peptidkötés kialakulását. A baktériumokban viszont, mivel nincs sejtmag, a transzláció a teljes sejtcitoplazmában történik, és gyakran egyidejűleg zajlik a transzkripcióval (transzkripció–transzláció kapcsolás).
Az mRNS szerepe, a genetikai kód és a leolvasás
Az mRNS bázissorrendje határozza meg azt az aminosavsorrendet, amelyből a későbbi polipeptid felépül. A genetikai kód tripletek (kodonok) rendszerén alapul: minden három nukleotid egy aminosavat (vagy a lánc végét jelző stopkodont) határoz meg. A kód degenerált: több kodon is megfelelhet ugyanannak az aminosavnak. A kodon leolvasása során a leolvasási keret (reading frame) megőrzése kritikus — egy eltolódás teljesen megváltoztathatja a szintetizált fehérje összetételét.
T-RNS-ek, aminosav-feltöltés és az enzimatikus ellenőrzés
Az aminosavakat specifikus tRNS-molekulák szállítják, amelyek mindenikének van egy 3 bázisból álló antikodonjai, hogy komplementer módon párosodjanak az mRNS kodonjaival (kodonjaihoz). Az egyes tRNS-eket aminosavakkal az aminoacil-tRNS-szintetázok töltik fel (ez a folyamat minden aminosavra speciális enzim által történik), ez biztosítja az aminosav–antikodon megfelelés pontosságát és a hibák kiszűrését.
A transzláció fő fázisai
Általában három fő szakasz különíthető el:
- Iniciáció (kezdet): az iniciációs komplex kialakulása: a kis riboszóma-alegység kötődik az mRNS-hez, felismeri a startkodont (legtöbbször AUG, amely Met-t kódol), majd az iniciátor tRNS és a nagy alegység csatlakozása után indul meg a láncépítés. Eukariótákban az iniciációs komplex gyakran a 5' sapkától indulva csúszik (scanning) a starthely keresésére; prokariótákban a Shine–Dalgarno-szekvencia segíti a helyes pozícionálást.
- Elongáció (lánchosszabbítás): a megfelelő aminoacil-tRNS-ek sorban érkeznek a riboszóma A- helyére, antikodonjuk párosodik az mRNS kodonjaival, a peptidkötést a riboszóma nagy alegységének peptidil-transzferáz aktivitása hozza létre (az rRNS-nek katalitikus szerepe is van), majd a riboszóma lépked egy kodonnal tovább. Az elongációhoz és a transzláció pontosságához GTP-függő faktorok (elongációs faktorok) járulnak hozzá, amelyek energiát adnak a lépésenkénti mozgáshoz és a hibajavításhoz.
- Termináció (befejezés): amikor a riboszóma stopkodont olvas (UAA, UAG vagy UGA), nem érkezik hozzá megfelelő tRNS, hanem speciális felszabadító faktorok (release factors) kötődnek, amelyek katalizálják a kész polipeptid elválását és a translációs komplex szétesését.
Poliriboszómák, összecsukódás és poszttranszlációs módosítások
Több riboszóma egyszerre dolgozhat egyetlen mRNS-en; az így kialakuló szerkezetet poliszóma (poliriboszóma) nevezzük. A szintézis után a keletkező polipeptidláncnak össze kell hajtogatódnia (folding), gyakran chaperonok segítéségével, hogy funkcionális fehérjévé váljon. Sok fehérjén poszttranszlációs módosítások (például foszforiláció, glikoziláció, diszulfidkötések kialakulása) történnek, amelyek szükségesek a stabilitás, működés vagy irányítás szempontjából.
Sejtalkotók közötti irányítás és szállítás
Sok eukarióta fehérjét a durva endoplazmatikus retikulum riboszómái állítanak elő: a szintézis során a jelpeptid felismerése és a jelreceptor-partner (SRP) által történő megállítás után a riboszóma az ER membránjához kapcsolódik, és a növekvő lánc az ER-lumenbe vagy membránba kerül. A membránhoz kapcsolódott riboszómák külső membránjához tapadnak; a létrejövő fehérjék gyakran az ER belsejébe jutnak, majd csomagolódnak és vezikulákba kerülnek. Ezek a vezikulák a fehérjéket más organellumokba vagy akár a sejt külső részébe (szekréció) szállítják.
Különbségek prokarióták és eukarióták között
Prokariótákban a transzláció a citoplazmában zajlik, és gyakran egyidejű a transzkripcióval, mivel nincs sejtmag. Eukariótákban a transzláció elkülönül a transzkripciótól, bonyolultabb iniciációs mechanizmusok (például Kozak-szekvencia) és több szabályozó fehérje működik. Emellett az eukarióta fehérjék gyakrabban és különböző módon kerülnek poszttranszlációs módosításra és célzott szállításra.
Minőségellenőrzés és szabályozás
A transzláció szigorúan szabályozott: a mRNS elérhetősége, az iniciációs faktorok aktivitása, az aminosav-ellátottság és a riboszómaösszetevők mennyisége mind befolyásolják a fehérjeszintézis sebességét. Hibák esetén a sejt minőségellenőrző mechanizmusai (például mRNS-ellenőrzés, hibás fehérjekomplexek lebontása) lépnek működésbe, hogy megelőzzék a káros fehérjék felhalmozódását.
Összefoglalva: a transzláció egy összetett, energiaigényes és szigorúan szabályozott folyamat, amely az mRNS kódját fordítja le funkcionális fehérjékké. A pontos antikodon–kodon párosodás, az aminosavak helyes feltöltése és a riboszóma aktivitása együtt biztosítják a fehérjék helyes szekvenciáját és szerkezetét, amelyek később a sejten belüli és kívüli feladatokat látják el.