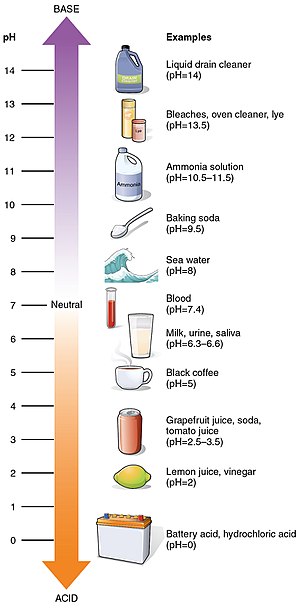
Mi az a pH? A pH egy 0-tól 14-ig terjedő savassági skála. Megmutatja, hogy egy anyag mennyire savas vagy lúgos. A savasabb oldatok pH-ja alacsonyabb, a lúgosabb oldatoké magasabb. A semleges oldatok pH-ja általában 7. A savak pH-ja 7-nél kisebb, míg a lúgok pH-ja 7-nél nagyobb.
A pH az oldatban lévő protonok (H+) koncentrációjának mérőszáma. S.P.L. Sørensen 1909-ben vezette be ezt a fogalmat. A p a német potenz, azaz hatvány vagy mérték (gyakran a negatív logaritmust jelöli), a H pedig a hidrogéniont (H+) jelenti.
Hogyan számoljuk ki a pH-t?
A legegyszerűbb és leggyakrabban használt képlet:
pH = - log 10 [ H + ] {\displaystyle {\mbox{pH}}=-\log _{10}\left[{\mbox{H}}}^{+}\right]}
A [H+] a H+-ionok koncentrációját jelöli (más néven [H3O+], a hidróniumionok azonos koncentrációját), literenként mólban mérve (molaritás). Példa: ha [H+] = 1·10-3 mol·L-1, akkor pH = −log10(1·10-3) = 3.
A helyesebb, kémiailag pontosabb forma azonban az ionok aktivitását használja:
pH = - log 10 [ a H + ] {\displaystyle {\mbox{pH}}=-\log _{10}\left[a_{\mathrm {H^{+}} }\right]}
ahol a H + {\displaystyle a_{\mathrm {H^{+}} }}
pH tartományok, példák és extrém értékek
A legtöbb anyag pH-ja 0 és 14 között van, azonban rendkívül savas vagy lúgos oldatok pH-ja lehet < 0 vagy > 14 is. Példák:
- Desztillált víz (25 °C-on): pH ≈ 7 (neutrális).
- Gyomorsav: pH ≈ 1–2.
- Szappanos víz vagy pH-értékű háztartási lúgok: pH ≈ 9–12.
- Vér: pH ≈ 7,35–7,45 (szigorúan szabályozott biológiai érték).
- 1 M HCl: [H+] ≈ 1 mol·L-1 → pH ≈ 0.
- Nagy koncentrációjú erős savak vagy lúgok: például koncentrált savak esetén előfordulhat pH < 0; nagyon koncentrált lúgoknál pH > 14.
pOH, Kw és a kapcsolat pH-val
A pOH analóg módon a hidroxidion-koncentráció negatív logaritmusa:
pOH = -log10[OH-]
25 °C-on a víz ionizációs egyensúlya (iontermék): Kw = [H+][OH-] = 1,0·10-14, ezért általánosan:
pH + pOH = 14 (25 °C).
Példa: ha [OH-] = 0,1 mol·L-1 → pOH = 1 → pH = 14 − 1 = 13.
Megjegyzés: Kw és így a 14-es összefüggés hőmérsékletfüggő; eltérő hőmérsékleten a sum pH+pOH nem feltétlenül 14.
Mérés és indikáció
- pH-mérő (üvegelektróda): a legpontosabb módszer laboratóriumban. Kalibrálni kell standard pufferoldatokkal (tipikusan pH 4, 7 és/vagy 10).
- pH-papír / indikátorok: egyszerű és gyors, de kevésbé pontos. Univerzális indikátor színskálával közelítő pH-értéket ad.
- Színindikátorok: egyes indikátorok csak bizonyos pH-tartományokban váltanak színt (pl. fenolftalein, metilnarancs).
Aktivitás vs. koncentráció
Gyakorlati mérésekben és sok egyszerű számításnál [H+] koncentrációt használunk, de kémiai precizitás esetén az aktivitás (aH+ = γ·[H+], ahol γ az aktivitási együttható) a mérvadó. Az aktivitási együttható függ az oldat ionerősségétől; nagy ionerősségű (tömény) oldatoknál a különbség jelentős lehet. A pontos számításokhoz vagy mérésekhez gyakran szükséges az aktivitás figyelembevétele.
Gyakorlati számítási példák
- Ha [H+] = 1·10-6 M, akkor pH = −log10(1·10-6) = 6.
- Ha 0,01 M (1·10-2 M) erős sav van, [H+] ≈ 1·10-2, pH ≈ 2.
- Ha [OH-] = 1·10-3 M → pOH = 3, így pH ≈ 14 − 3 = 11 (25 °C esetén).
Fontos megjegyzések és biztonság
- Erős savak és lúgok kezelésekor mindig tarts be biztonsági előírásokat (védőruha, szemvédelem, szellőzés).
- Biológiai rendszerek (pl. emberi vér) kismértékű pH-változást sem tolerálnak; ezért az élő szervezetekben gyakran működnek puffer rendszerek.
- A pH hőmérsékletfüggő lehet: hőmérsékletváltozás hatással van a víz ionizációjára és így a pH-értékekre is.
Röviden: a pH egy logaritmikus skála, amely a hidrogénionok koncentrációjának (illetve pontosabban aktivitásának) negatív logaritmusát adja meg. Egyszerűen használható a savasság/lúgosság összehasonlítására, de a pontosabb értelmezéshez ismernünk kell az oldat tulajdonságait (koncentráció, ionerősség, hőmérséklet) és a mérések pontosságát.
![{\displaystyle {\mbox{pH}}=-\log _{10}\left[{\mbox{H}}^{+}\right]}](https://www.alegsaonline.com/image/093977a79b6a17e02db4699475930e48c05d6468.svg)
![{\displaystyle {\mbox{pH}}=-\log _{10}\left[a_{\mathrm {H^{+}} }\right]}](https://www.alegsaonline.com/image/7a631c4037415f3d4483a6cb07e69858b64890fc.svg)