Az NS1-reakció a szerves kémiában egy szubsztitúciós reakció. Az "S" a Nnukleofil szubsztitúciót jelenti, az "1" pedig azt, hogy a sebességet meghatározó lépésben csak egy molekula vesz részt (unimolekuláris). A reakció tipikus intermedierje egy karbokation-intermedier, amelynek stabilitása döntő szerepet játszik a reakció valószínűségében. Christopher Ingold és munkatársai 1940-ben javasolták először a reakciómechanizmust, ezért az SN1-reakciók klasszikus esetei közé tartoznak a mechanisztikai tanulmányoknak.
Mechanizmus röviden
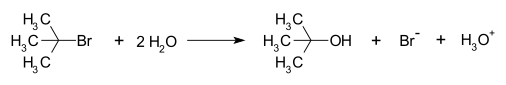
Az SN1 mechanizmus általában két fő lépésre bontható:
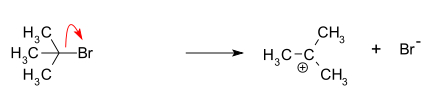
- Első lépés (lassú, sebességmeghatározó): a kiindulási anyagból kilép a kilépő csoport (pl. halogenid), és kialakul egy szabad karbokation. Ez a lépés unimolekuláris, ezért a reakció sebessége csak a kiindulási anyag koncentrációjától függ (rate = k[substrate]).
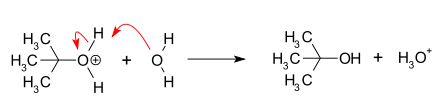
- Második lépés (gyors): a karbokationt a környezet nukleofil része (oldószer, ion vagy más nukleofil) megtámadja, így létrejön a szubsztituált termék.
Kinetika és befolyásoló tényezők
- Subsztrát szerkezete: a karbokation stabilitása az egyik legfontosabb tényező. Tercier > szekunder > primer; a primer általában nem megy SN1 úton, kivéve, ha a karbokation rezonánsan vagy konjugáltan stabilizált (pl. benzil, allyl).
- Kilépő csoport: jó kilépő csoport (pl. halogenidek közül I- vagy Br-) gyorsítja a disszociációt, mert könnyebben távozik és stabilizálja a kilépés után keletkező negatív töltést.
- Oldószer: a poláris protikus oldószerek (pl. víz, alkoholok) stabilizálják a töltéseket és így elősegítik a karbokation kialakulását, ezért ezek kedveznek az SN1 mechanizmusnak. Poláris aprotikus oldószerek viszont általában az SN2-t támogatják.
- Nukleofil: mivel a sebességmeghatározó lépésben nem vesz részt a nukleofil, annak koncentrációja kevésbé befolyásolja a reakció sebességét; azonban a nukleofil termodinamikai és kinetikai tulajdonságai befolyásolják a második lépés gyorsaságát és a termékösszetételt.
- Hőmérséklet: magasabb hőmérséklet általában gyorsítja a disszociációt, de a hőmérséklet hatása a reakciósebességre az aktiválási energiától függ.
Stereokémia és átrendeződések
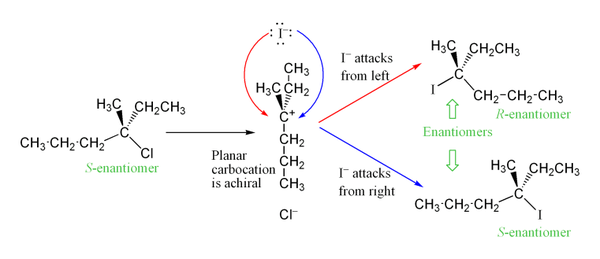
Az SN1-reakciók jellegzetes stereokémiai vonása a részleges vagy teljes racemizáció, ha a kiindulási anyag tércentrumot tartalmaz. A karbokation planáris sp2 hibridizációjú, így a nukleofil mindkét oldalról hozzáférhet, ami racemizációhoz vezet. Azonban ionpárképződés (tightly associated ion pair) esetén előfordulhat részleges megtartás vagy sztereokémiai torzítás.
A karbokation-intermedier hajlamos lehet átcsoportosulásokra (rearrangements), például hidrid- vagy alkilátcsoport vándorlására, ha az átrendezett karbokation energetikailag stabilabb. Ez fontos tényező lehet váratlan termékek kialakulásakor.
Példák és gyakori esetek
- Tercier alkil-halogenidek vizes hidrolízise: a tert-butyl-klorid vízben gyorsan hidrolizál SN1 mechanizmussal, mivel a tercier karbokation stabil.
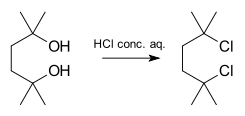
- Savas katalízisú alkoholok szubsztitúciója: erősen savas körülmények között szekunder vagy tercier alkoholokkal végzett reakciók gyakran SN1 mechanizmust követnek, mert a protonált alkohol jó kilépő csoporttá válik.
- Néhány gyakori NS1-reakció előfordul szekunder vagy tercier alkil-halogenidekkel, illetve olyan körülmények között, ahol az oldószer vagy a savas környezet támogatja a karbokation kialakulását; ritkábban terjedelmesen előfordulnak bázikus körülmények között is speciális esetekben.
- Primer alkilhalogenidek esetén általában az alternatív NS2 reakció dominál, kivéve ha a primer karbokation különösen stabilizált (pl. benzil vagy allyl helyzet).
Összehasonlítás az SN2-vel
- Kinetika: SN1: első rendű (rate = k[substrate]); SN2: másodrendű (rate = k[substrate][nukleofil]).
- Szubsztitúciós hely: SN1 kedvez a tersely helyezkedő, karbokationt stabilizáló csoportoknak; SN2 kedvez a kevésbé szubsztetizált (primer) szénatomoknak.
- Oldószer: poláris protikus oldószerek általában SN1-nek kedveznek, míg poláris aprotikus oldószerek megkönnyítik az SN2 reakciót.
- Stereokémia: SN1 gyakran racemizációt, SN2 tipikusan invertálódást (Walden-inverzió) eredményez.
Kísérleti bizonyítékok és energetikai kép
Az SN1 mechanizmus bizonyítékai közé tartozik a sebességi törvény elsőrendű volta, oldószer-dependencia vizsgálatok (poláris protikus oldószerek katalizáló hatása) és a karbokationátmeneti állapotokra utaló kísérleti jelek (pl. átrendezések, termékösszetétel). Az energia-diagramon a jellemző görbe egy magas aktiválási energiájú első átmeneti állapotot (kilépő csoport leválása, karbokation kialakulása) mutat, majd egy alacsonyabb energiaszintű második átmeneti állapotot (nukleofil megtámadás).
Összefoglalás
Az NS1 a nukleofil szubsztitúció egyik alapvető mechanizmusa, amelyet a karbokation-intermedier és a unimolekuláris sebességmeghatározó lépés jellemez. A reakciót a szubsztrát szerkezete, a kilépő csoport minősége, az oldószer és a környezeti feltételek határozzák meg. Mivel gyakran vezet átrendeződésekhez és racemizációhoz, fontos figyelembe venni reakciótervezéskor és termék-előrejelzéskor.