Az SN 2 reakció (más néven bimolekuláris nukleofil szubsztitúció) egy szubsztitúciós reakció a szerves kémiában. Ez a nukleofil szubsztitúció egyik típusa, amikor egy nukleofil (többnyire elektronpár-vezető) megtámad egy elektronhiányos elektrofil centrumot, és kötődik hozzá, miközben a helyét egy rosszabb kötőképes, úgynevezett távozó csoport foglalja el. A folyamat során a belépő csoport egyetlen, összehangolt lépésben helyettesíti a kilépő csoportot, ezért a mechanizmust gyakran egylépésesnek nevezik. Mivel a reakció sebességét a sebességmeghatározó lépésében két résztvevő — a nukleofil és a szubsztrát — koncentrációja határozza meg, az elnevezésben szerepel a bimolekuláris szó. A szervetlen kémikusok körében az SN 2 reakciót gyakran cseremechanizmusként is ismerik.
Mechanizmus és átmeneti állapot
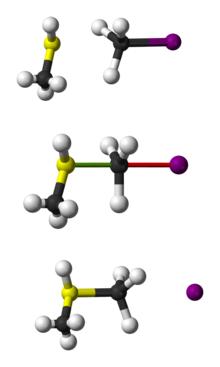
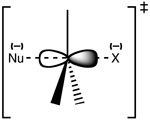
Az SN 2 mechanizmus lényege a hátsó (backside) támadás: a nukleofil ellentétes irányból közelíti meg a C–X (X = távozó csoport) kötet, és egyidejűleg részleges kötések alakulnak ki a nukleofil és a szén között, míg a kilépő csoport kötéserőssége csökken. Az átmeneti állapot jellemzője a részben ötkoordinált, pentakoordinált szerkezet (részleges kötésekkel a be- és kilépő csoportokhoz). Ennek következménye a Walden-inverzió: ha a kiindulási centrum sztereocentrum volt, a termék konfigúrációja 180°-kal fordul meg (inverzió).
Kinetika
Az SN 2 reakciók sebességtörvénye tipikusan másodrendű:
- rate = k [szubsztrát] [nukleofil]
Ez azt jelenti, hogy mindkét reaktáns koncentrációja befolyásolja a reakció sebességét, mert a sebességmeghatározó lépésben mindkét komponens részt vesz.
Főbb tényezők, amelyek befolyásolják az SN 2 reakciót
- Szubsztrát szerkezete: A sterikus gátlás döntő. Methyl > 1° > 2° esetén gyors, 3° gyakorlatilag kizárt az SN 2 miatt a nagy sterikus torlódás.
- Nukleofil erőssége: Erős, negatív töltésű és kevéssé delokalizált nukleofilek (például CN−, RS−, I−) gyorsítják az SN 2-t. A nukleofil reaktivitását csökkentik a szolvatációs kölcsönhatások és az elektronvonzó csoportok a közelben.
- Távozó csoport képessége: Jó távozó csoport (stabil töltés a kilépés után) — pl. I−, Br−, tosylát — elősegíti a reakciót. A fluorid rossz távozó csoport miatt általában lassú.
- Oldószer: Polar aprotikus oldószerek (pl. DMSO, DMF, aceton) kedvezőek, mert nem hidrogénezik erősen a nukleofilt, így az erősebbé válik. Polar protikus oldószerek (pl. víz, alkoholok) hidrogénezéssel gyengítik a nukleofilt, ezáltal lassítják az SN 2 reakciót.
- Hőmérséklet és koncentrációk: magasabb hőmérséklet és nagyobb nukleofil koncentráció gyorsíthatja a reakciót; a kinetika másodrendű voltából következik a koncentrációk jelentős szerepe.
Stereokémia
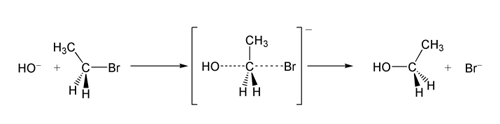
Sztereocentrumon végbemenő SN 2 reakció esetén a támadás hátsó irányú jellege miatt a termék konfigurációja megfordul (teljes vagy majdnem teljes Walden-inverzió). Ez fontos szempont szintetikus sztereokontrollban, például aszimmetrikus szintéziseknél vagy gyógyszerkémiai előállításnál.
Versengő folyamatok
Bizonyos körülmények között az SN 2 versenyez más reakciókkal:
- SN1: ha a szubsztrát stabil karbokationt tud képezni (pl. 3°), és az oldószer polar protikus, akkor az SN1 mechanizmus válhat dominánssá.
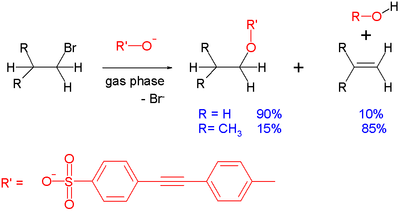
- E2 elimináció: erős, sterikusan nagy bázisok esetén (pl. t-BuO−) az E2 elimináció gyakran versenyez vagy felülírja az SN 2-t, különösen 2° és 3° szénközpontoknál.
Gyakorlati példák és alkalmazás
- CH3Br + CN− → CH3CN + Br− — egyszerű, gyors SN 2 példa, mivel a metilcsoportnál nincs sterikus gátlás.
- 2-bromobutan + OH− → 2-butanol (inverzióval) — másodlagos szénnél reagálhat SN 2 útvonalon, de a körülményektől függően versenyezhet az E2-vel.
- Szerves szintéziseknél az SN 2-t gyakran alkalmazzák alkilációk, funkciócsere lépések és védőcsoportok eltávolítása során, különösen, ha sztereokémiát kívánnak megőrizni vagy invertálni.
Összefoglalás
Az SN 2 egy egylépéses, bimolekuláris nukleofil szubsztitúció, amelyben a nukleofil hátulról támadva egyidejűleg kötődik a szénhez és kiszorítja a távozó csoportot. A reakció sebessége a szubsztrát és a nukleofil koncentrációjától függ, erősen befolyásolja a szubsztrát sterikája, a nukleofil ereje, a távozó csoport jósága és az oldószer típusa. Az SN 2 mechanizmus fontos eszköz a szerves szintézisben, különösen olyan esetekben, amikor sztereokémiai inverziót kívánnak elérni.