Az átrendeződési reakció olyan szerves reakció, amelyben a molekula szénváza átrendeződik. Az eredmény az eredeti molekula szerkezeti izomerje. Gyakran előfordul, hogy egy szubsztituens átkerül az egyik atomról egy másik atomra ugyanabban a molekulában. Az alábbi példában az R szubsztituens az 1. szénatomról a 2. szénatomra mozog:
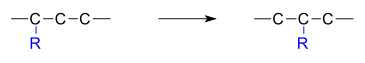
Molekulák közötti átrendeződések is végbemennek.
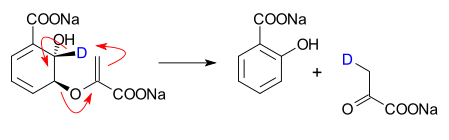
Mechanizmus — hogyan gondolkodjunk az elektronokról
A kémikusok gyakran nyilakkal ellátott ábrákat rajzolnak, amelyek azt mutatják, hogy az átrendeződési reakció során hogyan kerülnek át az elektronok a kötések között. Sok szerves kémia tankönyvben találhatók ilyen ábrák. Ezek azonban nem mondják el a reakció mechanizmusának teljes történetét.
Fontos megkülönböztetni két alapvető lehetőséget:
- Lépésenkénti (stepwise) mechanizmusok: a reakció közben stabil vagy félstabil köztesek (például karbokation, gyök, vagy anion) keletkeznek. Tipikus példák: karbokationos 1,2-eltolódások, ahol a váz átrendeződése egy karbokation stabilizációjának megfelelő irányban történik.
- Koncertált (concerted) mechanizmusok: az elektronok átrendeződése egyetlen, összehangolt esemény; nincs jól elkülöníthető, hosszú élettartamú köztes. Ilyenek például a periciklusos reakciók (sigmatropikus, elektrocyklook és cikloadíciós típusok), amelyeknél az orbitális kölcsönhatások döntőek és érvényesülnek a Woodward–Hoffmann-szabályok.
Az ábrákon mutatott elektronnyilak hasznosak a gondolkodáshoz, de nem mindig tükrözik fizikailag a elektronok folytonos elmozdulását; gyakran egyszerűsített, "mechanizmus-sémákat" adnak.
Típusok és tipikus példák
Az átrendeződési reakciók széles skálája létezik; néhány fontos típus:
- 1,2-átrendeződések (1,2-shift): kis távolságú (szomszédos) eltolódás, gyakran karbokationos köztesek révén. Ide tartozik a hidrid- és alkilátvándorlás, valamint a Wagner–Meerwein típusú átrendeződések. Ezeknél a vándorlás célja általában egy stabilabb karbokation kialakítása vagy feszültségcsökkentés (például gyűrűléptetés).
- Wagner–Meerwein átrendeződés: tipikus carbocation-közvetített alkilvándorlás; gyakori terület a szteroid- és terpénszintézisben. Az egyik klasszikus példa az izoborneol → kamfén átalakulás:
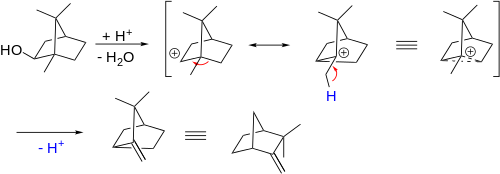
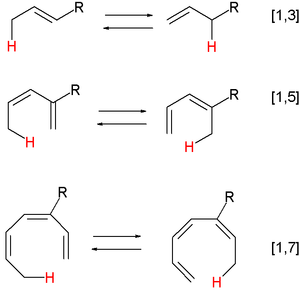
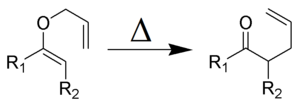
- Periciklusos reakciók (sigmatropikus, elektrocyklook, cikloadíciók): ezekben a reakciókban az orbitális szimmetria és a Woodward–Hoffmann-szabályok határozzák meg, hogy egy adott eltolódás engedélyezett-e hő vagy foton hatására. Jó példák: Claisen-átcsoportosítás, Cope-átalakulás, [3,3]-sigmatropikus eltolódások.
- Allilikus átrendeződések: az allilpozícióban történő elektron- vagy töltésátrendeződés; gyakran ionos jellegűek és rezonancia-stabilizáció játszik szerepet.
- Baeyer–Villiger-reakció: a karbonil-oxidáció során acilvándorlás történik az oxigénre; a reakció során vazoalapú átrendeződés zajlik (oxidáció + átrendeződés), fontos ipari alkalmazásokkal.
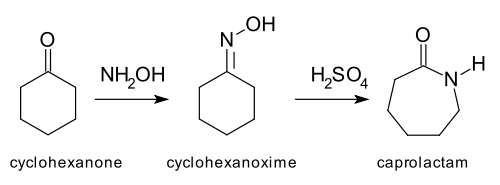
- Beckmann- és pinacol-átcsoportosítás: a Beckmann-reakciónál oximból keletkező amíd átépülése, a pinacolnál diolból karbonil képződik alkilvándorlással; mindkettő jól ismert szerves transzformáció.
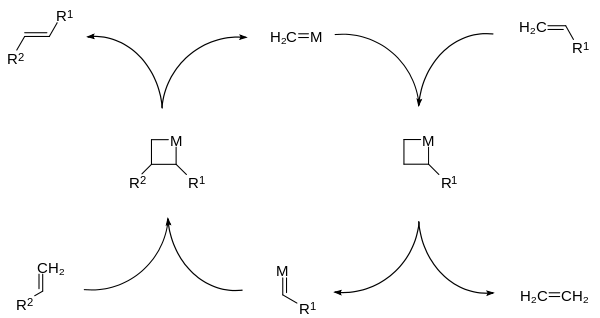
- Olefin-metatézis: bár nem klasszikus "átvándorlás" egyetlen molekulán belül, a metatézis során kettős kötések fel- és újraírása történik fém-karben katalizátorok (pl. Grubbs-, Schrock-katalizátorok) közreműködésével, ami szerkezetátalakító hatású.
Mi hajtja az átrendeződést? (energetika és motiváció)
- Stabilitás növelése: stabilabb karbokation, jobb konjugáció vagy aromás jelleg elérése.
- Feszültségcsökkentés: gyűrűfeszültség oldása (például hídvázak esetén).
- Termodinamikai preferencia: a végtermék energiaszempontból kedvezőbb lehet (stabilabb, szimmetrikusabb, kisebb belső feszültségű).
- Katalízis és külső tényezők: sav-katalízis, bázis, fémkatalizátorok vagy hő hatására egyes utak preferálódnak.
Stereokémia és bizonyítékok
Az átrendeződések stereokémiai kimenetele változó: a koncertált folyamatok általában sztereo-szelektívek lehetnek (megtartva vagy megfordítva bizonyos konfigurációkat, attól függően, hogy suprafaciális vagy antarafaciális a vándorlás), míg a lépésenkénti mechanizmusoknál racemizáció vagy konfigurációvesztés fordulhat elő, ha planarizált karbokation keletkezik.
A mechanizmusok igazolására gyakran alkalmaznak izotópos jelöléseket (13C, 2H), kinetikai vizsgálatokat, köztesek befogását, spektroszkópiát és számításos kémiai modellezést.
Gyakorlati jelentőség és alkalmazások
- Szintetikus kémia: komplex molekulák építésénél az átrendeződések lehetővé teszik gyors vázátalakítást, gyűrű-átalakítást vagy funkciócsoport-migrációt.
- Ipari folyamatok: bizonyos átrendezések ipari szintű előállításokban hasznosak (pl. Szent-Györgyi vagy más finomkémiai transzformációk).
- Biokémia: élő rendszerekben enzimkatalizált átrendeződések is fontosak, amint azt a fenti Isochorismate Pyruvate Lyase példa mutatja.
Összefoglalás és praktikus tanácsok
- Az átrendeződési reakciók sokfélék: lehetnek ionosak, gyökösök vagy koncertált periciklusos folyamatok.
- Az elektronnyilak rajzolása hasznos gondolkodási eszköz, de mindig ellenőrizzük a mechanizmus azonosságát kísérleti adatokkal (izotópjelölés, kinetika, spektroszkópia).
- A reakciók tervezésekor vegyük figyelembe a termodinamikai és kinetikai tényezőket, valamint a lehetőséget, hogy katalizátorral (sav, fém) vagy hővel a megfelelő irányba tereljük az átrendeződést.
Három fontos átrendeződési reakció az 1,2-átrendeződés, a periciklusos reakciók és az olefin-metatézis — mindegyik más mechanisztikus és alkalmazási jellemzőkkel bír, ezért külön-külön is érdemes részletesen tanulmányozni őket.
.png)