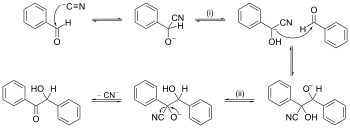
A reakciómechanizmus lépésről lépésre leírja, hogyan működik egy kémiai reakció. Általában csak az általános változás látható egy reakcióban. A közben keletkező dolgok túl gyorsan reagálnak ahhoz, hogy láthatóvá váljanak. Ezeket intermediereknek nevezzük, és az egyik intermedierből a másikba lépve egy átmeneti állapotot lépünk át. Fontos azonban megérteni az összes lépést, amely a teljes változást eredményezi. Ez azért van így, mert így megérthetjük a nehezebb reakciókat, vagy megpróbálhatunk egy reakciót egy bizonyos módon működésre bírni.
Sokféle reakciómechanizmus létezik. A szerves kémiában a leggyakoribbak a nukleofil szubsztitúció, az elimináció és az addíció. Az emberek néha nyilazással rajzolják meg, hogyan mozognak az elektronok egy reakció során. Így könnyen láthatóvá válik, hogy a folyamat során milyen kötések jönnek létre, és melyek szakadnak meg.
Az elemi lépések és a molekuláriság
Egy reakciómechanizmus elemi lépések sorozatából áll — minden elemi lépés egyszerre, egyetlen eseményként megy végbe. Az elemi lépések lehetnek:
- unimolekuláris (egymolekula-átalakulás),
- bimolekuláris (két részecske ütközése vagy kölcsönhatása),
- trimolekuláris (ritka, három részecske együttlépése).
A reakciók gyorsaságát és a koncentrációfüggést (rend) az elemi lépések határozzák meg; egy soklépéses mechanizmus esetén a lassú lépés lesz a reakció rátáját meghatározó, azaz a rate-determining step.
Átmeneti állapotok és energiapálya
Minden elemi lépés áthalad egy átmeneti állapoton, amelyet a reakcióenergiai görbén csúcspont jelöl. Ez határozza meg az adott lépés aktiválási energiáját. A teljes mechanizmus energetikai leírását gyakran reakciókoordináta-diagramon ábrázolják, ahol jól látszanak az intermedierek energiáinak különbségei és az egyes aktiválási gátak magasága.
Gyakori fogalmak röviden
- Intermedier: rövid élettartamú, de valódi részecske (pl. karbokation, radikál), amelyet kísérletekkel vagy számítással lehet kimutatni vagy igazolni.
- Átmeneti állapot: nem megfigyelhető, a reakció során kialakuló, legmagasabb energiájú konfiguráció.
- Katalizátor: új, alacsonyabb energiájú útvonalat biztosít, így csökkenti az aktiválási energiát; maga a katalizátor a reakció végén visszaáll eredeti formájára.
- Elektronnyíl (curly arrow): a szerves kémiában használt jelölés az elektronpárok mozgásának szemléltetésére.
Példák mechanizmusokra
- SN1: kétlépéses nukleofil szubsztitúció; első lépésben kilép egy csoport és karbokation képződik (lassú), majd a nukleofil kapcsolódik. Jellemző a racemizáció sztereoizomerizáció.
- SN2: egylépéses nukleofil támadás és kilépés egyszerre; hátulról történő támadás invertálja a szerves központ konfigurációját. Gyorsan csökken a szubsztituált szén környezeti hinderével.
- E1 és E2 elimináció: E1 hasonló az SN1-hez (karbokationos intermedier), E2 pedig egylépéses protoneltávolítás és csoportkiválás együttesen; E2-ben a sztereokémia fontos (anti-elimination).
- Radikállánc-reakció (pl. metán-halogenálása): initáció (radikálképződés), propagáció (radikálok folyamatos létrehozása és fogyasztása), termináció (radikálok párosodása). Ez gyakori a radikálmechanizmusoknál.
Hogyan vizsgálják a mechanizmusokat?
Néhány gyakori módszer:
- Kinetikai mérések: hogyan függ a reakció sebessége a koncentrációktól és hőmérséklettől — segít felderíteni az elemi lépéseket és a rátát meghatározó lépést.
- Izotópcímkézés: nehéz izotópok (pl. D, 13C) beépítésével követhető, hogy mely kötés szakad fel vagy keletkezik.
- Spektroszkópia: NMR, IR, UV–Vis, EPR stb. segítségével lehet intermediereket vagy gyorsan átmeneti állapotok jeleit detektálni.
- Trapolás: reaktív intermediereket csapdába ejtenek stabilizáló reagensekkel, hogy kimutathatók legyenek.
- Számítógépes kémiák: DFT és más elméleti módszerek használhatók átmeneti állapotok és energiagörbék meghatározására.
Miért fontos a reakciómechanizmus ismerete?
- Segít megérteni és előre jelezni a reakciótermékek szelektivitását és hozamát.
- Lehetővé teszi katalizátorok és reakciófeltételek tervezését a kívánt útvonal előnyben részesítéséhez.
- Segít a melléktermékek csökkentésében és biztonságos, hatékony folyamatok kialakításában.
Összefoglalva: a reakciómechanizmus a kémiai transzformáció belső „forgatókönyve” — elemi lépések, intermedierek és átmeneti állapotok sorozata, amely megmutatja, hogyan jönnek létre és bomlanak a kötések. A mechanizmusok megértése alapvető a modern kémia kutatásában és gyakorlati alkalmazásaiban.