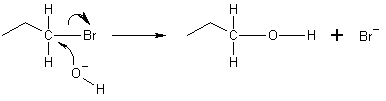
A nukleofil olyan faj, amely egy reakcióban kémiai kötés kialakításához elektronpárt ad egy elektrofilnek. Minden szabad elektronpárral rendelkező molekula vagy ion nukleofil lehet. Ezt az elektronpárt magányos párnak nevezzük. Mivel a nukleofilek elektronokat adományoznak, megfelelnek a Lewis-bázisok definíciójának.
A nukleofil a nukleofil vonzását írja le a magokhoz. A nukleofilitás, amelyet néha nukleofil erősségnek is neveznek, egy anyag nukleofil jellegére utal, és gyakran használják az atomok vonzásának összehasonlítására.
A semleges nukleofil reakciókat oldószerekkel, például alkoholokkal és vízzel "szolvolízisnek" nevezzük. A nukleofilek nukleofil szubsztitúciós reakciókban is részt vehetnek. Ezekben a reakciókban a nukleofil vonzódik egy teljes vagy részleges pozitív töltéshez.
Mit jelent nukleofilitás — kinetika és termodinamika
A nukleofilitás két oldalról értelmezhető: egyrészt termodinamikai értelemben egy nukleofil mennyire kedvezően alakít ki kötést egy adott elektrofillel (ez a végső termék stabilitásában látszik), másrészt kinetikai értelemben milyen gyorsan reagál (ez a reakciósebességet határozza meg). Gyakran a gyakorlatban a reaktivitást, azaz a reakciósebességet értjük nukleofilitás alatt.
Főbb tényezők, amelyek befolyásolják a nukleofilitást
- Töltés: az anionok általában erősebb nukleofilek, mint a semleges molekulák (például OH– erősebb, mint H2O).
- Elektronegativitás: alacsonyabb elektronegativitású atomok kevésbé tartják erősen elektronjaikat, ezért gyakran reaktívabb nukleofilek.
- Polarizálhatóság: nagyobb, könnyen polarizálódó ionok (pl. I–) jól stabilizálják a tranzíciós állapotot és gyakran erősebb nukleofilek protikus oldószerekben.
- Oldószer hatása: protikus oldóserek (pl. víz, alkoholok) hidrogénkötéssel "befogják" az anionokat, ami csökkenti azok nukleofilitását; aprotikus poláris oldószerek (pl. DMSO, acetontitril) viszont gyakran növelik az anionok nukleofilitását.
- Sztérikus hatás: nagy, elágazó csoportok körülményeket nehezebbé teszik az elektrofilhez való közelítést, így csökkentik a nukleofilitást.
- HSAB-elv (hard–soft acid–base): a "soft" nukleofilek jobban reagálnak "soft" elektrofilekkel, és fordítva. Ez segít megmagyarázni, miért kedvelnek bizonyos párkapcsolatok speciális reakcióutakat.
Gyakori nukleofil típusok és példák
- Anionok: OH–, RO– (alkoxidok), CN–, RS– (tiolátok), halidionok (Cl–, Br–, I–).
- Semleges nukleofilek: NH3, R2O (éterek), RSH (tiolok) — ezek gyakran gyengébb nukleofilek azonos feltételek mellett, mint az anionok.
- Ambident nukleofilek: például CN–, amely C- vagy N-atomon keresztül is támadhat; a támadási hely függ a reakciótípustól és a környezettől.
Nukleofil reakciótípusok
- Nukleofil szubsztitúció (SN):
- SN2: egylépcsős, szimultán kötésképződés és kötésbontás; a reakciósebesség erősen függ a nukleofil koncentrációjától. Erős, kevéssé sztereospecifikus nukleofilek és jó leaving group kedveznek ennek az útnak.
- SN1: kétszakaszos, elhagyó csoport leválása után képződik karbokation, majd azt támadja a nukleofil. Itt a nukleofil erőssége kevésbé fontos a sebesség szempontjából; a karbokation stabilitása döntő.
- Szolvolízis: különleges eset, amikor az oldószer maga a nukleofil (például víz vagy alkoholok). Sok SN1 reakció szolvolízis formában zajlik le.
- Addíció a kettős kötéshez vagy karbonilhoz: nukleofilek támadhatják a szén–szén kettős kötést (pl. epoxidnyitás) vagy a karbonil-szenet (nukleofil addíció), kötést hozva létre.
- Transzmetalláció és más szervorganometál reakciók: itt nukleofilek (pl. organometallionok) vesznek részt, amelyeknél a reakciók mechanikája a kötés karakterétől függően eltérő lehet.
Nukleofil vs. bázis — mi a különbség?
Bár mindkettő elektronpárt ad, a nukleofil és a bázis eltérő szerepet tölt be: a bázis proton (H+) elfogására specializálódik, míg a nukleofil elektromosan vagy részlegesen pozitív szénatomot (vagy más elektrofil központot) támad meg. Sok esetben a legerősebb bázisok jó nukleofilek is, de nem minden: például F– nagyon erős bázis aprotikus környezetben, de protikus oldószerekben nukleofilitása relatíve gyenge a szoros szolvátképződés miatt.
Gyakorlati megfontolások szintetikus kémiában
A nukleofil megválasztása során figyelembe kell venni a reakció mechanizmusát (SN1 vagy SN2), az oldószert, a kívánt szelektivitást és a potenciális mellékreakciókat (például elimináció). A jó leaving group megléte és a reakciókörülmények optimalizálása alapvető a kívánt szubsztitúció eléréséhez.
Összefoglalva: a nukleofilok olyan reakciópartneretek, amelyek elektronpárral támadnak elektrofileket, és nukleofilitásukat több tényező — töltés, polarizáció, oldószer, sztérika és HSAB-jelleg — határozza meg. Ezek a tulajdonságok döntik el, hogy egy adott nukleofil mennyire gyorsan és mely mechanizmuson keresztül reagál.