A szerves kémiában eliminációs reakcióról akkor beszélünk, amikor néhány atom vagy atomcsoport kiválik egy nagyobb molekulából. Általában kettős vagy hármas kötés jön létre e reakció során. Az elimináció fontos módja annak, hogy telített vegyületekből telítetlen (alkének, alkinek) rendszereket kapjunk, és sok szerves szintézis alaplépése.
E1 és E2 — alapfelépítés
Az eliminációs reakciókat gyakran két tipikus mechanizmusra szokás bontani: E1 és E2. A legfontosabb különbségek röviden:
- E1: kétlépéses mechanizmus. Első lépésben kilép a távozó csoport, és egy karbokation kialakul; második lépésben egy bázis elveszi a β‑hidrogént, és kialakul a kettős kötés. Kinetikailag elsőrendű a szubsztrát koncentrációjára (rate = k[substrate]).
- E2: egylépéses, együttes (koncert) folyamat; a bázis egyszerre távolítja el a protont és a távozó csoport kilép. Gyakran másodrendű kinetikát mutat (rate = k[substrate][base]).
Mikor melyik mechanizmus valószínű?
- Szubsztrát szerkezete: tercier szén közvetlenül a távozó csoport mellett általában kedvez az E1-nek (könnyen stabilizálódó karbokation). Szekunder lehet mindkettő; elsődleges általában E2 (karbokation kialakulása ritka).
- Bázis/nukleofil erőssége: erős, sterikusan kicsi bázisok E2-t támogatnak. Gyenge bázisok és jó távozó csoportok polar protikus oldószerben inkább E1-re vezetnek.
- Oldószer: polar protikus oldószerek stabilizálják a karbokationt → E1 előnyösebb. Polar aprotikus oldószerek növelik a bázis/ nukleofil reaktivitását → E2 valószínűbb.
- Hőmérséklet: magasabb hő általában az eliminációt (E) részesíti előnyben a szubsztitúcióval (SN) szemben.
Stereokémia, szelektivitás és elméleti szabályok
Az E2 reakciók erősen stereokémia-függőek: gyakran szükség van arra, hogy az eltávolítandó β‑hidrogén és a távozó csoport anti‑periplanárisan (egymással 180°‑ban) helyezkedjenek el. Ez különösen fontos ciklohexán-szerű gyűrűkben, ahol csak axialis helyzetek adnak megfelelő geometriát.
Az eliminációs termékekre vonatkozó gyakori szabályok:
- Zaitsev-szabály: általában a kevésbé hidrogénezett (stabilabb, több szubsztituált) alkén a főtermék.
- Hofmann‑szelektivitás: nagy, sterikusan akadályozott bázisok használatakor gyakran a kevésbé szubsztituált (Hofmann) alkén lesz a főtermék.
Egyéb mechanizmus: E1cB
Van egy harmadik, kevésbé gyakori mechanizmus, az E1cB (elimináció, ahol először deprotonálás történik). Ilyenkor a β‑hidrogént először elveszik, stabilizált karbanion (vagy enolát) keletkezik, majd a rossz távozó csoport kilép. Ez fordul elő például akkor, ha a β‑hidrogén különösen savas (például nitro- vagy karbonilcsoport mellett), vagy ha a távozó csoport nagyon gyenge, és a karbanion relatíve stabil.
Karbokation‑átrendeződések
E1 mechanizmus esetén a karbokation intermedierként történő kialakulása lehetőséget ad hidrid vagy alkil eltolódásokra (rearrangements). Ezek az eltolódások más, stabilabb karbokationt hozhatnak létre, és így megváltoztathatják a kapott alkén szerkezetét a várthoz képest — ezért fontos figyelembe venni őket szintézis tervezésekor.
Példák és gyakorlati megjegyzések
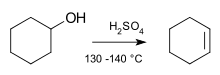
Az alkoholokkal gyakori eliminációs reakció történik. Ha erős sav van a közelben, egy vízmolekula eliminálódhat a kettős kötés kialakulásához: az alkohol protonálódik, a víz mint jó távozó csoport kilép, és ha a körülmények engedik, E1 mechanizmussal alkén képződik. Ez jellemzően sekundér és tercier alkoholoknál könnyebb; elsődleges alkoholoknál a közvetlen karbokation‑képződés ritka, és gyakran E2 típusú vagy más mechanizmus szükséges.
Tipikus laboratóriumi példák:
- Alkil‑halogenidek eliminációja erős bázissal → alkének (E2 gyakori, de megfelelő körülmények között SN2 is verseng).
- Alkoholok savas dehidratációja (H2SO4, H3PO4, vagy fűtés) → alkének (E1 gyakori másod- és tercier esetekben).
- Bázis‑vezérelt elimináció α‑pozícióban savas hidrogénekkel (E1cB jelleg) — például bizonyos karbonil- vagy nitrocsoportok mellett.
Összefoglaló gondolatok
Az eliminációs reakciók (E1, E2, E1cB) megértése a szubsztrát szerkezetén, a bázis/oldószer jellemzőin, a hőmérsékleten és a távozó csoport minőségén múlik. A gyakorlatban gyakran verseny zajlik az elimináció és a szubsztitúció között (SN1/SN2), ezért az optimális feltételek megválasztása kulcsfontosságú a kívánt termék eléréséhez.