A kémiában az elektrofil egy olyan molekula vagy atom, amely elektronpár befogadására vagy elektronok átmeneti megszerzésére hajlamos egy másik részecskétől. Gyakran rendelkezik részleges vagy teljes pozitív töltéssel, ezért sok elektrofil az Lewis-sav kategóriájába tartozik (elektronpár-akceptor). Az elektrofilek fontos szerepet játszanak mind az szervetlen, mind az szerves kémiai reakciókban.
Tulajdonságok és jellemzők
- Pozitív töltés vagy részleges pozitív jelleg: Az elektrofilek lehetnek kationok (pl. H+), vagy olyan semleges molekulák, amelyekben egy atom erősen poláros kötés miatt részlegesen pozitívvá válik.
- Elektronszegény központ: Az a hely, amelyhez a nukleofil kapcsolódik, elektronhiányos és elektronpár felvételére képes.
- Lewis-sav viselkedés: Sok elektrofil elektronpár-elfogóként működik, ezért Lewis-savként írható le.
- Reagálhat nukleofilekkel: Az elektrofileket általában nukleofil részecskék támadják meg, amelyek elektronpár- vagy elektronban gazdag központtal rendelkeznek.
Példák
Néhány gyakori elektrofil:
- Protonok (H+): savas közegben a proton elektrofilként működik és addíciós vagy szubsztitúciós lépéseket indíthat.
- HCl: a H+ része elektrofil, a Cl− a nukleofil rész.
- karbonilcsoportok (C=O): a karbonil karbonja részlegesen pozitív, ezért nukleofilek támadhatják meg.
- Karbokationok (R–C+–R): erősen elektrofilek, gyakori reakcióköztes állapotok szerves reakciókban.
- Akil- és acil cationok, nitrozó és nitronium ionok (NO2+), halogénmolekulák vagy halogénkationok (Br+, Cl+): tipikus elektrofilek nitrálásnál, halogénezésnél, acilezési reakcióknál.
- Oxidálószerek: sok oxidálószer elektronfelvétel révén viselkedik, ezért elektrofil jellegű lehet bizonyos körülmények között.
Fő reakciótípusok, ahol az elektrofilek szerepelnek
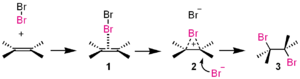
- Elektrofil addíció: Alkénekre vagy alkénekre poli- és egyszeres addíciós reakciók, amikor az elektrofil (pl. H+) először kötődik a kettős kötéshez, majd a keletkező szigma-komplexet nukleofil támadja.
- Elektrofil aromás szubsztitúció (EAS): aromás gyűrűk nitrálása, szulfonálása, halogénezése és Friedel–Crafts acilezése mind elektrofil köztes lépést tartalmaznak, ahol a gyűrű átmenetileg elveszti aromás jellegét a elektrofil kapcsolódása miatt.
- Acilezés és alkilezés: acil– vagy alkil-kationokkal (vagy ezek előállításával) történő reagálások.
- Nukleofil támadás karbonilokra: a karbonil karbonjára irányuló nukleofil addíciók és kondenzációk (pl. észterképződés, aminok hozzáadása) szintén elektrofil centrummal dolgoznak.
Milyen tényezők növelik egy részecske elektrofil jellegét?
- Pozitív töltés: formális kationok mindig erős elektrofielek.
- Poláros kötés vagy nagy elektronegatívitású szomszédos atomok: ha egy atomot erősen vonzó szomszédok vesznek körül, az atom részlegesen pozitív lesz (például a karbonilcsoportban a C).
- Induktív és mezomer effektusok: elektronelvonó csoportok (pl. –NO2, –CO–) növelik a központi atom elektrofilebbé válását.
- Rezonalizáció hiánya vagy gyenge stabilizáció: kevéssé stabil, elektronhiányos központok erősebb elektrofilek, hacsak nincs jelentős rezonancia-stabilizációjuk.
- Savas környezet és katalízis: savak protonálhatnak bizonyos csoportokat, így ezekből erős elektrofilek lesznek; Lewis-savak is aktiválhatnak több funkciós csoportot.
Mechanizmusok — hogyan történik a nukleofil támadás?
Általában az elektrofil és a nukleofil közötti reakció során:
- az elektrofilhez való közeledéskor kialakul egy átmeneti komplex (pl. karbokation vagy szigma-komplex),
- továbblépve a nukleofil átad egy elektronpárt az elektrofil részére,
- ennek eredményeként új kötés jön létre és gyakran oldaltermék vagy ionos melléktermék is keletkezik.
Gyakorlati megjegyzések
- Az elektrofilek reakciókészsége nagyban függ a környező oldószertől, hőmérséklettől és a jelenlévő katalizátoroktól.
- Bizonyos reakciókban (például katalitikus ciklusokban) az elektrofil képződése és eltűnése határozza meg a reakció sebességét és szelektivitását.
- A biztonsági előírásokat betartva kell kezelni olyan erősen elektrofil reagenseket, mint a nitroniumiont vagy erős acilező szereket, mivel ezek gyakran korrodálóak vagy erősen kipárolgóak lehetnek.
Összefoglalva: az elektrofil olyan elektronhiányos részecske, amelynek alapvető szerepe van a kémiában, különösen a különféle addíciós és szubsztitúciós reakciókban. A viselkedését és reaktivitását determináló tényezők ismerete segít megjósolni és tervezni a kívánt kémiai átalakulásokat — legyen szó egyszerű sav–bázis kölcsönhatásokról vagy bonyolult szerves szintézisekről.