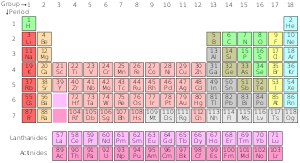
A kémiai elemek periódusos rendszere az ismert kémiai elemek rendszerezett listája, amely az elemek fő tulajdonságai és egymáshoz való viszonyuk áttekintésére szolgál. A táblázatban az elemek atomi számuk sorrendjében vannak elhelyezve, kezdve a legalacsonyabb, egyes számmal, a hidrogénnel. Egy elem atomi száma megegyezik az adott atommagban lévő protonok számával. A periódusos rendszerben az elemek periódusokba és csoportokba vannak rendezve: a vízszintes sorokat periódusoknak, a függőleges oszlopokat pedig csoportoknak nevezzük.
Periódusok és csoportok — hogyan kell olvasni a táblázatot
Minden periódusban az elemek egymást követő atomi szám szerint helyezkednek el. A jelenleg ismert elemek a 1–7. periódusokban találhatók; a 8. periódusban elméleti és még nem stabil, szintetikus elemek lehetségesek. Az 1. periódusból csak két elem áll: a hidrogén és a hélium. A 2. és 3. periódusokban mindegyikben 8-8 elem található, a középső periódusok (különösen a 4. és 5.) hosszabbak, mert több elektronhéj és alhéj töltődik fel.
Az elemek egy oszlopa a táblázatban csoport. A standard periódusos rendszer 18 csoportból áll, melyeket az IUPAC ma arab számokkal (1–18) számoz. Az egy csoportba tartozó elemek elektronjai hasonló módon rendeződnek, különösen az értékelektronok száma szerint, ami hasonló kémiai tulajdonságokat eredményez. Például a 18-as csoport a nemesgázoknak felel meg: ezek atomok általában gázhalmazállapotúak és kémiai reakciókban tompák (kevésbé reagálnak).
Főbb elemosztályok és jellegzetes csoportok
- Alkáli fémek (1. csoport) — nagyon reakcióképes fémek (kivéve a hidrogén különleges esetét); lágyak és könnyen oxidálódnak.
- Alkáli földfémek (2. csoport) — szintén reaktív fémek, de kevésbé, mint az alkáliak.
- Átmenetifémek (3–12. csoport) — jól vezetnek hőt és elektromosságot, sokféle oxidációs állapotot mutatnak; fontos ipari katalizátorok.
- Halogének (17. csoport) — nagyon reaktív nemfémek, erősen elektronvonzóak.
- Nemesgázok (18. csoport) — kémiailag legkevésbé reaktív elemek.
A táblázatban található elemek nagyobb csoportosítása: fémek, metalloidok és nemfémek. A fémesség általában balra lent növekszik (például a cézium nagyon fémes), míg a nemfémes tulajdonságok jobbra és felfelé erősödnek (például a hélium gázként viselkedik).
Elektronkonfiguráció és a periódusosság oka
A periódusos rendszer ismétlődő mintázatai (periodicitás) az elektronok elhelyezkedéséből származnak: különösen az elektronhéjak és alhéjak feltöltődéséből. Az elemek helye megmutatja, hány elektron töltődik az adott külső héjra (értékelektronok), ez határozza meg kémiai viselkedésüket. A táblázat blokkokra bontható (s-, p-, d-, f-blokk) az alapján, melyik alhéj töltődik fel éppen.
Periodikus trendek
- Atomsugár: általában balról jobbra csökken (nagyobb vonzóerő a mag részéről), fentről lefelé nő (több elektronhéj).
- Ionizációs energia: az az energia, amely egy elektront eltávolít; általában balról jobbra nő, fentről lefelé csökken.
- Elektronegativitás: az atom más atom elektronjainak vonzása; balról jobbra általában nő, fentről lefelé csökken.
Ritkaföldfémek, lantanoidok és aktinoidok
A táblázat alján gyakran külön sorokban találjuk a lantanoidokat és aktinoidokat (az úgynevezett f-blokk elemei). Ezek a ritkaföldfémek és megfelelőik fontos szerepet játszanak a modern technológiákban (mágnesek, katalizátorok, nukleáris reaktorok).
Történet és jelentőség
A periódusos rendszert a Dmitrij Ivanovics Mendelejev (1834–1907) orosz kémikus fejlesztette ki. Mendelejev az elemeket akkor még részben ismert tulajdonságaik és rendezett atomtömegeik alapján helyezte el, és a táblázatába üres helyeket hagyott olyan elemek számára, amelyeket még nem ismertek — ezzel később pontosan megjósolta több ismeretlen elem tulajdonságait. Később Henry Moseley kimutatta, hogy az atomok rendezése helyes alapja az atomi szám (protonok száma), nem pedig csupán az atomtömeg, ami tovább pontosította a táblázatot.
Az IUPAC 1990-ben hivatalosan is elfogadta a ma használt, arab számokkal jelölt csoportszámozást, ezzel kiváltva a korábbi római számokkal és eltérő jelölésekkel dolgozó rendszereket. Az elemek közül ma már több szintetikus, rövid élettartamú, nehéz (szupernehéz) elem is ismert; például a 101-es rendszámú elemnek Mendelejev után a mendelevium nevet adták.
Gyakorlati alkalmazások és olvasási tippek
A periódusos rendszer ismerete segít megérteni és előre jelezni az elemek kémiai viselkedését, reakcióképességét és vegyületeik tulajdonságait. Amikor egy elemet keresünk a táblázatban, érdemes megfigyelni:
- az atomi számát (protonok száma);
- az átlagos atomtömeget (izotópok miatti érték);
- a csoportját (azonos csoport tagjai hasonló kémiai viselkedést mutatnak);
- a periódust (melyik héj töltődik éppen).
Például a hidrogén sajátos helyzetben van: bár egyes rendszerek a 1. csoporthoz sorolják, tulajdonságai egyes tekintetben a halogénekre emlékeztetnek. A cézium és más alkáli fémek erősen reagálnak vízzel, míg a hélium inert gázként stabil és szinte nem reagál.
Összefoglalás
A periódusos rendszer tehát nem csupán elemek listája: strukturált eszköz, amely megmutatja az elemek közötti rendszerszerű kapcsolatokat, kémiai viselkedésüket és trendjeiket. Mindennapi tudományos és ipari alkalmazások alapja, segítve az új anyagok felfedezését és az elemek gazdaságos, célzott felhasználását.