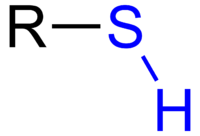
A tiol olyan molekula, amely R-SH csoporttal rendelkezik. A tiolok olyanok, mint az alkoholok, amelyeknél egy oxigénatomot kénatomra cseréltek. Gyakran nagyon erős és rossz szaguk van. A tiolokat azért adják a földgázhoz, hogy az emberek érezzék a szagát. A metánnak ugyanis nincs szaga, de nagyon könnyen felrobbanhat.
Fizikai tulajdonságok
A tiolok általánosságban polárosabbak, mint a szénhidrogének, de gyengébb hidrogénkötést képeznek, mint az alkoholok, ezért általában alacsonyabb forráspontjuk van az azonos molekulatömegű alkoholokhoz képest. Sok alifás tiol erős, kellemetlen, jellegzetes szagú (például a metil- és etil-tiolok szaga). A szagnak köszönhető, hogy nagyon kis koncentrációban is könnyen észlelhetők — emiatt használják őket gázzal kapcsolatos figyelmeztető anyagként (odoránsokként).
Kémiai tulajdonságok és reakciók
A tiolok nagyon könnyen oxidálódnak. Egyszerű oxidációs reakció során két tiolból diszulfid (R-S-S-R) képződik, ez a folyamat fontos a fehérjék szerkezetében és a kémiai szintézisekben egyaránt. Erősebb oxidálószerekkel a tiolok tovább oxidálhatók sulfenic (R-SOH), sulfinic (R-SO2H) és sulfonic (R-SO3H) savakká.
Elég savasak is, jobban, mint az alkoholok: a legtöbb tiol pKa értéke körülbelül 10–12 (alkoholoknál ez általában sokkal magasabb), tehát könnyebben adnak le protont. Ha a protont egy bázis elveszi, a tiol nukleofillá válhat (R-S−, thiolát anion). A thiolátok erős nukleofilek, ezért olyan reakciókat tudnak végrehajtani, mint a nukleofil szubsztitúció (például alkil-halidek átalakítása tiolokká vagy tioéterekké).
A tiolokra jellemző további reakciók és szerepek:
- Diszulfidképződés: 2 R-SH → R-S-S-R + 2 H+ + 2 e− — fontos biokémiai és kémiai folyamat.
- Redukció: a diszulfidok visszaredukálhatók tiolokká (pl. ditiotreitol, β-merkaptoetanol használatával).
- Alkilálás és acilezés: a tiolák könnyen alkilezhetők, így tioéterek (R-S-R') vagy thioészterek képződhetnek.
- Radikáladdíciók (thiol-ene reakciók): a tiolcsoportok gyakran vesznek részt radikál addíciós származtatásokban polimerizációs és szintetikus alkalmazásokban.
Biológiai jelentőség
Az egyik természetes aminosav, a cisztein, szerkezetében egy tiol található. A cisztein oldalláncának tioolja alapvető szerepet játszik a fehérjék térszerkezetének stabilizálásában (diszulfidkötések kialakításával), redoxszabályozásban és katalízisben. A tiolcsoportok részei olyan fontos biomolekuláknak is, mint a glutation, amely sejtszintű antioxidáns és redox-regulátor.
Előállítás és alkalmazások
- Előállítás: tiolokat lehet előállítani alkil-halidek nukleofil cseréjével kénhidrogénnel vagy tiolátokkal, tiourea közbeiktatásával (isothiouronium-só hidrolízise), vagy diszulfidok redukciójával.
- Alkalmazások: odoránsok (földgáz érzékeltetésére), polimerkémia (thiol-ene), szintetikus kémia (védőcsoportok, szulfidok előállítása), fémkötnék kialakítása katalízisben és biológiában.
Biztonság és környezeti hatások
Sok tiol gyúlékony és rossz szagú; kis koncentrációban is erősen érezhetők. Néhány tiol mérgező lehet nagyobb dózisban, és irritáló hatásuk is lehet. A természetben és iparban keletkező tiolok és diszulfidok szagproblémákat okozhatnak, ezért gyakran kezelik vagy átalakítják őket szagsemlegesítő eljárásokkal. Gázokhoz adagolt tiolok (odoránsok) életmentőek lehetnek, mert a szag segítségével észlelhetővé válik egy színtelen, szagtalan, de robbanásveszélyes gáz szivárgása.
Összefoglalva: a tiolok (más néven mercaptánok) fontos kis molekulák, melyek jellegzetes szaguk, kémiai reakcióképességük (oxidáció, diszulfidképzés, nukleofil viselkedés) és biológiai szerepük révén számos területen — az ipartól a biológiáig — jelentősek.