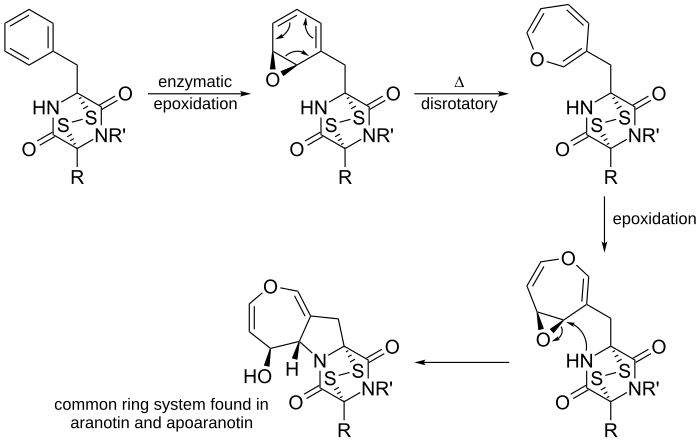
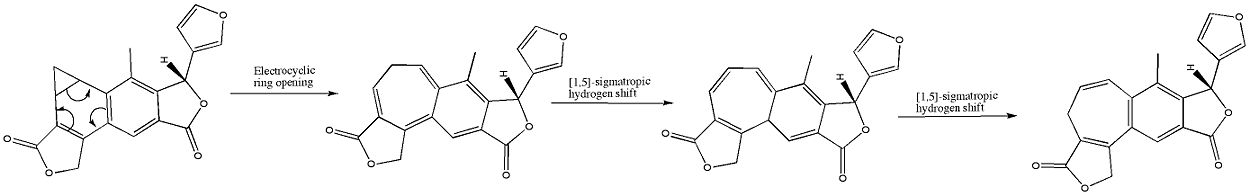
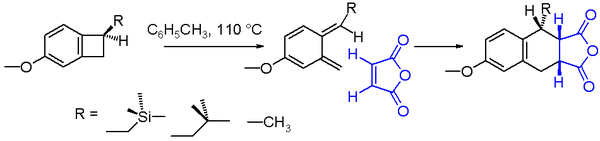
A szerves kémiában az elektrociklikus reakció a periciklikus átrendeződési reakciók egy típusa. A reakció akkor elektrociklusos, ha az eredmény egy pí-kötésből egy szigma-kötéssé, vagy egy szigma-kötésből egy pí-kötéssé alakul. Gyakran ezek a folyamatok gyűrűk képződését vagy gyűrűnyílását jelentik, és koncertezetten, az egész rendszeren végbemenő elektronmozgással zajlanak. Az elektrociklikus reakciók főbb jellemzői:
- az elektrociklikus reakciókat fény ( fotoindukált ) vagy hő (termikus) folyamatok indítják;
- a reakciómódot elsősorban a rendszerben lévő pí-elektronok száma határozza meg (a több pí-kötéssel rendelkező részen);
- egy elektrociklikus reakció lezárhat egy gyűrűt (elektrociklizáció) vagy nyithat egy gyűrűt;
- a sztereospecifitást a Woodward–Hoffmann-szabályok által megjósolt konrotatórikus vagy diszrotatórikus átmeneti állapot határozza meg.
Mechanizmus — határ-orbitálok és Woodward–Hoffmann
Az elektrociklikus reakciók megértéséhez hasznos a határ-orbitál (frontier orbital) szemlélet és a Woodward–Hoffmann-szabályok alkalmazása. Röviden:
- A reakciókban fontos szerepet játszik a legmagasabb elfoglalt molekuláris orbitál (HOMO) és a legalacsonyabb betöltetlen molekuláris orbitál (LUMO) szimmetriája.
- A Woodward–Hoffmann-szabályok szerint a molekuláris orbitálok szimmetriájának megőrzése határozza meg, hogy termikus vagy fotokémiai körülmények között melyik sztereomód (konrotáció vagy diszrotáció) lesz megengedett.
- Általános szabályok (egyszerűsítve): termikus folyamatban a 4n pí-elektronú rendszerek konrotatórikus úton, míg a (4n+2) pí-elektronú rendszerek diszrotatórikus úton reagálnak; fotokémiai gerjesztés esetén ezek a szabályok megfordulnak.
Konrotáció és diszrotáció — mi történik fizikailag?
Konrotációs során a gyűrűnyílás vagy gyűrűképzés végpontjain lévő szubsztituensek ugyanabba az irányba forognak (mindkettő „be” vagy mindkettő „ki”), míg diszrotációs esetén ellentétes irányba forognak. Ez a forgás határozza meg a termék sztereokémiáját (cis/trans, R/S konfigurációk stb.).
Termikus vs. fotoindukált reakciók
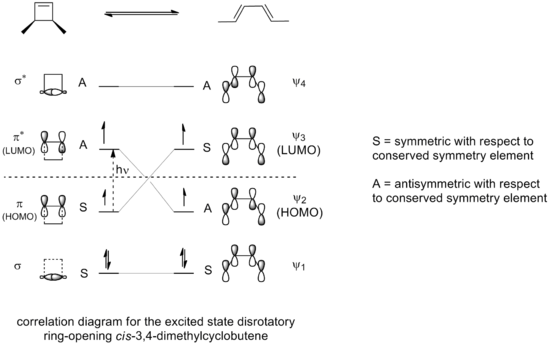
Termikus (hő által indított) reakciókban a rendszer a legalsó energiaállapot környezetében reagál, és a szimmetriamegőrző útvonalak kötelezőek a Woodward–Hoffmann-elv alapján. Fotoindukált reakciókban egy elektron gerjesztődik (HOMO → LUMO), ami megváltoztatja a határ-orbitálok szimmetriáját, és így más mechanizmusok (a termikushoz képest ellentétes sztereomódok) válnak lehetségessé.
Torquoszelektivitás
A torquoszelektivitás egy elektrociklikus reakcióban a szubsztituensek forgási irányára utal. Egy konrotatorikus reakció elvileg két forgásirányt enged meg, amelyek egymás tükörképi termékéhez (enantiomerekhez) vezetnek. Ha a reakció környezetében (szubsztituensek, oldószer, katalizátor, hőmérséklet) aszimmetria van, az egyik forgásirány előnyösebb lehet — ezt nevezzük torquoszelektivitásnak. Ennek eredményeképp a termék enantiomerfeleslegben (ee) képződhet, ami fontos aszimmetrikus szintéziseknél.
Példák és tipikus reakciók
A Nazarov-ciklizáció egy tipikus gyűrűzáró elektrociklikus reakció: divinilketonokat alakít át ciklopentenonokká, és jól használható öt tagú gyűrűk előállítására. A reakciót Ivan Nyikolajevics Nazarov (1906–1957) írta le. A Nazarov-folyamat gyakran savkatalizált, és a reakciófeltételekkel (sav erőssége, oldószer) befolyásolható a szelektivitás és hozam.
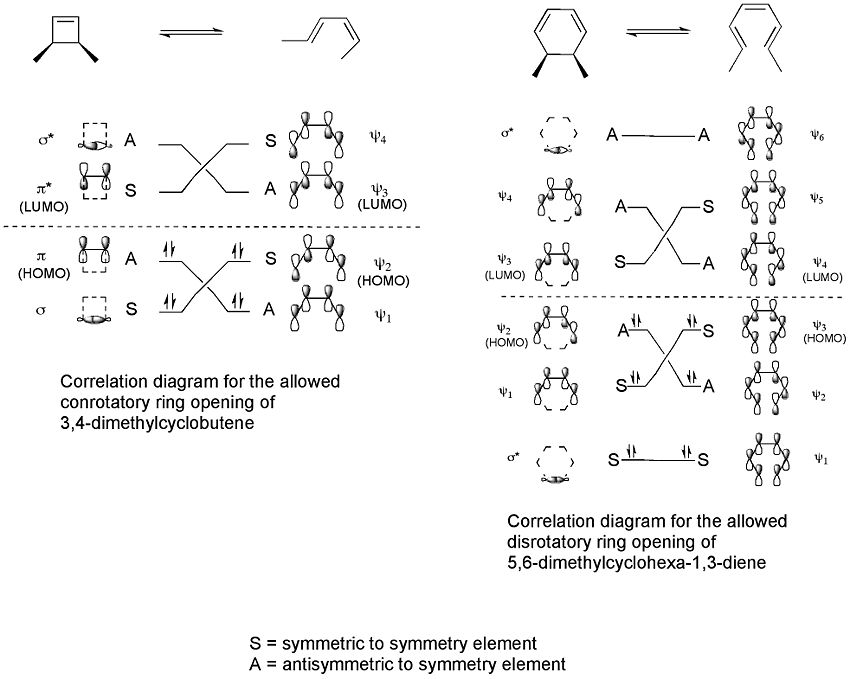
Konkrét példa a 3,4-dimetil-ciklobutén termikus gyűrűnyitása. A cisz-izomerből csak cisz,transz-2,4-hexadién keletkezik, míg a transz-izomer transz,transz-diént ad:
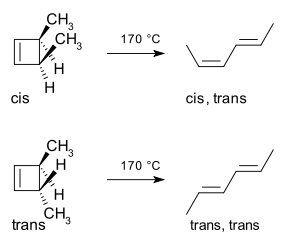
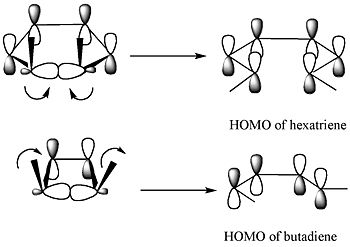
A reakciót a határ-orbitál módszer magyarázza: a szigma-kötés felhasadása úgy történik, hogy a keletkező p-orbitálok szimmetriája egyezzen a termék (butadién) HOMO-jával. Ebben a példában ez csak konrotációs gyűrűnyílással valósulhat meg, különben antikötés jönne létre. Az alábbi ábra bemutatja a mechanizmust a határ-orbitál szemlélettel:
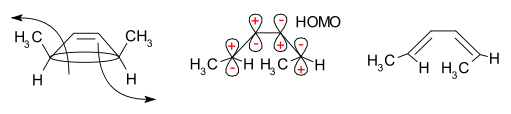
Sztereospecifikusság és sztereokémia
Az elektrociklikus reakciók gyakran sztereospecifikusak: a reaktánsok konfigurációja közvetlenül meghatározhatja a termék sztereokémiáját. A konrotatorikus és diszrotatorikus utak különböző sztereokémiai kimeneteleket adnak, ezért ezek ellenőrzése fontos a célzott szintéziseknél. Torquoszelektív stratégiák és katalizátorok alkalmazásával enantioszelektív elektrociklizációkat is végeznek.
Gyakorlati alkalmazások és kísérleti megfontolások
- A gyakorlatban fontos a megfelelő hőmérséklet, fényforrás (fotokémiai esetben), oldószer és esetleges sav/bázis vagy fémkatalizátor megválasztása.
- Sok elektrociklikus reakció gyorsan zajlik le, ezért a reakciókinetika és a klasszikus termodinamikai vs. kinetikai kontroll megértése szükséges a kívánt termékek eléréséhez.
- Szintetikus kémiai alkalmazásokban az elektrociklizáció hatékony módszer komplex szénvázak és természetes termékek előállítására.
Elmélet és kísérleti igazolás
A kémikusokat azért érdeklik az elektrociklikus reakciók, mert a molekulák geometriája és a kapott termékek számos, az elméleti kémikusok által készített előrejelzést megerősítenek. Ezek a vizsgálatok alátámasztják a molekuláris orbitál szimmetria megőrzésének elvét, és lehetővé teszik részletes számításokkal (pl. DFT, átmeneti állapot-számítások) a mechanizmusok vizsgálatát.
Összefoglalás
Az elektrociklikus reakciók fontos, jól szabályozható átrendeződések a szerves kémiában, amelyek megértése kombinálja a kvantumkémiai elveket (határ-orbitálok, Woodward–Hoffmann-szabályok) és a gyakorlati kísérleteket. A sztereokémiai kimenetel irányítható konrotáció/diszrotáció és torquoszelektív stratégiák alkalmazásával, ezért az elektrociklizációk értékes eszközei a modern szintetikus kémiának.