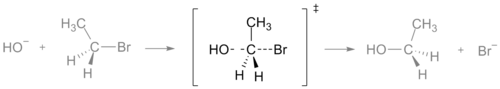Egy kémiai reakcióban az átmeneti állapot az a pont, ahol a rendszer potenciális energiája a reakció mentén a legmagasabb. Ennek az energiának a reagensek energia-szintjéhez mért különbségét nevezzük aktiválási energiának. Ha a reagensek ütközésekor a rendelkezésre álló energia eléri vagy meghaladja ezt az aktiválási energiát, akkor a részecskék át tudnak lépni az átmeneti állapoton, és megtörténhet a kötések átrendeződése, új molekulák keletkeznek.
Amikor két vagy több molekula keveredik és egymásnak ütközik, a sikeres reakcióhoz nemcsak az ütközés, hanem elegendő energia és megfelelő térbeli orientáció is szükséges. Az átmeneti állapotban részben megszakadnak a régi kötések, miközben részben új kötések alakulnak ki; ez az állapot tehát egyszerre mutat a kiindulási anyagokra és a termékekre jellemző vonásokat. A reakcióenergetikai görbén az átmeneti állapotot gyakran a kettős tőr ‡ szimbólummal jelölik.
Energiaprofil és aktiválási energia
Egy tipikus energiagörbe (reakciókoordináta-diagram) a függőleges tengelyen az energiát, a vízszintes tengelyen pedig a reakció előrehaladását (reakciókoordinátát) mutatja. Az átmeneti állapot a reagensek és a termékek közötti energiamaximum; az aktiválási energia (Ea) ennek a maximumnak és a reagensek energia-szintjének a különbsége. Az aktiválási energia fontos szerepet játszik a reakciósebesség meghatározásában, amit az Arrhenius-egyenlet ír le: k = A e^(−Ea/RT), ahol k a sebességi együttható, A az előfaktor, R az univerzális gázállandó és T a hőmérséklet.
Átmeneti állapot mint nyeregpont
Az átmeneti állapot a többdimenziós potenciálenergia-felületen (PES) egy úgynevezett nyeregpont (saddle point): stabil irányokban lokális maximum, egy irányban pedig minimum; matematikailag ezt úgy szokás jellemezni, hogy a Hess-mátrixnak pontosan egy negatív sajátértéke van. Ez a tulajdonság különbözteti meg a valódi átmeneti állapotot a hosszabb élettartamú köztes állapottól, amelyek az energia minimumaihoz kapcsolódnak.
Miért nehéz tanulmányozni?
Az átmeneti állapotok élettartama rendkívül rövid, tipikusan femtoszekundumos (10^−15 s) vagy rövidebb, ezért hagyományos kísérleti módszerekkel nehezen közvetlenül megfigyelhetők. Ezért különösen fontos a következő megközelítések kombinálása:
- Ultragyors kísérleti technikák: femtószekundumos lézerspektroszkópia (femtokémia), pump–probe mérések, amelyek lehetővé teszik az átmeneti állapotokhoz közeli folyamatok időfelbontású követését.
- Kinetikai mérések és izotóphatás: reakciósebesség-vizsgálatok, kinetikai izotóphatás (KIE) segítségével következtethetünk a kötésszakadás/keletkezés menetére és a reakció állapotára.
- Számítógépes módszerek: kvantumkémiai számítások (ab initio, DFT), átmeneti állapot keresése és az intrinsic reaction coordinate (IRC) követése, amelyek modellezik a potenciálenergia-felületet és megadják a nyeregpont szerkezetét és energiáját.
- Átmeneti állapot-analógok: stabil molekulák tervezése, amelyek szerkezetileg hasonlítanak az átmeneti állapothoz; különösen fontos ez gyógyszerkutatásban és enzimkatalízis vizsgálatánál.
Reakciómechanizmusok és katalízis
Az átmeneti állapotok vizsgálata kulcsfontosságú a reakciómechanizmusok megértéséhez és a kémiai kinetika területén. A katalizátorok működésének lényege gyakran az, hogy csökkentik az aktiválási energiát azáltal, hogy stabilizálják az átmeneti állapotot (vagy alternatív, alacsonyabb energiaigényű átmeneti állapotot hoznak létre). Az enzimek például gyakran kifejezetten az átmeneti állapot megkötésére specializálódtak, ami jelentősen megnöveli a reakció sebességét.
Szerkezet és elméleti megfontolások
A Hammond-elv (Hammond–Leffler elv) röviden azt mondja ki, hogy egy átmeneti állapot szerkezete hasonló lesz ahhoz a reakcióállapothoz (reagensekhez vagy termékekhez), amelyhez energiában közelebb van. Ennek gyakorlati jelentősége például a szubsztruens-effektek és az endoterm/egzoterm reakciók értelmezésében rejlik. Az átmeneti állapotok lehetnek szinkronok (a kötésszakadás és kötésképződés egy időben történik) vagy aszinkronok (a folyamatok részben elcsúsznak egymáshoz képest), és ez hatással van a reakció stereokémiájára és szelektivitására.
Különbség átmeneti állapot és köztes állapot között
Nagy fontos megkülönböztetni az átmeneti állapotokat a köztes állapotokkal. A köztes állapotok az energia minimumaihoz kapcsolódnak a potenciálenergia-felületen, ezért viszonylag hosszabb ideig (jóval a femtoszekundumnál hosszabb ideig) élhetnek, izolálhatók vagy közvetve megfigyelhetők. Ezzel szemben az átmeneti állapotok rövid élettartamú, magas energiaállapotok, és nem stabilizálhatók hosszabb ideig.
Összefoglalás
- Az átmeneti állapot a reakcióenergia-görbe maximuma; ezen az energián múlik a aktiválási energia.
- Az átmeneti állapot általában nagyon rövid élettartamú és nehezen megfigyelhető, ezért kombinált kísérleti és számítógépes módszerek szükségesek a tanulmányozásához.
- Katalízis során a katalizátorok gyakran azáltal növelik a sebességet, hogy csökkentik az aktiválási energiát, azaz stabilizálják az átmeneti állapotot vagy alternatív átmeneti állapotot biztosítanak.
- Az átmeneti állapotok szerepének megértése alapvető a reakciómechanizmusok és a kémiai kinetika tanulmányozásában.