A szerves kémiában a torquoszelektivitás olyan elektrociklikus reakciókat ír le, amelyekben a reakció során a kiindulási molekula különböző forgásirányai különböző mértékben járulnak hozzá a termékek kialakulásához, azaz az egyik izomer jelentősen nagyobb mennyiségben keletkezik, mint a másik. Hivatalosan ez a jelenség a "a szubsztituensek befelé vagy kifelé történő forgásának preferálása a konrotációs vagy diszrotációs elektrociklikus reakciókban" — más szóval: a forgásirányok nem egyenrangúak, és így aszimmetrikus termékeloszlás jön létre. Az elnevezés onnan ered, hogy az elektrociklizáció során a szubsztituensek a gyűrű mentén "látszólag forognak", és ez a forgásirány döntő a kialakuló szerkezet szempontjából. A koncepciót eredetileg Kendall N. Houk és munkatársai dolgozták ki elméleti és számításos vizsgálatok alapján.
Mechanizmus, konrotáció vs. diszrotáció és a torquoszelektivitás kapcsolata
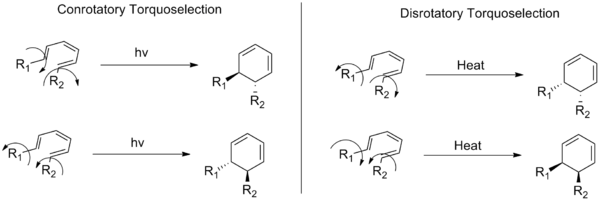
Az elektrociklikus reakciókat a Woodward-Hoffmann-szabályok irányítják, amelyek meghatározzák, hogy egy adott rendszer termikus vagy fotokémiai körülmények között konrotorikus vagy diszrotorikus módon záródik vagy nyílik-e. A torquoszelektivitás ezeken túlmutat: még ha a konrotációs vagy diszrotációs mód egyértelműen adott is, a szubsztituensek azon belüli forgásiránya (például mindkét csoport óramutató-, vagy ellentétes irányba fordul-e) meghatározza, melyik diasztereo- vagy enantiomer alakul ki.
Például egy tipikus elektrociklikus gyűrűzárásnál a konrotációs vagy diszrotációs mód kiválasztása önmagában még két enantiomert eredményezhet. A torquoszelektivitás ekkor a lehetséges enantiomerek közötti megkülönböztetés: aszimmetrikus indukcióval az egyik forgásirány preferálhatóvá válik, és így egy enantiomer dominál.
Kik a meghatározó tényezők? (mi okozza a szelektivitást)
A torquoszelektivitást több, gyakran együttes hatásban működő tényező befolyásolja:
- Sztérikus kölcsönhatások: nagyobb helyigényű csoportok elkerülik az egymás közeli orientációját, így az egyik forgásirány előnyösebb lehet.
- Elektronikus hatások: szubsztituensek elektrondonor vagy elektronelvonó jellege módosíthatja a tranzíciós állapot energiaszintjét, és ezáltal befolyásolja a preferált forgásirányt.
- Másodlagos orbitálkölcsönhatások és hyperkonjugáció: bizonyos orientációk kedvezőbb orbitalis átfedést biztosítanak, ami stabilizálja a tranzíciós állapotot.
- Elektrosztatikus kölcsönhatások: töltés- vagy dipólus-kölcsönhatások aszimmetriát vezethetnek be a tranzíciós állapotok között.
Termikus vs. fotokémiai körülmények, torquoselectivity vs. torquospecificity
Fontos megkülönböztetni a torquoszelektivitást és a torquospecifikusságot: a torquoszelektivitás azt jelenti, hogy az egyik forgásirány erősebben preferált, de a másik irányból is keletkezhet termék; a torquospecificitás viszont arra utal, hogy csak egy forgásirány valósul meg (a másik teljesen tiltott). A kísérleti körülmények — hőmérséklet, fény, oldószer, katalizátor — gyakran befolyásolják, hogy mennyire „tiszta” a preferencia. Gyakran számításokkal (pl. DFT) vizsgálják a tranzíciós állapotok energiáit, hogy megértsék a szelektivitás eredetét.
Gyakori példák
Számos tipikus elektrociklikus reakcióban előfordul torquoszelektivitás:
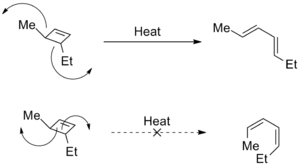
- Ciklobuténgyűrűk termikus gyűrűnyílása: 3-szubsztituált ciklobutének termikus gyűrűnyílásakor a szubsztituensek forgásirányának preferenciája határozza meg az E/Z-izomer arányát a keletkező 1,3-butadiénnél.
- Hexatrien → ciklohexadién záródás: a konrotorikus vagy diszrotorikus mozgás mellett a végső stereokémiát a komponensek forgásiránya finomítja.
- Nazarov-ciklizáció (4π elektrociklizáció): a divinil-ketonok ciklizációja során a különböző forgásirányok eltérő ciklopentenon-izomereket eredményeznek. Példa: királis allenilvinil-ketonok torquoszelektív Nazarov-ciklizációja során az axiális kiralitás átadható a keletkező tetraéderes központokra, így chirális ciklopentenonok jönnek létre.
Elérés módjai a szintetikus kémiában
A torquoszelektivitás gyakorlati alkalmazása a királis termékek szintézisében különböző módszerekkel valósítható meg:
- Királis katalizátorok: például királis Lewis-sav katalizátorok képesek aszimmetrikus indukciót biztosítani, és így egy forgásirányt preferálni.
- Szomszédos sztereocentrumok befolyása: ha a kiindulási molekulában már van kiralitás, az indukálhat torquoszelektivitást (ebben az esetben a torquoszelektivitás a diasztereoszelektivitás egy esete).
- Királis auxiliáriumok vagy szubsztrát-konfigurációk: a szubsztrátban lévő kiralitás átadása (pl. axiális → tetraéderes chiralitástranszfer) hatékony módja lehet egy enantiomer előnyben részesítésének.
Mérések és elemzés
A torquoszelektivitás mértéke kísérleti úton a termékarányok és az enantiomer-tisztaság (ee) meghatározásával mérhető. A kísérleti eredményeket gyakran számításos vizsgálatokkal (pl. tranzíciós állapot számítások, potenciálenergia felületek) egészítik ki, hogy feltárják a szelektivitás eredetét és tervezzenek jobb katalizátorokat vagy szubsztrátokat.
Jelentőség és alkalmazások
A torquoszelektivitás fontos eszköz a szintetikus kémikus számára, mert lehetővé teszi aszimmetrikus gyűrűzárások és gyűrűnyitások kontrollálását, ami különösen értékes komplex, funkciógazdag molekulák — például természetes vegyületek és bioaktív molekulák — szelektív előállításához. A mechanisztikus megértés és a királis katalizátorok fejlődése folyamatosan bővíti alkalmazhatóságát.
Összefoglalva: a torquoszelektivitás az elektrociklikus reakciók finom sztereokémiai irányításának egyik kulcseleme. A preferált forgásirányok kialakulását sztérikus, elektronikus és másodlagos orbitalis tényezők határozzák meg, és a jelenség tudatos kihasználásával sztereoszelektív és enantioszelektív szintézisek valósíthatók meg.
A torquoszelektivitás más mechanizmusokra is vonatkozhat, beleértve a királis Lewis-sav katalizátorokat, a szomszédos sztereocentrumok általi indukciót (ebben az esetben a torquoszelektivitás a diasztereoszelektivitás esete) és az axiális-tetraéderes kiralitásátvitelt. Az axiális-tetraéderes kiralitásátvitelre az alábbiakban egy királis allenilvinil-keton torquoszelektív Nazarov-ciklizációs reakciójára mutatunk példát.