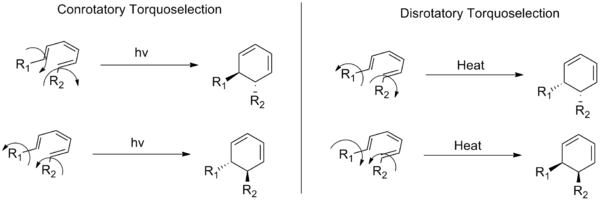
Ezek a kifejezések az elektrociklikus reakciók (a szerves kémiai reakciók egyik típusa) két feltűnő stereokémiájú lezárási/nyitási módját írják le. Konrotációs módban a konjugált kettős kötésrendszer végein elhelyezkedő szubsztituensek a gyűrűnyitás vagy gyűrűzárás során azonos irányba (mindkettő az óramutató járásával megegyezően vagy mindkettő ellentétes irányban) forognak. Ezzel szemben a disrotatorikus módban a két végpont ellenkező irányba mozog: egyikük jobbra, a másik balra forog.
A különbség megértéséhez hasznos a rendszer legfelső elfoglalt molekuláris orbitáljának (HOMO) fázisszerkezete. A reakció során a terminális p-orbitáloknak olyan fázisviszonyban kell kapcsolódniuk, hogy létrejöjjön a sigma-kötés; ez a fázisviszony határozza meg, hogy konrotáció vagy disrotáció lesz-e „szimmetriailag megengedett” (azaz alacsonyabb energiájú, könnyebben lejátszódó) útvonal.
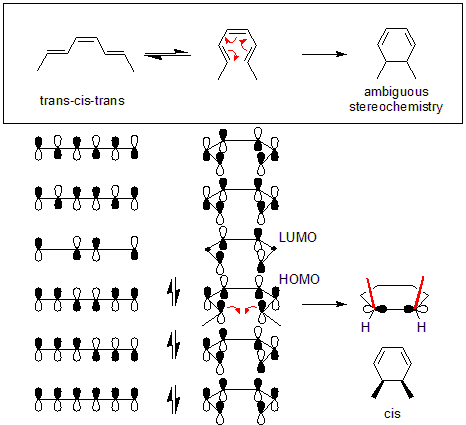
Példa: oktatrien → ciklohexadién
Egy konkrét példa a transz–cisz–transz-2,4,6-oktatrien átalakulása cisz-dimetil-ciklohexadiénné (az ábra tetején). Ennek a reakciónak az orbitális mechanikája disrotációt követel meg: az oktatrien HOMO-jának szimmetriája miatt a végponti π-orbitálok ellentétes irányú elfordulása szükséges ahhoz, hogy megfelelő fázisviszonyú σ-kötést alakuljon ki a termékben.
Általános szabályok (összefoglalás)
- Termikus (hő által vezetett) elektrociklikus reakciók:
- 4n + 2 π-elektronos rendszerek (például 6 π) — disrotatorikus lezárás.
- 4n π-elektronos rendszerek (például 4 π) — konrotatorikus lezárás.
- Fotokémiai (fény-aktivált) elektrociklikus reakciók:
- A fenti szabályok megfordulnak: 4n + 2 rendszerek fotokémiai úton konrotatorikusak, míg 4n rendszerek disrotatorikusak.
Ez a viselkedés a legfelső elfoglalt és a legalsó betöltetlen orbitalis fázisviszonyainak a gerjesztés hatására bekövetkező megváltozásából adódik: fotokémiai gerjesztés során elektron kerül az LUMO-ba, így az izomer orbitálszimmetria uralja a reakciót, emiatt a preferált forgásirány megváltozik.
Woodward–Hoffmann-szabályok és az „engedettség” fogalma
A Woodward-Hoffmann-szabályok általános keretet adnak a periciklikus reakciók (köztük az elektrociklikusok) sztereokémiai kimenetének megjóslására az orbitálszimmetria megőrzése alapján. A szabályok szerint egy periciklikus folyamat akkor „szimmetriailag engedett” (allowed), ha van olyan reakcióút, amely során az elektronikus állapotok folytonosan párosíthatók (korrelálhatók) az induló és termék állapotok között anélkül, hogy orbitál-szimmetriatilalomba ütköznénk. Az engedett utak általában alacsonyabb aktivációs energiával járnak, míg a tiltott (forbidden) utaknál nagyobb energiaköltség vagy fotokémiai aktiválás szükséges.
Gyakorlati megjegyzések
- A konrotációs/disrotációs szabályok fontosak a szintetikus kémiai tervezésnél: megmondják, milyen relatív konfigurációjú termék várható egy adott feltétel (hő vs. fény) mellett.
- Kisebb gyűrűk vagy merev szerkezetek esetén a geometriai korlátozások (sterikus feszültség) befolyásolhatják, hogy melyik mód játszódik le, és néha ritkábban előforduló antarafaciális átmenetek is fontolóra jöhetnek, de ezek nagyobb sebészi feszültséget igényelnek és ritkábbak.
- A reakció mechanizmusának pontos megértéséhez gyakran alkalmaznak molekuláris orbitalis számításokat és spektroszkópiai vizsgálatokat, amelyek megerősítik a HOMO/LUMO fázisszerkezetének szerepét.
Összefoglalva: a konrotáció és disrotáció az elektrociklikus reakciók két lehetséges stereokémiai lefolyása, amelyeket az elektronok számának (4n vagy 4n+2) és az aktiválás módjának (termikus vagy fotokémiai) kombinációja határoz meg. A Woodward-Hoffmann-szabályok segítségével ezek a kimenetek kiszámíthatók és megérthetők az orbitálszimmetria elve alapján.