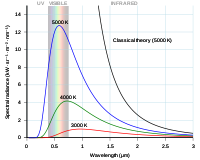
A Planck-állandó (h) a kvantumfizika egyik alapvető állandója, amely összekapcsolja a foton által szállított energia mennyiségét az elektromágneses hullám frekvenciájával. A mennyiséget Max Planck vezette be a fekete test sugárzásának leírására, és ma is a kvantummechanika legtöbb alapvető összefüggésében megjelenik; ezért fontos mennyiség a kvantumfizikában.
Definíció és alapösszefüggések
A legegyszerűbb formájában a Planck-állandó megadja egy foton energiáját a frekvencia függvényében: E = h f, ahol E az energia és f a frekvencia. Az impulzus és hullámhossz viszonyában, illetve szögfrekvencia használatakor gyakran a csökkentett Planck-állandót (ħ = h / 2π) alkalmazzuk, amellyel az energia szögfrekvencia szerint: E = ħ ω.
Mértékegység, dimenzió és pontos érték
A Planck-állandó a fizikai cselekvés dimenziói szerint az energia és az idő szorzata, illetve a lendület és a távolság szorzata. SI-egységekben a Planck-állandó joule-másodpercben (J⋅s) fejeződik ki (azonos dimenzióban kimutatható mint N⋅m⋅s vagy kg⋅m2⋅s−1).
SI-egységben a Planck-állandó pontosan 6,62607015×10−34 J-s (ez a pontos érték az SI rendszer 2019-es átdolgozásának következménye: a Planck-állandó értékét rögzítették, így az új definíciók alapján a kilogramm meghatározása is ehhez kapcsolódik). A Planck-állandó pontos rögzítése lehetővé teszi más alapegységek pontosabb definícióját és mérését.
Kvantumfizikai szerep és jelentés
A Planck-állandó a kvantummechanikában az akció (action) kvantáltságát fejezi ki: az energia átvitele nem folytonos, hanem diszkrét egységekben (kvantumokban) történik, ahol a h adja meg az alapegységet. Gyakori alkalmazások és következmények:
- Fotonegyenlet: E = h f — egy foton energiája arányos a frekvenciájával.
- Csökkentett Planck-állandó (ħ): a Heisenberg-féle határozatlansági relációk és a kvantummechanikai operátorok kommuntációs relációi gyakran ħ-vel írhatók: például a pozíció és impulzus kommutátora [x, p] = i ħ, és a határozatlansági reláció egyik formája Δx Δp ≥ ħ/2.
- Energiaidő határozatlanság: ΔE Δt ≳ ħ/2, ami a kvantumátmenetek és állapotok élettartamának korlátait írja le.
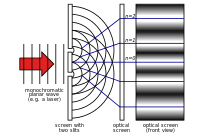
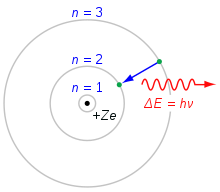
- Spektrumok és energiaszintek: az atomi és molekuláris energiaszintek különbségei és az azokból származó fotonok frekvenciái Planck-összefüggéssel számíthatók.
Kapcsolódó mennyiségek és alkalmazások
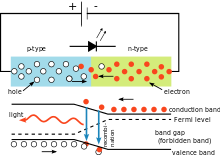
A Planck-állandó szerepel a Planck-egységrendszer képleteiben: például a Planck-hossz és a Planck-idő kiszámításában, amelyek a gravitáció és kvantumelmélet összefüggéseinél használt alapvető skálák. Továbbá a Planck-állandó fontos szerepet játszik a kvantummező-elméletben, a statisztikus mechanikában és a kvantuminformatikában (például qubit energiaszintek és frekvenciák meghatározásában).
Rövid történeti megjegyzés
Max Planck 1900-ban vezette be az energiakvantum fogalmát a fekete test sugárzásának matematikai leírására. Ez volt a kvantumelmélet egyik kiindulópontja, amely később a foton koncepciójának és a modern kvantummechanika kialakulásának alapját képezte.
Összefoglalva: a Planck-állandó alapvető szerepet játszik a kvantumok világában — mérőszámként jelenik meg az energia, frekvencia, impulzus és hullámhossz kapcsolatában, és a természettörvények kvantált jellegének kifejezője.








![Az illusztráció Newton eredeti, a Royal Society-nek írt leveléből származik (1671. január 1. [Julián-naptár]). Az S a napfényt jelképezi. A fény a BC és DE síkok között színes. Ezek a színek újra egyesülnek, és a GH síkon a napfényt alkotják.](https://www.alegsaonline.com/image/NewtonDualPrismExperiment.jpg)







![{\displaystyle h={\frac {\mu _{0}\pi }{12c^{3}}}{[{q_{0}}{[0.9163a_{0}]}^{2}]^{2}}{f_{1r}}^{5}\cdot {s}=6.63\times 10^{-34}J\cdot s}](https://www.alegsaonline.com/image/4c47db8d0ec87cc985fc3b80db4214489e87a164.svg)





