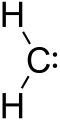A karbén olyan molekula, amelynek egy szénatomja csak két kötéssel kapcsolódik a környezetéhez, és két másik elektronja nincs kötésben (ezeket néha nemkötő elektronpárnak vagy egyszerűen párosítatlan elektronoknak nevezik). Az ilyen szénatom formálisan csak hat elektronnal rendelkezik a külső héján, ezért a karbének általában nagy reaktivitást mutatnak. Az általános képletet egyszerűen R2C: vagy R-(C:)-R' alakban írhatjuk fel.
Elektronikus szerkezet: singlet és triplet
A karbén két alapvető elektronikus állapotban fordulhat elő: singlet és triplet.
- Singlet karbén: A két nemkötő elektron párosítva van ugyanabban az orbitálisban, ezért nincs nettó spininverzió. Egy klasszikus leírás szerint a szénatom gyakran sp2 hibridizáltságú, egyik hibridpályán van a páros elektronpár, míg egy üres p-orbitál áll rendelkezésre. A singlet karbének elektromos és szterikus hatások révén stabilizálhatók.
- Triplet karbén: Itt a két elektron különböző orbitálokon helyezkedik el és párhuzamos spin állapotban van, ezért a rendszer diradikális jellegű. A triplet állapot gyakran magasabb energiaszintű lehet, de bizonyos karbének esetén a triplet a stabilabb alapállapot (például az egyszerű metilén, :CH2, gáznemű formában triplet alapállapotú).
Az, hogy egy adott karbén singlet vagy triplet állapotú-e, nagyban függ a szubsztituensektől és azok elektronikus hatásaitól: elektronadó csoportok, π-donorok vagy -akkceptorok, valamint a szterikus védelem mind befolyásolják az állapotok relatív energiáját.
Típusok és stabilizáció
A karbéneket több szempontból csoportosítjuk:
- Szubsztituens szerint: egyszerű szénhidrogén karbének (pl. metilén), halogénezett karbének (pl. dichloro-carbene), heteroatomokkal stabilizált karbének (pl. nitrogénnel delokalizált változatok).
- Koordinált fém-karbének: a karbén lehet ligandum fémkomplexekben. Itt megkülönböztetjük a Fischer és Schrock típusú karbénokat: a Fischer-karbénok általában alacsony oxidációs állapotú fémhez kötődnek és elektrofílikusabbak, a Schrock-karbénok pedig korai, magasabb oxidációs állapotú fémekhez tartoznak és gyakran nukleofil jellegűek.
- Tartós (persistent) karbének: bizonyos szerkezetek — például az N-heterociklusos karbének (NHC) — annyira stabilak, hogy izolálható, szilárd anyagként is léteznek. Ezek a karbének széles körben használatos ligandumok a modern katalízisben.
A stabilizáció fő mechanizmusai: elektronikus delokalizáció (például heteroatomokkal való rezonancia), elektronelnyelő vagy -adó csoportok, valamint erős szterikus védettség, amely megakadályozza a dimerizációt vagy más gyors bimolekuláris reakciókat.
Főbb reakciók és alkalmazások
A karbének sokféle reakcióban vesznek részt; elektrofílikus vagy nukleofil karakterük a típusuktól függ. A legfontosabb reakciók közé tartoznak:
- Ciklopropanáció: az alkénekkel való addíció során karbének könnyen létrehoznak ciklopropán gyűrűket — ezt a reakciót gyakran használják szintetikus kémiában.
- Insertiók: karbének beépülhetnek C–H, O–H vagy N–H kötésekbe, új C–X kötéseket létrehozva.
- Ylide-képzés és átrendeződések: karbének reakcióba léphetnek például foszfinokkal vagy más nukleofilekkel, ylide-ket alkotva; bizonyos karbének Wolff- és más átrendeződéseket is mutathatnak.
- Fém-karbén mechanizmusok: átmenetifém-karbének kulcsszereplők az olyan katalitikus folyamatokban, mint az olefin metatézis — itt a karbén fém-alkilidén komplex formájában működik. A Robert Grubbs nevéhez fűződő Grubbs-katalizátorok is ilyen fém-karbén komplexek.
Az eredeti szövegben szereplő megfogalmazás: Keletropikus reakciókban is előfordulnak. Ezt pontosítva: a karbének sokféle reakciót végeznek, köztük addíciókat, insertiókat, ciklopropanációt és különféle mechanizmusokat (beleértve szabadgyökös és periciklikus utak szerepét is) — tehát a karbének reakciókészsége széles körű, és számos szintetikus és katalitikus alkalmazásban kihasználható.
Kimutatás és vizsgálat
A karbének gyakran rövid életűek, ezért kémiai csapdázással, spektroszkópiával (például ESR a triplet karbének esetén) és gyors kinetikai módszerekkel tanulmányozzák őket. A stabil, izolálható karbének lehetővé teszik a roncsolásmentes szerkezeti vizsgálatokat és széles körű alkalmazást a katalízisben.
Példák és történeti megjegyzések
- Egyszerű példa: metilén (:CH2) — gáznemű, alapvetően triplet alapállapotú.
- Dichlorocarbene (:CCl2) — egy jól ismert karbén, amely gyakran singlet karakterű, és széles körben alkalmazzák szintetikus átalakításokhoz.
- Tartós karbének: az Arduengo-féle N-heterociklusos karbének az 1990-es években tették lehetővé a karbének izolálását és széles körű katalitikus felhasználását.
- A fém-karbének közül a Grubbs-katalizátorok (ruthenium-karbén komplexek) forradalmasították az olefin metatézist, és ez a kutatás Robert Grubbs Nobel-díjához is kapcsolódik.
Összefoglalva: a karbén egy különleges, általában nagyon reaktív szénalapú részecske, amelynek elektronikus szerkezete (singlet vagy triplet) és stabilitása nagymértékben függ a környező csoportoktól. Bár sok karbén rövid életű, néhány stabil változat ma már nélkülözhetetlen eszköz a modern szintetikus és katalitikus kémiában.