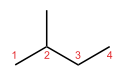A szerkezeti izoméria (az IUPAC ezt alkotmányos izomériának nevezi) az izoméria egyik fajtája. Ebben az izomerizmusban két kémiai anyagnak ugyanaz a molekulaformulája, de a molekulák atomjai más-más sorrendben kapcsolódnak egymáshoz — vagyis eltér a kötésrend és a kapcsolódási séma. A szerkezeti (alkotmányos) izoméria lényege tehát a különböző kapcsolódási sorrend; ellentéte a sztereoizoméria, ahol a kapcsolódási sorrend azonos, de a térbeli elrendeződés különbözik. Számos kifejezés és altípus létezik a szerkezeti izomériára, ezeket az alábbiakban részletezzük.
Típusok és példák
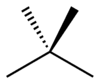
- Vázizomerek (lánc- vagy csontváz-izomerek): ugyanaz a képlet, de a szénváz szerkezete különbözik. Példa: n-bután (bután, CH3–CH2–CH2–CH3) és izobután (2-metilpropán, (CH3)2CH–CH3) — mindkettő C4H10, de eltérő a lánc elágazódása.
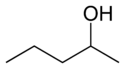
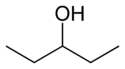
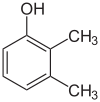
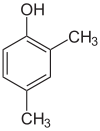
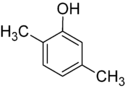
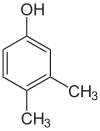
- Helyzeti (pozicionális, regio-) izomerek: ugyanaz a funkciós csoport és főváz, de a funkciós csoport helye különbözik a vázon. Példák: 1-butanol (CH3–CH2–CH2–CH2–OH) és 2-butanol (CH3–CH2–CH(OH)–CH3) — mindkettő C4H10O, de más a hidroxilcsoport pozíciója; 1-klórbután vs 2-klórbután is hasonló eset.
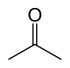
- Funkcionális izomerek: az izomerek eltérő funkciós csoportot tartalmaznak, noha a képlete azonos. Klasszikus példa: etanol (CH3CH2OH) és dimetil-éter (CH3–O–CH3) — mindkettő C2H6O, de az egyik alkohol, a másik éter. Másik példa: propanal (alkanal) és propanon (acetone, keton) — mindkettő C3H6O, de aldehid és keton típusúak.
- Tautomerek (a funkcionális izomerek különleges altípusa): protonátmenettel és kettős/kötésátalakulással járó egyensúlyi átalakulások, tipikus a keto–enol tautomerizmus. Példa: a 2,4-pentándion (acetil-aceton) keto és enol formái, amelyek dinamikus egyensúlyban vannak.
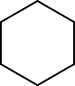
- Gyűrű–lánc izomerek: ugyanaz a képlet lehet gyűrűs vagy láncos formában. Példa: ciklohexán (C6H12) és hex-1-én (C6H12) — eltérő szerkezet, ugyanaz a molekulasúly és képlet.
- Metamerizmus (történetileg használt kategória): olyan esetek, amikor a funkciós csoport körüli két alkilrész eltér. Példa éterekre: etil-metil-éter és dietil-éter lehetnek ugyanazon képlettel (C4H10O) különböző alkilcsoportokkal.
Hogyan különböztetjük meg az alkotmányos izomereket?
- Fizikai tulajdonságok: olvadáspont, forráspont, sűrűség, oldhatóság gyakran eltér az izomerek között (például egyenes láncú alkoholok általában magasabb forráspontúak, mint elágazó társaik).
- Spektroszkópia: NMR (1H, 13C) a leginformatívabb, mert megmutatja az atomok közötti kapcsolódási környezetet; IR segít felismerni funkciós csoportokat; tömegspektrometria jellegzetes fragmentációs mintázatot ad.
- Kémiai reakciók: funkcionális izomerek eltérő reaktivitást mutatnak (pl. alkohol és éter másképp reagál savakkal vagy oxidálószerekkel), így egyszerű kémiai próbák is elkülöníthetik őket.
Miért fontos a szerkezeti izoméria?
A szerkezeti izoméria megmutatja, hogy az azonos összegképlettel rendelkező molekulák teljesen eltérő tulajdonságokkal és felhasználási területekkel rendelkezhetnek. Ez döntő fontosságú a gyógyszerkutatásban (egy izomer hatóanyagként működhet, másik nem), az anyagtervezésben és az ipari kémiai folyamatokban. A szerkezet–tulajdonság összefüggések megértése segít a kívánt fizikai és kémiai jellemzők céltudatos kialakításában.
Összefoglalva: a szerkezeti (alkotmányos) izoméria azonos molekulasúlyú, de különböző kötési sorrendű molekulákat jelöl; alapvető altípusai a váz-, helyzeti és funkcionális izomerek (a tautomerek ezek közül speciális esetet alkotnak). Megkülönböztetésükre spektrális és kémiai módszerek, valamint a fizikai tulajdonságok vizsgálata szolgál.