Elektronkonfiguráció alatt értjük az elektronok elrendeződését az atomban. Az elektronkonfiguráció megmutatja, hogy az elektronok melyik pályákon (orbitálokon) helyezkednek el, és hány elektron van az egyes pályákon. Az elemek periódusos rendszerének felépítése, kémiai tulajdonságaik és kötésképző képességük jelentős része az elektronkonfiguráción alapul.
s, p, d és f orbitálok — alak és kapacitás
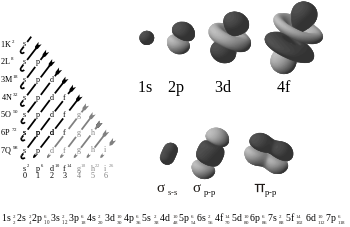
Az atomorbitálok főbb típusai az s, p, d és f orbitálok. Jellemzők:
- s-orbitál: közel gömb alakú, minden energiaszintben egy s-alapú alhéj van; kapacitása: 2 elektron.
- p-orbitál: súlyzó vagy hengerre emlékeztető alakú, egy energiaszinten három p-alapú alhéj van (px, py, pz); kapacitása: 6 elektron.
- d-orbitál: jellemzően lóhere-szerű elrendeződésű, egy energiaszinten öt d-alapú alhéj van; kapacitása: 10 elektron.
- f-orbitál: összetett matematikai formájú, egy energiaszinten hét f-alapú alhéj van; kapacitása: 14 elektron.
Az elektronok feltöltésének alapelvei
Az elektronok az atompályákat egy meghatározott sorrendben töltik fel. A legfontosabb elvek és szabályok:
- Aufbau-elv (feltöltés elve): az elektronok először az alacsonyabb energiájú pályákat töltik fel. Gyakori feltöltési sorrend: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d … (ez az ún. diagonális szabály alapján könnyebben megjegyezhető).
- Pauli-elv (Pauli-exklúzió): egyetlen atomon belül két elektron sem rendelkezhet teljesen azonos négy kvantumszámmal, ezért egy orbitálban maximum két elektron lehet, ellentétes spinűek.
- Hund-szabály: azonos energiájú (degenerált) alhéjakban (például a három p-orbitál) az elektronok először párosítatlanul, párhuzamos spinnel helyezkednek el, hogy a teljes spin minél nagyobb legyen.
Kvantumszámok röviden
Az elektronok elhelyezkedését négy kvantumszámmal jellemezzük: a főkvantumszám (n – héj/energia), az impulzusmomentum-kvantumszám (l – alhéj: s=0, p=1, d=2, f=3), a mágneses kvantumszám (m vagy m_l – az alhéj egyes orbitáljai), és a spin (m_s – +1/2 vagy −1/2). Ezek határozzák meg, hogy egy elektron melyik orbitálban és milyen állapotban van.
Elektronkonfigurációs jelölés és példák
Az elektronkonfigurációt általában úgy írjuk le, hogy megadjuk a héjszámot és az alhéj betűjelét, majd a fölötte lévő elektronok számát felső indexként (például 1s2). Gyakori a nemesgáz rövidítés is: az előző nemesgáz elektronkonfigurációját zárójelbe tesszük, majd utánuk írjuk a maradék elektronok eloszlását (például Fe: [Ar] 4s2 3d6).
Pár tipikus példa:
- H: 1s1
- He: 1s2
- O: 1s2 2s2 2p4
- Fe: [Ar] 4s2 3d6 (gyakran írják így; a 3d és 4s energiája közel van egymáshoz)
Kivételes esetek
Néhány elem esetén az elektronok „átrendeződnek” a stabilabb fél- vagy teljesen kitöltött d-alhéjak miatt. Ismert kivételek például:
- Króm (Cr): elvárható [Ar] 4s2 3d4 helyett valós konfiguráció: [Ar] 4s1 3d5 (egy félkitöltött d-alhéj stabilitása miatt).
- Réz (Cu): elvárható [Ar] 4s2 3d9 helyett: [Ar] 4s1 3d10 (teljesen kitöltött d-alhéj előnyösebb).
Az ilyen kivételek oka az elektron–elektron kölcsönhatások és az energiák nagyon kis különbsége a 4s és 3d pályák között.
Miért fontos az elektronkonfiguráció?
- Az elektronkonfiguráció határozza meg az atom kémiai tulajdonságait, például a vegyértéket és a kötőképességet.
- A periódusos rendszer felépítése — csoportok és periódusok — közvetlenül kapcsolódik az elektronkonfigurációk ismétlődéséhez.
- Segít megérteni az anyagok mágneses, elektronikai és optikai tulajdonságait is.
Összefoglalva: az elektronkonfiguráció leírja, hogy az atomok elektronjai milyen sorrendben és milyen pályákon helyezkednek el. Az s, p, d és f alhéjak formája és kapacitása, valamint az Aufbau-, Pauli- és Hund-elv szabályai együtt teszik lehetővé, hogy megértsük az atomok viselkedését és a periódusos rendszer szerkezetét.