Az aminosavak a fehérjék alapvető építőkövei: az eukariótákban általában 20 standard aminosav fordul elő, amelyekből a sejtek szinte minden fehérjéje felépül. A sorrendjük határozza meg a fehérje háromdimenziós szerkezetét és funkcióját, ezért az aminosavak szerepe hasonlítható egy betűkészlethez: korlátozott számú „betűből” nagyon sokféle „szöveg” írható.
Mi az aminosav (biokémiai értelemben)?
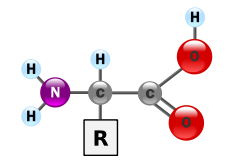
A biokémiában az aminosav minden olyan molekula, amely egyszerre tartalmaz egy amin csoportot (–NH2) és egy karboxil csoportot (–COOH). Gyakori az alfa-aminosavak általános képlete: H2N–CHR–COOH, ahol R az oldallánc (oldalcsoport), amely az egyes aminosavakat megkülönbözteti (lásd az ábrát). Fizikai körülmények között (pl. fiziológiás pH-n) az aminosavak zömök formában zwitterionként vannak jelen, azaz az amin csoport protonálódhat (–NH3+) és a karboxil deprotonálódhat (–COO–), így az összmolekula semleges, de két töltéspontot hordoz.
Alapvető szerkezeti és kémiai jellemzők
- Chirális centrum: a legtöbb aminosav alfa-szénatomja királis; a fehérjékben kizárólag L-konfigurációjú aminosavak fordulnak elő (kivéve a glicint, amely achirális).
- Peptidkötés: aminosavak között kondenzációs reakcióval (vízkilépéssel) peptidkötés (–CO–NH–) jön létre, így épülnek fel a peptidek és fehérjék.
- Oldalláncok (R): kémiai tulajdonságaik (nem poláris, poláris, savas vagy bázikus) meghatározzák az aminosav viselkedését és a fehérje szerkezetét.
- Ionizáció: minden aminosavnak jellegzetes pKa-értékei vannak (amin-, karboxil- és egyes oldalláncok esetén), ami befolyásolja töltését és kölcsönhatásait különböző pH-kon.
Osztályozás oldallánc szerint
Az aminosavakat gyakran az oldalláncuk tulajdonsága szerint csoportosítjuk. A legismertebb csoportok:
- Nem poláris, apoláris: glicin (Gly), alanin (Ala), valin (Val), leucin (Leu), izoleucin (Ile), metionin (Met), fenilalanin (Phe), triptofán (Trp), prolin (Pro).
- Poláris, töltés nélküli: szerin (Ser), treonin (Thr), cisztein (Cys), tirozin (Tyr), aszparagin (Asn), glutamin (Gln).
- Savas (negatív töltésű) oldalcsoportok: aszparaginsav (Asp), glutaminsav (Glu).
- Bázikus (pozitív töltésű) oldalcsoportok: lizin (Lys), arginin (Arg), hisztidin (His).
Esszenciális és feltételesen esszenciális aminosavak
A 20 standard aminosav közül az ember számára kilenc esszenciális, azaz a szervezet nem képes nagyobb mennyiségben előállítani őket más vegyületekből (szintetizálni), ezért táplálékkal kell bevinni őket. Ezek:
- hisztidin (His)
- izoleucin (Ile)
- leucin (Leu)
- lizin (Lys)
- metionin (Met)
- fenilalanin (Phe)
- treonin (Thr)
- triptofán (Trp)
- valin (Val)
Ezen felül egyes aminosavak életkor vagy betegség esetén feltételesen esszenciálissá válhatnak: például az arginin bizonyos növekedési fázisokban, vagy a cisztein és a tirozin, melyek más aminosavakból (metioninból és fenilalaninból) képződnek. Az esszenciális aminosavak listája fajonként is eltérhet; a növényevőknek például különösen figyelniük kell az étrendi forrásokra, mert egyes növényi fehérjékben adott aminosav korlátozó lehet.
Táplálkozás és források
A húsok, tojás és tejtermékek teljes fehérjeforrásoknak számítanak (minden esszenciális aminosavat tartalmaznak megfelelő arányban). Sok növényi eredetű élelmiszer (hüvelyesek, gabonafélék, diófélék) jelentős aminosavforrás, de gyakran egy-egy esszenciális aminosav aránya alacsonyabb, ezért növényi alapú étrendnél a különböző növényi fehérjék kombinálása (pl. bab + rizs) biztosítja a teljes aminosav-összetételt.
A fűből táplálkozó növényevőknek speciális stratégiáik vannak: például a kérődzők (mint a tehenek) a bendőjükben élő mikrobák segítségével képesek bizonyos aminosavakat és fehérjéket előállítani, így kielégítik szükségletüket olyan táplálékból is, ami más emlősök számára nem teljes értékű.
Funkciók az emberi szervezetben
- Fehérjeszintézis: az aminosavak építőkockái a test struktúráinak és enzimjeinek.
- Prekurzorok: több aminosavból fontos molekulák képződnek: például a triptofánból szerotonin, a tirozinból dopamin és noradrenalin, az argininból nitrogén-oxid (NO).
- Antioxidánsok és gon-átalakítás: a glutathion (glutamát–cisztein–glycin) fontos antioxidáns; kreatin és kreatinfoszfát izomenergetikában vesz részt (glycin és arginin prekurzorok).
- Energiaforrás és glukoneogenezis: éhezés vagy intenzív fizikai terhelés alatt bizonyos aminosavak szénvázát a máj glükózzá alakíthatja.
- Reguláció és jelátvitel: sok aminosav és származékuk (pl. hisztidinból képződő hisztamin) fiziológiai szabályozó szerepet tölt be.
- Poszttranszlációs módosítások: a fehérje-oldalláncok foszforilációja, acetilációja, metilációja vagy glicoszilációja befolyásolja a fehérje működését és lokalizációját.
Emésztés és felszívódás
A táplálékkal bevitt fehérjéket a gyomor- és bélrendszer proteázai (pl. pepszin, tripszin, kimotripszin) darabolják di- és tripeptidekre, illetve szabad aminosavakra. A bélhámsejtek speciális transzporterek segítségével veszik fel ezeket, majd a véráramon keresztül a májhoz és más szövetekhez kerülnek. A felszívódás folyamata fontos a táplálkozási hiányok és a gyógyszeradagolás szempontjából is.
Összefoglalás
Az aminosavak sokoldalú, alapvető biomolekulák: a fehérjék építőkövei, anyagcserében betöltött központi szerepük és szerepük a jelátvitelben, antioxidáns védelemben, valamint energetikai és anyagforgalmi utakban mind kritikusak. Az emberi étrendben a kilenc esszenciális aminosav megfelelő bevitele létfontosságú, és bizonyos élettani állapotokban további aminosavak válnak feltételesen esszenciálissá.