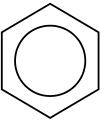
Az aromás szénhidrogén vagy arén egy szénhidrogéngyűrűs vegyület. A szénatomok között gyűrűket alkotó kettős és egyszerű kötések váltakoznak, de a valódi szerkezetet a delokalizált π-elektronrendszer írja le, amely a gyűrű mentén egyenletes elektroneloszlást biztosít. Sok vegyületnek édes vagy jellegzetes illata van, innen ered az „aromás” kifejezés. Az aromás vegyületek hat szénatomból álló gyűrűjét benzolgyűrűnek nevezik, a legegyszerűbb ilyen gyűrű a benzol. Az aromás szénhidrogének lehetnek monociklusos (MAH) vagy policiklusos (PAH) szénhidrogének.
Mi teszi aromássá a vegyületet?
Egy vegyület aromás akkor, ha teljesíti az aromásság feltételeit: zárt, sík gyűrűs szerkezet, konjugált π-kötésrendszer és a Hückel-szabály szerinti (4n+2) π-elektronszám. Az ilyen rendszerekben a π-elektronok delokalizálva stabilizálják a molekulát, ezért az aromás rendszerek általában reaktívabbak bizonyos szempontból (pl. elektrofíliás szubsztitúcióra vannak hajlamosak), ugyanakkor több reakciótípusban nagyobb stabilitást mutatnak, mint a nem aromás alkének.
Típusok és példák
- Monociklusos aromások (MAH): a legismertebb példa a benzol. Hozzátartoznak a toluol, xilolok és különféle szubsztituált benzolok, amelyeket oldószerként, kiindulási anyagként és ipari alapanyagként használnak.
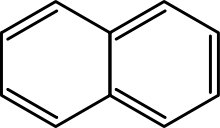
- Policiklusos aromás szénhidrogének (PAH): két vagy több kondenzált benzolgyűrűt tartalmaznak, például naphthalin, antracén, fenanthrén. Sok PAH természetes úton keletkezik tökéletlen égés során, és környezeti szennyezők lehetnek.
- Heteroarének: néhány nem benzol alapú vegyület, az úgynevezett heteroarének, amelyek a Hückel-szabályt követik, szintén aromás vegyületek. Ezekben a vegyületekben legalább egy szénatomot oxigén, nitrogén vagy kén valamelyikével helyettesítenek. Gyakori példák: piridin, furan, tiofén, pirrol.
Fizikai és kémiai tulajdonságok
- Szerkezeti jellegzetesség: aromás gyűrűk sík geometriájúak, és a gyűrűn belüli kötéshosszak kiegyenlítettek a delokalizáció miatt.
- Reakciók: az aromás vegyületek jellemzően elektrofíliás aromás szubsztitúció (EAS) útján reagálnak — tipikus reakciók a nitrálás, szulfonálás, halogénezés, Friedel–Crafts alkilezés/acilezés. Hidrogénezésük nagyobb energiát igényel, mint a nem aromás alkéneké, mivel az aromás stabilitás elvesztésével jár.
- Spektrális tulajdonságok: aromás gyűrűk jól felismerhetők NMR-ben a jellegzetes aromás kémiai eltolódásokkal, UV–Vis-ben látható π→π* átmenetekkel, és IR-ben a C–H és C=C rezgések jellemző sávjaival.
- Oldhatóság és halmazállapot: kisebb aromások általában folyékonyak és apoláris oldószerekben jól oldódnak; nagyobb PAH-ok szilárdak, alacsony vízoldékonysággal.
Előfordulás, előállítás és felhasználás
- Természetes és ipari források: aromások keletkeznek növényi eredetű illóolajokban, kőolajfrakciókban és égési folyamatok során (pl. gépjármű-kipufogógáz, füst).
- Előállítás: iparilag aromatizálás (dehidrogenezés), Friedel–Crafts-reakciók és különböző katalitikus átalakítások révén állítanak elő szubsztituált aromás vegyületeket.
- Felhasználás: oldószerek, műanyag-, festék- és gyógyszeripari kiindulási anyagok, robbanóanyagok és kozmetikumok alkotórészei lehetnek.
Környezet és egészség
Sok PAH és egyes szubsztituált aromások toxikusak vagy karcinogének (például a benzo[a]pirén). Az aromás szénhidrogének környezeti perzisztenciája és lipofilitása miatt bioakkumulálódhatnak, ezért lég- és vízszennyezés szempontjából fontos szerepük van. Az ipari és laboratóriumi munkavégzés során megfelelő védőintézkedések szükségesek (szellőzés, személyi védelem), továbbá tűz- és robbanásveszély miatt gyúlékonyak lehetnek.
Rövid összefoglaló
Az aromás szénhidrogének különleges, delokalizált π-elektronrendszerrel rendelkező gyűrűs vegyületek, amelyek stabilitásuk, jellegzetes kémiai reakcióik (pl. elektrofíliás aromás szubsztitúció) és széles körű ipari illetve környezeti jelentőségük miatt fontosak a kémiában. A heteroarének — ahol a gyűrűben oxigén, nitrogén vagy kén fordul elő — kiterjesztik az aromás rendszerek sokféleségét, miközben továbbra is megfelelnek a Hückel-szabálynak.