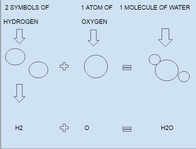
A kémiai képlet a kémikusok által használt módszer a molekulák leírására. A képlet megmondja, hogy milyen atomok és az egyes típusokból hány van a molekulában. Néha a képlet megmutatja, hogy az atomok hogyan kapcsolódnak egymáshoz, néha pedig azt, hogy az atomok hogyan helyezkednek el a térben.
A betű azt mutatja, hogy az egyes atomok milyen kémiai elemek. Az index az egyes atomtípusok számát mutatja. Például a hidrogén-peroxid képlete H2 O .2 A metánnak egy szénatomja (C) és négy hidrogénatomja van; a kémiai képlete CH4 . A cukormolekula, a glükóz hat szénatomból, tizenkét hidrogénatomból és hat oxigénatomból áll, így a kémiai képlete C 6H 12O 6.
A kémiai képleteket kémiai egyenletekben használják a kémiai reakciók leírására.
A 19. századi svéd kémikus, Jöns Jacob Berzelius dolgozta ki ezt a rendszert a kémiai képletek írására.
Alapfogalmak és jelölési szabályok
- Elem jelölése: Minden kémiai elemnek van egy nagybetűs szimbóluma (például C, H, O, Na). Ha a vegyjel két betűből áll, a második betű kisbetű (például He, Cl).
- Alsó indexek (indexek): Az elem mellé írt kicsi számmal (n) jelöljük, hány atom található belőle a részecskében (pl. H2O jelenti, hogy két hidrogén és egy oxigénatom van).
- Az 1-es indexet általában nem írjuk: CH4-ben nem írjuk C1 vagy H4 helyett H4 továbbra is, de C-t nem írunk C1-ként.
- Szorzás/koefficiensek: Kémiai egyenletekben a molekulák elé írt szám (például 2H2O) azt jelenti, hogy kétszer annyi molekula szerepel. Ez nem része a molekula összetételének, csak az egyenletben szereplő mennyiséget adja meg.
Formulák típusai
- Molekula- vagy összegképlet (molecular formula): Megadja az egy molekulában lévő atomok számát (pl. C6H12O6 glükóz). Nem mutatja meg a kötéseket vagy a szerkezetet.
- Empirikus képlet (empirical formula): A legegyszerűbb egész számú arányt adja meg az elemek között. Például a benzol molekulájának (C6H6) empirikus képlete CH.
- Szerkezeti képlet: Megmutatja az atomok közötti kötéseket (például vonalakkal). Léteznek részletes képek és egyszerűsített, összevont (condensed) formák is: például etanolra CH3CH2OH.
- Ionos képlet/ionok: Ionoknál a töltést + vagy − jelöli (például Na+, SO42−). Ioncsoportokat zárójelbe teszünk, ha több van belőlük: Ca(OH)2.
Gyakori jelölési elemek és példák
- Zárójelek: Ha egy csoport több példányban szerepel, zárójelezni kell: például aluminium-szulfát Al2(SO4)3.
- Hidrátok: Vízmolekulák kötődnek a kristályszerkezethez ponttal jelölve: CuSO4·5H2O (réz(II)-szulfát-pentahidrát).
- Izotópok: Az atom tömegszámát felső indexként lehet jelezni: 14C jelenti a szén-14 izotópot.
- Hill-rendszer (elemek sorrendje): Organikus vegyületeknél hagyományosan előbb a szén (C), utána a hidrogén (H), majd az összes többi elem ábécé-sorrendben szerepel (pl. C2H5OH). Ha nincs C, akkor minden elem ábécé sorrendben jön.
Olvasási és írási tippek
- Mindig figyelj a nagy- és kisbetűkre (Cl nem CL, és nem cl).
- Ne írj számot az elem jeléhez előtte (például helytelen: 2H2O a molekula belsejében); a molekula összetételét mindig alsó indexekkel jelöljük.
- Az ionoknál tüntesd fel a töltést felső indexként: például SO42−.
- Ha szerkezeti információt is szeretnél adni, használj szerkezeti képletet vagy összevont formát (pl. CH3CH2OH a lehetséges kötéseket is tükrözi).
Rövid gyakorlati példák magyarázattal
- H2O — víz: két hidrogén- és egy oxigénatom; molekulaképlet.
- H2O2 — hidrogén-peroxid: két hidrogén- és két oxigénatom; erős oxidálószer.
- CH4 — metán: egy szén- és négy hidrogénatom; egyszerű alkán.
- NaCl — nátrium-klorid (ionvegyület): Na+ és Cl− ionokból áll; az összegképlet az ionok arányát tükrözi.
- Ca(OH)2 — kalcium-hidroxid: egy Ca2+ és két OH− ion; zárójelek szükségesek az OH-csoport többszörös előfordulásához.
Összefoglalás
A kémiai képletek tömören és pontosan adják meg egy anyag összetételét. Megkülönböztetünk egyszerű összegképleteket, amelyek csak az atomok számát mutatják, és szerkezeti képleteket, amelyek a kötéseket és atomrendeződést is ábrázolják. A helyes jelölés ismerete fontos a kémiai számításokhoz, reakciók leírásához és a vegyületek közötti különbségek megértéséhez.