A pentán egy szerves vegyület, amelynek kémiai képlete C
5H
12. Öt szénatomot tartalmazó alkán. Általában a "pentán" mindhárom izomer (n-pentán, izopentán és neopentán). Az IUPAC-ban azonban a pentán csak az n-pentánt jelenti. Az IUPAC-ban a másik két izomer a 2-metilbután és a 2,2-dimetilpropán. A ciklopentán kémiai képlete: C
5H
10, tehát nem a pentán izomerje.
Általános jellemzés
A pentán (C5H12) telített szénhidrogén, szobahőmérsékleten színtelen, jellegzetes szagú, illékony és gyúlékony folyadék/gáz (izomerektől függően). Főként kőolaj-frakciókban fordul elő, és a finomításból származó üzemanyagok összetevője. Kémiailag viszonylag kevésbé reakcióképes, mint a funkciós csoportot tartalmazó vegyületek, de könnyen vesz részt radikális reakciókban (pl. szubsztitúció halogénekkel) és égésben.
Izomerek és szerkezet
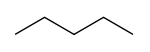
- n-pentán (pentán, IUPAC neve: pentán): egyenes láncú alkán. Legstabilabb lánckonformációk: anti és különböző gauche alakok.
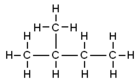
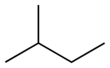
- izopentán (2-metilbután): egyszeresen elágazó molekula (egy metilcsoport a 2. szénatomon).
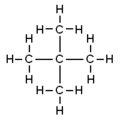
- neopentán (2,2-dimetilpropán): erősen elágazó, szimmetrikus szerkezet (a központi szénhez négy metil csoport kapcsolódik két szénatomon át), ami befolyásolja fizikai tulajdonságait (pl. olvadáspontja viszonylag magas a szimmetria miatt).
Fizikai tulajdonságok (összefoglaló)
- Állapot: szobahőmérsékleten folyadék (néhány izomer könnyen gőzzé alakul).
- Móláris tömeg: 72,15 g·mol−1.
- Kinézet: színtelen, átlátszó folyadék (folyékony halmazállapotban a kondícióktól függően).
- Forráspontok (megközelítő értékek):
- n-pentán: kb. 36,1 °C
- 2-metilbután (izopentán): kb. 27,8 °C
- 2,2-dimetilpropán (neopentán): kb. 9,5 °C
- Olvadáspontok (példák):
- n-pentán: kb. −129,7 °C
- 2-metilbután: kb. −160 °C
- neopentán: kb. −16,6 °C (a szimmetria miatt relatíve magasabb olvadáspont)
- Sűrűség: folyékony pentánok sűrűsége körülbelül 0,60–0,63 g·cm−3 (20 °C körül), tehát könnyebbek a víznél.
- Oldhatóság: vízben gyakorlatilag oldhatatlan, de jól oldódik szerves oldószerekben (éter, benzén stb.).
Kémiai tulajdonságok
- Égés: teljes égés esetén: C5H12 + 8 O2 → 5 CO2 + 6 H2O. Rossz égés részleges égéshez, CO-képződéshez vezethet.
- Radikális szubsztitúció: alkil-halogenidek előállítására alkalmas halogénekkel és UV-sugárzással (láncreakciós mechanizmus, primer/másodlagos szénatomok reaktivitási különbségei).
- Katalitikus átalakulások: hő- vagy katalizátoralapú krakkolás, izomerizáció és dehidrogenálás lehetséges ipari körülmények között.
- Stabilitás: telített alkánként viszonylag kémiailag inaktív, ellenáll a savas és bázisos környezetnek, de oxidálószerekkel erősen reagál.
Előfordulás és előállítás
A pentán elsősorban a kőolaj-finomítás melléktermékeként és frakciói között található (gázolaj, könnyű benzinek). Ipari előállítása történt frakcionált desztillációval, valamint katalitikus krakkolással és reformálással. Laboratóriumban szintetizálható egyszerű szerves reakciókkal is, de ipari szinten a fosszilis források olcsóbb forrást jelentenek.
Felhasználás
- Oldószerként laboratóriumban és iparban.
- Hűtőközegként és habfúvószerként (pl. polisztirol hab előállításában), ahol alacsony forráspontú alkánokra van szükség.
- Gázolaj- és benzinkeverékek alkotóeleme, könnyű üzemanyag-összetevő.
- Nyersanyagként szerves szintéziseknél.
Biztonság és egészség
- Gyulladásveszély: igen gyúlékony; gőzei levegővel robbanóképes elegyet képezhetnek. Kerülni kell a nyílt lángot, szikrát, hőt.
- Belégzés: nagy koncentrációban központi idegrendszeri depressziót, fejfájást, szédülést okozhat.
- Bőr- és szemkontaktus: irritációt okozhat; tartós bőrkontaktus szárító hatású lehet.
- Környezeti hatás: illékony szerves vegyület (VOC), hozzájárulhat légköri fotokémiai szennyeződéshez.
- Tárolás: jól szellőző, hő- és gyújtóforrástól távoli helyen, földelt és robbanásbiztos berendezéssel.
Megjegyzés a ciklikus öt szénatomos vegyületekről
A ciklopentán kémiai képlete C
5H
10, tehát nem izomerje a pentánnak, mert gyűrűs szerkezete miatt két hidrogénatom hiányzik (telített gyűrűhöz kötődő szén-szén kötés). A ciklikus és az aciklusos C5 vegyületek eltérő fizikai és kémiai tulajdonságokkal rendelkeznek.
Rövid összefoglalás
A pentán (C5H12) egyszerű, telített szénhidrogén, amely három fő aciklusos izomerrel rendelkezik: n-pentán, 2-metilbután és 2,2-dimetilpropán. Ezekkel a vegyületekkel a finomítás és az ipari szintézisek során gyakran találkozunk; fontos szerepük van oldószerként, üzemanyag-összetevőként és habfúvószerként. Fizikai és kémiai tulajdonságaik — pl. forráspont, olvadáspont, illékonyság és reakciókészség — jelentősen függnek a molekulaszerkezettől és az elágazottságtól.