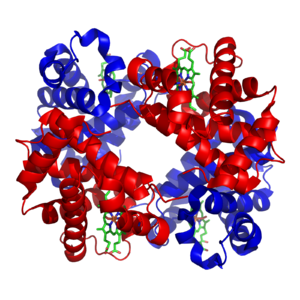
A globuláris fehérjék a fehérjék egyik gyakori és változatos csoportját alkotják. Jellemzőjük a kompakt, általában gömbszerű (globuláris) térszerkezet, amelyet a polipeptidláncok hajtogatódása eredményez.
Definíció és szerkezet
Ezek a fehérjék a fehérjék hajtogatásának eredményeként kialakuló harmadlagos (és gyakran negyedleges) szerkezettel rendelkeznek: a láncok belsejében elsősorban hidrofób oldalláncok helyezkednek el, míg a felszínen hidrofil (vízkedvelő) csoportok találhatók, ezért sok globuláris fehérje jól oldódik vízben. Léteznek azonban olyan globuláris fehérjék is, amelyeknek a felszínén hidrofób foltok találhatók (pl. kölcsönhatások vagy membránhoz kötődés céljából), így ezek oldhatósága eltérő lehet.
Típusok és példák
A globuláris fehérjék igen változatosak: enzimek, hormonok, transzportfehérjék, receptorok, antitestek és számos más funkcionális fehérje tartozik ide. Példák a csoportból: a mioglobin és a hemoglobin, amelyek oxigénszállító és -raktározó szerepet töltenek be.
Biológiai szerepek
Ellentétben a kizárólag szerkezeti szerepet betöltő rostos fehérjékkel, a globuláris fehérjék sokféle dinamikus funkciót látnak el. Tipikus feladataik:
- Az enzimek a szervezetben zajló szerves reakciókat katalizálják, általában enyhe körülmények között és nagyfokú specificitással — például különböző észterázok és más enzimek végzik ezeket a feladatokat.
- hírvivők, azaz olyan molekulák előállítása és közvetítése, amelyek üzeneteket továbbítanak a biológiai folyamatok szabályozására. Ezt a funkciót a hormonok, például az inzulin, és más jelátvivő fehérjék látják el.
- Más molekulák transzportereiként és hordozóiként működnek a sejtekben és a membránokon keresztül történő anyagforgalomban.
- Aminosavkészletek biztosítása: egyes fehérjék tartalékként szolgálnak aminosavak számára (például tápláléktartalékok vagy fejlődés során felszabaduló források).
- Szabályozás: sok molekula aktivitását, szerkezetét vagy lokalizációját globuláris fehérjék szabályozzák (pl. alloszterikus szabályozás, inhibitorok és aktivátorok révén).
- Vannak olyan, alapvetően strukturális szerepű fehérjék is, mint az aktin és a tubulin, amelyek monomerként gyakran oldódó, gömbszerű elemekből állnak, de polimerizálódva hosszú, merev filamentumokat hoznak létre, így kombinálják a globuláris és rostos jellemzőket.
Szerkezet–funkció összefüggés
A globuláris fehérjék működését a térszerkezet határozza meg: az enzimaktív helyek, kötőfelületek és alloszterikus centrumok egyedi elrendeződése biztosítja a specifikus kötődést és katalízist. A negyedleges szerkezet — amikor több polipeptidlánc (alunit) kapcsolódik össze — különösen fontos például a hemoglobin esetében, ahol az alunitok közötti kölcsönhatások befolyásolják az oxigénkötést.
A stabilitást hidrogénkötések, ionos kölcsönhatások, diszulfidkötések és a hidrofób hatások egyaránt biztosítják. A külső környezet (pH, ionerősség, hőmérséklet) vagy kémiai anyagok megváltoztatása a fehérjék denaturációjához, funkcióvesztéséhez vezethet.
Vizsgálati módszerek és klinikai jelentőség
A globuláris fehérjéket többféle módszerrel tanulmányozzák: röntgenkrisztallográfia, NMR-spektroszkópia, kriogén elektronmikroszkópia (cryo-EM), cirkuláris dichroizmus és tömegspektrometria segítik a szerkezet és funkció feltárását. Klinikai szempontból fontos, hogy a fehérjék hibás hajtogatódása és aggregációja neurodegeneratív betegségekhez (pl. Alzheimer-, Parkinson-kór) és más betegségekhez vezethet; emellett a hormonális és enzimatikus globuláris fehérjék hiánya vagy működési zavara számos anyagcserezavart okozhat.
Összefoglalva: a globuláris fehérjék a sejt életműködésének sokoldalú végrehajtói — katalizálnak reakciókat, közvetítenek jeleket, szállítanak molekulákat és részt vesznek a sejtes szabályozásban. Példáik, mint a mioglobin és a hemoglobin, jól szemléltetik, hogyan kapcsolódik össze a szerkezet és a biológiai funkció.