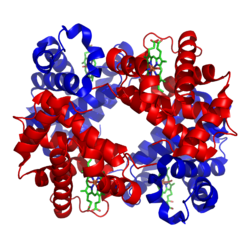
A hemoglobin (vagy hemoglobin) a vörösvértestek fehérjéje, amely vasat tartalmaz. Az emberi szervezetben elsősorban az oxigén szállítására szolgál: a tüdőben felveszi az oxigént, majd a szövetek felé továbbítja. A hemoglobin a fehérvérű halak kivételével minden gerinces állat vörösvérsejtjeiben megtalálható, és egyes gerinctelen állatokban is előfordul. Néhány más gerinctelen állat más vegyi anyagokat, például hemocianint használ az oxigénszállításhoz.
Szerkezete
A hemoglobin egy tetramer: négy fehérjeláncból (globinokból) áll, amelyekhez négy hemtömcs (porfirinváz + centrális vasatom) kapcsolódik. A felnőtt emberben a leggyakoribb formája az HbA, amely két alfa (α) és két béta (β) láncból áll (α2β2). Minden egyes hemtömcs egy Fe2+ vasatomot tartalmaz, amelyhez egy oxigénmolekula kapcsolódhat — így egy hemoglobinmolekula összesen négy oxigénmolekulát képes szállítani.
Működése és gázszállítás
A hemoglobin nemcsak az oxigént szállítja, hanem a szervezet légúti szén-dioxidjának egy részét is (kb. 20–25%). A szén-dioxid egy része hemoglobinhoz kötődve, karbaminoformában jut vissza a tüdőbe. Emellett a hemoglobin részt vesz a vér pH-jának szabályozásában is, mivel képes H+ ionokat megkötni és szállítani.
Az oxigénkötődés jellemzője a kooperativitás: amikor egy oxigénmolekula kötődik az egyik hez, a maradék hetek oxigénhez való affinitása megnő, így a kötődés görbéje szigmoid (S-alakú). Ez segíti a tüdőben a felvételt és a szövetekben a leadást. Az oxigénhez kötött hemoglobint gyakran oxihemoglobinnak nevezzük.
Speciális formák és kóros kötődések
A magzatok hemoglobinja (HbF) magasabb oxigénaffinitású, mint az anyai hemoglobin, ami előnyös az anyai magzati oxigénátvétel szempontjából. Léteznek további normál izoformák (például HbA2) és sok öröklött vagy szerzett eltérés: a szicklecellás betegségben egy pontmutáció miatt az egyik béta-láncban eltérés jön létre (HbS), a thalassaemiák pedig a globinláncok termelésének csökkenésével járnak.
Néhány anyag kórosan köti a hemoglobint: a szén-monoxid nagyon erősen kapcsolódik a hemoglobinhoz (carboxyhemoglobin képződik), ezért CO-mérgezésnél az oxigénszállítás hatékonysága súlyosan csökken. A hemoglobin vasatomának oxidációja (Fe2+ → Fe3+) methemoglobint hoz létre, amely nem képes oxigént kötni — ez is csökkentheti a szöveti oxigénellátást.
Élettani forgalom, szintézis és lebontás
A hemoglobin szintézise a csontvelőben zajlik, a vörösvértestek fejlődése (eritropoezis) során. A folyamathoz vasra, valamint megfelelő mennyiségű B12-vitaminra és folsavra van szükség. Egy egészséges vörösvértest élettartama körülbelül 120 nap; elöregedett vagy sérült sejtek a lépben és a májban bomlanak le. A hem leből bilirubin keletkezik (ami az epefestékek közé tartozik), a vas visszakerül a vasraktárakba és újrahasznosítható.
Klinikai jelentőség
A hemoglobin koncentrációja fontos laboratóriumi paraméter: teljes vérkép (CBC) részeként mérik. Tipikus referenciaértékek felnőttekben (könnyű eltérések laboronként):
- férfiak: kb. 13,8–17,2 g/dL
- nők: kb. 12,1–15,1 g/dL
Gyakoribb klinikai vizsgálatok és fogalmak: hematokrit (a vérsejtek térfogataránya), MCV, MCH, MCHC (a vörösvérsejtek méretére és hemoglobintartalmára vonatkozó mutatók). A pulzoximéter noninvazívan becsli az artériás oxigénszaturációt az oxi- és deoxihemoglobin fényelnyelési különbsége alapján.
Összefoglalás
A hemoglobin alapvető szerepet játszik az oxigén és részben a szén-dioxid szállításában, emellett a vér színét is a hemoglobin adja. Szerkezete és működése lehetővé teszi a hatékony gázcserét a tüdő és a szövetek között, miközben számos betegségi állapot (például anémia, hemoglobinopathiák, CO-mérgezés, methemoglobinémia) közvetlenül befolyásolja a szervezet oxigénellátását.