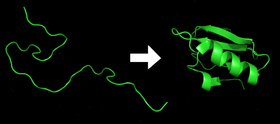
A fehérje hajtogatása az a folyamat, amelynek során a molekula elnyeri működéséhez szükséges háromdimenziós alakját, azaz a konformációját — más szóval a funkcionális alakját. Ez általában egy önszerveződő folyamat: a láncban levő aminosavak egymással kölcsönhatva rendeződnek, és létrejön a működőképes szerkezet.
A hajtogatás fő lépései és szerkezeti szintek
Röviden a folyamat lépései:
- Minden fehérje egy kibontatlan polipeptidként vagy véletlenszerű tekercsként létezik, amikor az mRNS-szekvenciából lineáris aminosavlánccá fordítják le. Ez a polipeptid kezdetben nem rendelkezik kifejlett háromdimenziós szerkezettel.
- Az aminosavak kölcsönhatásba lépnek egymással, hogy egy jól meghatározott háromdimenziós szerkezetet, a hajtogatott fehérjét hozzanak létre. Ezt nevezzük natív állapotnak. Az így kialakuló szerkezetet alapvetően az aminosav-szekvencia határozza meg (vö. Anfinsen dogmája).
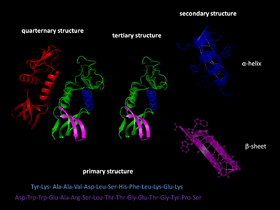
A fehérjék szerkezetét hagyományosan négy szintre szokás bontani:
- Primer szerkezet: az aminosavak sorrendje a láncban.
- Szekunder szerkezet: lokális elemek, például α-hélixek és β-lemezek, amelyeket főként hidrogénkötések tartanak össze.
- Terciér szerkezet: az egész polipeptid háromdimenziós elrendeződése — a lánc összecsuklása eredményezi a működő formát.
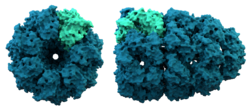
- Kvaterner szerkezet: több fehérjeszubegység összekapcsolódása egy komplexbe (ha a fehérje több láncból áll).
Molekuláris erők és mechanizmusok
A hajtogatást többféle kölcsönhatás vezérli: hidrofób hatás (a nem poláris oldalláncok belső irányba rendeződnek), hidrogénkötések, elektrosztatikus kölcsönhatások, diszulfidkötések (ciszteinek között), valamint van der Waals-erők. A hajtogatás energetikailag egy ún. energia-üdülők (funnel) mentén zajlik: a rendszert csökkenő szabadenergiába vezeti, amíg eléri a stabil natív állapotot.
Sejten belüli sajátosságok: kotranszlációs hajtogatás és segítő gének
A valós sejtben a hajtogatás gyakran kotranszlációsan történik: a polipeptidlánc már a riboszómánál elkezd összeállni. A sejt speciális chaperon fehérjéi segítik a folyamatot és megelőzik a hibás összecsapódást. Példák:
- Hsp70 család: megköti a részben kibomlott láncokat, megakadályozva az aggregációt.
- Chaperoninok (például GroEL/GroES): zárt kamrában biztosítanak megfelelő környezetet a hajtogatáshoz.
- Diszulfid-izomerázok és peptid-proil-cisz-transz izomerázok: katalizálják bizonyos kötésátalakításokat, amelyek szükségesek lehetnek a helyes hajtogatáshoz.
A sejt proteosztázis-rendszere (minőségellenőrzés) magába foglalja a hibás fehérjék felismerését és lebontását, például a proteaszóma és az autofágia útján.
Hibás hajtogatás és egészségügyi hatások
Ha egy fehérje nem a natív alakjába hajtódik, gyakran inaktívvá válik és hajlamos aggregálódni; ezek az aggregátumok sokszor toxikusak. Számos betegség kapcsolódik a hibásan hajtódó fehérjékhez:
- Neurodegeneratív betegségek: Alzheimer-kór (β-amiloid és tau), Parkinson-kór (α-szinuklein), Huntington-kór (polyQ aggregátumok).
- Prion-betegségek: a prionfehérjék konformációváltása fertőző aggregátumokhoz vezet.
- Genetikai betegségek: például a cisztás fibrózis egyes mutációi (CFTR) hibás hajtogatást és degradációt okoznak.
Emellett a fehérjék hajtogatása szerepet játszik az immunválaszban és az allergiát a kiváltó folyamatokban: az immunrendszer szelektíven ismer fel szerkezeteket, és nem termel antitesteket minden lehetséges fehérjeszerkezet ellen, ezért egy adott konformáció erősebb immunválaszt válthat ki.
Kutatási módszerek és gyakorlati alkalmazások
A fehérjehajtogatás vizsgálatára sok módszert használnak: röntgenkrisztallográfia, nuclear magnetic resonance (NMR), cryo-EM, cirkuláris dichroizmus (CD), fluoreszcencia alapú kinetikai mérések és biokémiai denaturációs vizsgálatok. Ezek segítségével megérthető a szerkezet, a stabilitás és a hajtogatási útvonal.
A hajtogatás ismerete fontos a gyógyszerfejlesztésben (hibás hajtogatás elleni terápia, chaperon modulátorok), a biotechnológiában (rekombináns fehérjék helyes előállítása) és a diagnosztikában.
Fontos elméleti gondolatok
Az Anfinsen dogmája arra utal, hogy az aminosav-sorrend általában meghatározza a natív szerkezetet — de a sejten belüli környezet, chaperonok és poszttranszlációs módosítások gyakran döntő szerepet játszanak. A Levinthal-paradoxon azt mutatja, hogy a fehérjék nem véletlenszerűen tesztelnek minden konformációt; helyette energia- és kinetikai úton, irányított összehajtogatással jutnak el a natív állapothoz.
Összefoglalás
A fehérje hajtogatás kritikus biológiai folyamat, amely meghatározza a fehérjék működését és stabilitását. A sejtben speciális segítő mechanizmusok biztosítják, hogy a legtöbb fehérje gyorsan és hatékonyan érje el natív alakját; amikor ez a rendszer megbomlik, komoly betegségek alakulhatnak ki. A hajtogatás kutatása továbbra is aktív terület, mert jobb megértése új terápiás lehetőségeket nyithat meg.