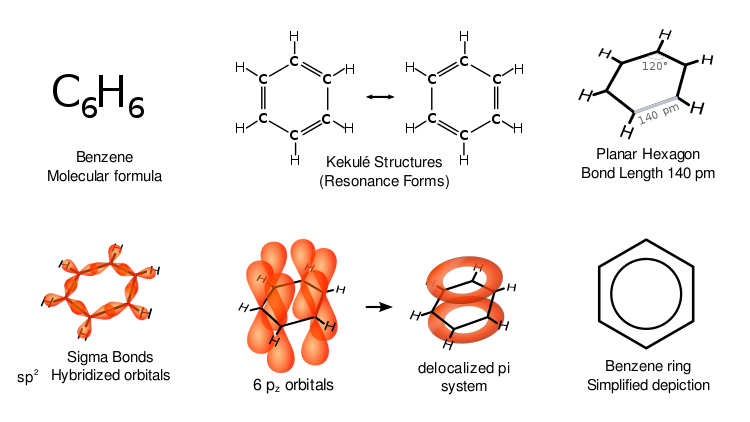Benzol (C6H6): színtelen, gyúlékony aromás vegyület — tulajdonságok, rákkeltő egészségkockázatok és ipari felhasználás (oldószer, alapanyagok).
A benzol, más néven
benzén, egy szerves kémiai vegyület, képlete
6CH6. Színtelen, jellegzetesen édeskés illatú, gyúlékony folyadék. Molekuláját hat szénatom alkotja, amelyek gyűrűt formálnak, és minden szénhez egy hidrogénatom
kapcsolódnak. Ez az elrendezés aromás szerkezetet eredményez: a gyűrű delokalizált π-elektronrendszere miatt a benzol általában nem vesz részt egyszerű addíciós reakciókban, hanem elektrofílikus aromás szubsztitúcióra hajlamos.
Fizikai és kémiai tulajdonságok
- Olvadáspont: kb. 5,5 °C; forráspont: kb. 80,1 °C. - Sűrűség: ~0,88 g/cm3 (20 °C körül). - Vízben gyakorlatilag oldhatatlan (kis mértékben oldódik), jól old más szerves anyagokat. - Nagy a gőznyomása és könnyen párolog, ezért levegőben gyorsan terjed. - Kémiailag stabil aromás vegyület; tipikus reakciói közé tartozik a nitrálás, szulfonálás, halogénezés és alkilezés. Ipari előállításnál és átalakításnál fontos kiindulóvegyület.
Előfordulás és ipari előállítás
A benzol természetesen is előfordul a
nyersolajban, és ezért jelen van a
benzinben. Ipari forrásai közé tartozik a kőolaj-finomítás és a petro-kémiai eljárások (pl. katalitikus reformálás, toluol hidro-dealkilezése). Egyes ipari folyamatok és égési folyamatok (pl. gépjármű-kipufogó, ipari égés) is kibocsátanak benzolt a levegőbe.
Fő felhasználások
A benzolt széles körben használják és számos vegyipari termék alapanyagaként szolgál:
- Oldószerként az iparban és laboratóriumokban, mivel jól old sok szerves anyagot (oldószer).
- Adalékanyagként és komponensként a benzinben (régebben az ólommentesítést és oktánszám növelését szolgálta).
- Kiindulóanyagként műanyagokban, gumiban és színezékekben előállítandó vegyületekhez.
- Ipari előanyag sok más fontos vegyülethez: például fenol, ciklohexán/kaprolaktám (nyersanyag műszálakhoz), styrol, anilin stb.
- Sok gyógyszer és finomkémiai termék molekuláris vázában találhatók benzolgyűrűs részletek.
Egészségkockázatok és toxikológia
A benzol rákkeltő vegyület: hosszabb idejű, tartós expozíció növeli a
rákot, különösen a vérképzőszervi daganatok (pl. akut myeloid leukémia) kialakulásának kockázatát. A fő egészségügyi hatások:
- Akut hatások: belégzés esetén fejfájás, szédülés, fáradékonyság, émelygés, eszméletvesztés súlyosabb expozícióban.
- Krónikus hatások: a csontvelő károsodása (leukopénia, anémia, thrombocytopenia), aplasztikus anémia, fokozott leukémia-kockázat.
- Légzési út a legfontosabb expozíciós út (belégzés), de bőrön át is felszívódhat, illetve ritkán lenyelés útján is veszélyt jelenthet.
Az expozíció csökkentése alapvető: helyi elszívás, zárt rendszerek, megfelelő szellőzés, személyi védőeszközök (gázmaszk, kesztyű) és munkahigiénés szabályok betartása.
Szabályozás és biztonság
- Nemzetközi szervezetek (pl. IARC) a benzolt emberre bizonyítottan rákkeltő anyagként sorolják be. A munkahelyi expozíciós határértékek országonként eltérnek; ezért mindig az adott ország előírásait kell követni. - Veszélyes anyagként történő tárolásnál tartsuk távol gyújtóforrásoktól, jól szellőző, hűvös helyen, eredeti, zárt edényzetben. - Tűz esetén a benzol hevesen ég — gyúlékony gázok képződhetnek; oltáshoz alkoholálló habot, száraz vegyszert vagy szén-dioxidot használjanak, és a tűzoltást képzett személyzet végezze.
Környezetre gyakorolt hatás
A benzol illékony, ezért a levegőbe kerülve gyorsan eloszlik, de lokálisan légszennyezést és szagproblémákat okozhat. Talajba vagy talajvízbe jutva hosszabb ideig szennyező forrás lehet; egyes mikroorganizmusok képesek lebontani, de a környezeti tisztítás gyakran költséges. A kibocsátások csökkentése és a szivárgások megelőzése fontos a környezetvédelem szempontjából.
Elsősegély és teendők expozíció esetén
- Belégzés: friss levegőre vinni az érintettet, szükség esetén orvosi ellátás. Súlyos légzési nehézség vagy eszméletvesztés esetén hívjuk a mentőket. - Bőrkontaktus: a szennyezett ruhát levenni, az érintett bőrfelületet bő vízzel és szappannal alaposan lemosni. - Szembe kerülés: öblítés bő vízzel legalább 10–15 percig, orvosi vizsgálat. - Lenyelés: orvosi ellátás szükséges; hánytatni nem szabad, ha a beteg eszméleténél van. Összefoglalva: a benzol fontos ipari alapanyag, de jelentős egészség- és környezetkárosító hatásokkal jár. Munkahelyi és ipari körülmények között a kitettség szigorú szabályozást, műszaki intézkedéseket és személyi védelmet igényel annak érdekében, hogy minimalizáljuk a rövid- és hosszú távú kockázatokat.

_1964,_MiNr_440.jpg)