A kémiában a konjugált rendszer olyan összekapcsolt p-orbitálisok rendszere, amelyekben delokalizált elektronok vannak. Konjugációt általában úgy kapunk, hogy egymástól váltakozó többszörös és egyszerű kötések sorozata jön létre (pl. C=C–C=C). A konjugált rendszerek csökkenthetik a molekula teljes energiáját, növelhetik stabilitását, és különleges fizikai-kémiai tulajdonságokat eredményeznek. Egy konjugált rendszer tartalmazhat magányos párokat, gyököket vagy karbéniumionokat is, és lehet ciklikus, aciklikus, lineáris vagy vegyes felépítésű. A molekula atomjait általában egyszerű kötések tartják össze, ahol a szomszédos atomok pályái átfedik egymást, és az ilyen átfedés adja a delokalizáció alapját.
Hogyan működik a konjugáció?
A konjugáció lényege, hogy egy p-orbitál átfedése egy másik p-orbitállal a köztük lévő szigma kötésen (vagy egyszerű kötésen) keresztül megengedi a pi-elektronok mozgását több atom között. (Nagyobb atomok esetén a d-orbitálok is hozzájárulhatnak a konjugált rendszerhez.)
Az átfedő p-orbitálisok egy kiterjedt régiót alkotnak, amely áthidalja a köztük lévő egyszerű kötéseket, és lehetővé teszi a pi-elektronok delokalizációját minden, egymással megfelelően igazított p-orbitálison keresztül. A pi-elektronok nem egyetlen kötéshez vagy atomhoz tartoznak, hanem az egész konjugált atomcsoporthoz oszlanak meg.
Feltételek és fontos fogalmak
- Folytonos p-p átfedés: minden atomnak a konjugáció mentén rendelkeznie kell p-orbitállal vagy egyéb olyan pályával (pl. d-orbitál), amely átfed.
- Planaritás: a legtöbb konjugált rendszer hatékony delokalizációhoz közel sík geometriát igényel, mert így az összes p-orbitálison jobb az átfedés.
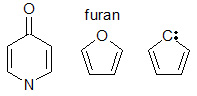
- Elektronok száma és Hückel-szabály: ciklusos, konjugált rendszerek esetén az aromás stabilitás gyakran Hückel 4n+2 szabályával írható le (például a benzén 6 π-elektronnal aromás).
- Resonancia és delokalizáció: a rezonanciaszerkezetek szemléletesek: a valós elektroneloszlás az összes hozzájáruló rezonanciastruktúra szuperpozíciója, ezért a kötésrendek átlagolódnak.
- Különbségek: konjugált (váltakozó kettőssel és egyszerűvel) ≠ kumulált (például alleneknél több egymás melletti kettős kötés) — a kumulált rendszerek nem mindig mutatnak azonos delokalizációt. Létezik továbbá kereszt-konjugáció, ahol a delokalizáció nem egy lineáris láncon, hanem elágazásokkal valósul meg.
Példák
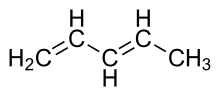
- Nyílt láncú konjugált verseny: 1,3-butadien (CH2=CH–CH=CH2) — egyszerű példa, ahol a π-elektronok delokalizálódnak a négy szénatomon.
- Gyűrűs aromás: benzén — hat π-elektron delokalizált a hatos gyűrűn; erős stabilitás és sajátos reaktivitás jellemzi.
- Vezető polimerek: poli-acetilén és egyéb vezető polimerek — hosszú konjugált láncok, amelyek félig vezető/vezető tulajdonságokat adnak.
- Nagy konjugált rendszerek: grafitban, a vezető polimerekben és a szén nanocsövekben találhatók — ezekben nagyon kiterjedt delokalizáció van, ami vezetőképességhez és speciális mechanikai/térhálós tulajdonságokhoz vezet.
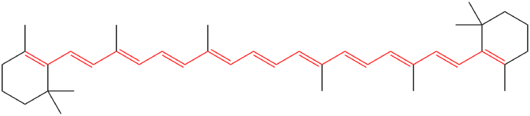
- Biomolekulák és pigmentek: β-karotin és más karotinoidok — a konjugált kettős kötések lánca adja a színt (UV/visible elnyelés).
Hogyan befolyásolja a konjugáció a tulajdonságokat?
- Stabilitás: a delokalizáció általában csökkenti a molekula energiáját, ezért stabilabbak a konjugált rendszerek, mint izolált kettős kötések sorozata.
- Reakciókészség: a konjugált rendszerek másként reagálnak — például 1,3-dieneknél a Diels–Alder reakció, vagy a konjugált ennek megfelelően különböző elektrofil adíciós mintázatokat mutatnak.
- Spektroszkópia: a konjugáció csökkenti a HOMO–LUMO energiakülönbséget, így az elnyelési maximumok vöröseltolódnak (hosszabb hullámhosszra), ezért sok konjugált rendszer színes. A NMR-kémiai eltolódások is jellemzően módosulnak a delokalizáció miatt.
- Elektronvezetés: kiterjedt konjugáció esetén (pl. grafén, polimer vezetők) az elektronok könnyebben mozdulnak el a szerkezetben, ezért javul a vezetőképesség.
Aromás és antiaromás rendszerek
A ciklikus, konjugált rendszerek különleges esete az aromásitás: ha a gyűrű sík és a π-elektronok száma Hückel-szabály szerint 4n+2, akkor az adott rendszer különösen stabil (aromás). Ha viszont 4n π-elektron van, az antiaromás viselkedést eredményezhet, ami rendkívül instabil állapot.
Mérések, elméletek és modellezés
A konjugáció energiáját és hatását különböző módszerekkel lehet vizsgálni: rezonanciaenergiák számítása, elektronikus szerkezetmodellezés (MO-elmélet, DFT), UV–Vis spektroszkópia (elnyelési maximumok), valamint elektrokémiai mérések. Egyszerű elméleti megközelítés a Hückel-módszer, amely jól szemlélteti a π-rendszerek energiaszintjeit és a HOMO–LUMO rés nagyságát.
Gyakorlati alkalmazások
- Festékek és pigmentek: a konjugált rendszerek határozzák meg a színt.
- Organikus elektronika: konjugált polimerek fontosak organikus fénykibocsátó diódákban (OLED), napelemekben és félvezetőkben.
- Katalízis és reakciótervezés: konjugált ligandok és intermediátok szerepe a reakciómechanizmusokban.
Összefoglalva: a konjugált rendszerek kulcsfontosságúak a molekuláris szerkezet, reaktivitás és optikai/elektromos tulajdonságok megértésében. A delokalizált π-elektronok többatomos megoszlása adja sok jellegzetes viselkedésük alapját, ezért a konjugáció ismerete elengedhetetlen a szerves kémiai szerkezet-reakció kapcsolatokban.