A röntgenkrisztallográfia segítségével megismerhetjük egy molekula háromdimenziós szerkezetét. Az atom elektronfelhője kissé elhajlítja a röntgensugarakat, és a kristályról leolvasott diffrakciós képekből számítással vissza lehet állítani az elektron-sűrűség eloszlását, ami alapján fel lehet építeni az atommodellt. Ezáltal a molekuláról egy képernyőn látható "kép" készül. Szerves és szervetlen molekulák esetében egyaránt alkalmazható. Bár a vizsgálat általában nem „megsemmisítő”, a röntgensugárzás okozhat radiációs károsodást, ezért gyakran alkalmaznak kryo-hűtést és alacsony dózist a minta védelmére.
Alapelvek
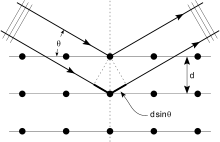
A módszer fizikai alapja, hogy a kristályba érkező röntgensugarak a kristályban rendezetten elhelyezkedő atomok elektronfelhőin szóródnak. A szórt hullámok interferenciája hozza létre a detektált mintázatot. A jellegzetes csúcsok helye és intenzitása alapján számítják ki az elektron-sűrűség Fourier-transzformáltját. A gyakorlatban gyakran alkalmazott leíró szabály a Bragg-törvény, amely egyszerű formában: 2d sinθ = nλ (ahol d a kristályrétegek távolsága, θ a beesési szög, λ a röntgensugárhossz, n pedig egy egész szám).
Módszer lépései
- Kristályosítás: A legtöbb röntgenkrisztallográfiai vizsgálat első és gyakran legnehezebb lépése jól rendezett kristály előállítása (kis molekulákhoz és nagy biomakromolekulákhoz más-más körülmények szükségesek).
- Mintaelőkészítés és rögzítés: A kristályt gyakran egy vékony üvegtűre vagy hengerre erősítik, és kryo-hűtőközegbe helyezik, hogy csökkentsék a radiációs károsodást.
- Adatgyűjtés: A röntgensugarakat laboratóriumi csőből vagy nagy intenzitású szinkrotron sugárforrásból bocsátják ki; a kristályt különböző szögekben forgatva detektálják a diffrakciós képeket.
- Indexelés és integráció: A képeken megjelenő csúcsokat azonosítják és intenzitásukat mérik; ez adja az inputot a további számításokhoz.
- Skálázás és korrekciók: Több kép, esetleg több kristály adatainak kombinálása, valamint háttér- és abszorpciókorrekciók elvégzése.
- Fázisprobléma megoldása: A diffrakcióval mért intenzitásokból csak a amplitúdók ismertek; a fázisok hiányoznak, ezért külön módszereket alkalmaznak (lásd alább).
- Térfogati elektron-sűrűség számítása: Fourier-transzformáción alapuló térképek készítése, amelyek alapján egyértelművé válik az atomok helye.
- Modellépítés és finomítás: Az atommodellek illesztése az elektron-sűrűséghez és matematikai finomítása (például R-faktor, R-free minimalizálása).
- Validálás és archiválás: A kész szerkezet ellenőrzése minőségi mutatókkal, majd gyakran adatbázisba (például PDB) való feltöltése.
Fázisprobléma és megoldásai
A diffrakciós kísérletek során csak a csúcsok intenzitását mérjük; a fázisok azonban szükségesek az elektron-sűrűség visszaállításához. Gyakran használt megoldások:
- Molekuláris helyettesítés (molecular replacement, MR): Ha hasonló szerkezet ismeretes, azt használják kiinduló modellként.
- Isomorf helyettesítés (MIR): Nehézfém-behelyezés különböző kristályokba, majd intenzitások összehasonlítása.
- Anomális szórás (SAD/MAD): Szinkrotronon, különböző hullámhosszokon mért anomális szórásból kinyerhetőek a fázisok.
Felbontás és minőség
A szerkezet részletességét a felbontás (Ångström, Å) határozza meg: minél kisebb az Å-érték, annál részletesebb a térkép. Kis szerves molekuláknál gyakori a 0.8–1.5 Å, fehérjéknél jellemzően 1.0–3.5 Å tartomány. A minőséget további mutatók (pl. R-factor, R-free, adat redundanciája) is jellemzik.
Alkalmazások és korlátok
A röntgenkrisztallográfia széles körben alkalmazott:
- Gyógyszertervezés, célfehérjék és ligandok kölcsönhatásainak vizsgálata
- Enzimek és katalízis mechanizmusok feltárása
- Anyagtudomány: kristályos anyagok szerkezetének meghatározása
- Kis- és nagymolekulák szerkezetvizsgálata: szerves és szervetlen vegyületek egyaránt
Korábban említett hátrányok és kihívások:
- Szükség van jó minőségű kristályra: sok biomolekula nehezen kristályosítható.
- Részlegesen rendezetlen vagy flexibilis régiók: Ezek gyenge vagy hiányzó sűrűséget adnak, így nem láthatók jól.
- Radiációs károsodás: Különösen nagy dózisoknál, ezért gyakori a kryo-hűtés és a szinkrotronok gyors adatgyűjtése.
További technológiai fejlődés
A modern fejlesztések közé tartozik a nagyobb intenzitású szinkrotronforrások használata, a röntgengenerátorok és detektorok gyorsuló fejlődése, valamint a mikro- és nanokristályok vizsgálatát lehetővé tevő módszerek. Emellett a számítási módszerek — például automatizált modellezés és mesterséges intelligencia alapú finomítás — jelentősen meggyorsítják és pontosabbá teszik a szerkezetmeghatározást.
Történeti érdekesség
A technikát Sir William Bragg (1862–1942) és fia, Sir Lawrence Bragg (1890–1971) találta fel; ők kapták 1915-ben a fizikai Nobel-díjat. Lawrence Bragg a legfiatalabb Nobel-díjas. Ő volt a Cambridge-i Egyetem Cavendish Laboratóriumának igazgatója, amikor 1953 februárjában James D. Watson, Francis Crick, Maurice Wilkins és Rosalind Franklin felfedezték a DNS szerkezetét. Rosalind Franklin híres diffrakciós felvételei (történetileg „Photo 51”) jelentős szerepet játszottak a kettős hélix felismerésében.
Összefoglalva, a röntgenkrisztallográfia és azon belül a röntgendiffrakció rendkívül hatékony eszköz a molekuláris szerkezet háromdimenziós feltárására, amely nélkülözhetetlen a modern kémia, biokémia és anyagtudomány számára.