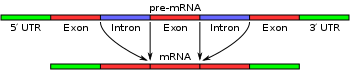
Az RNS-splicing a génátírás egyik szakasza. A hírvivő RNS (mRNS), amely a DNS-ről a kódot a fehérjékre továbbítja, két szakaszban épül fel. Az első szakaszban minden gén pre-mRNS-é alakul. Ezután a pre-mRNS-ekben lévő exonokat splicinggel egyesítik, ami a spliceoszómákban történik.
Erre azért van szükség, mert a gén kódoló szakaszokra, úgynevezett exonokra és nem kódoló szakaszokra, úgynevezett intronokra oszlik. Az exonokat splicinggel hozzák össze.
A molekuláris biológiában tehát a splicing egy olyan folyamat, amelynek során intronokat távolítanak el és exonokat kapcsolnak össze. Így jön létre a végleges mRNS. Ezt a hírvivő RNS-t ezután a megfelelő fehérje előállítására használják fel a transzláció révén.
Mi történik pontosan — a splicing folyamata
A splicinget legtöbbször a sejtek nagy RNP-komplexe, a spliceoszóma végzi. A spliceoszóma fő alkotói kis nukleáris RNS-ekhez (snRNS) kötődő fehérjecsoportok, az snRNP-k (például U1, U2, U4, U5 és U6). A folyamat röviden:
- Pre-mRNS felismerése: a 5' splicing helyet (donor) általában az U1 snRNP ismeri fel, a branch point (ágpont) környékét pedig az U2 snRNP.
- Spliceoszóma összeállása: az U4/U6·U5 tri-snRNP csatlakozik, majd sorozatos szerkezeti átrendeződések következnek, amelyekhez ATP-függő helicázok járulnak hozzá.
- Két transzeszterifikációs reakció: először az ágpont adeninjének 2'-OH csoportja nukleofilként megtámadja a 5' splice hely foszfodiészter kötését, létrehozva az intron "hurok" vagy lariat szerkezetét. Másodszor a felső exon 3'-OH-ja megtámadja a 3' splice helyet, ami az exonok összekapcsolásához és az intron felszabadulásához vezet.
- Intron lebomlása: a kilépett lariat intront enzimek bontják le, alkotórészei újrahasznosulhatnak.
Fontos: az egyes kémiai lépések (a transzeszterifikációk) nem igényelnek ATP-t, de a spliceoszóma összeállítása és átrendeződése ATP-függő folyamatokkal jár.
Alapvető jellemzők — splicing helyek és jelek
- A 5' splice site (donor) és a 3' splice site (acceptor) konzervált rövid bázisszekvenciákkal rendelkezik, amelyek felismerését az snRNP-ek végzik.
- Az ágpont (branch point) körül általában egy konzervált adeninnukleotid található, és gyakran van mellette egy polipirimidin traktus a 3' vég közelében.
Alternatív splicing — hogyan növeli a fehérjék változatosságát
Az alternatív splicing lehetővé teszi, hogy egyetlen génből többféle mRNS-variáns és így különböző fehérje-izoformák keletkezzenek. Gyakori alternatív splicing típusok:
- Exon kiesés (exon skipping)
- Kölcsönösen kizáró exonsorok (mutually exclusive exons)
- Alternatív 5' (donor) splice site
- Alternatív 3' (acceptor) splice site
- Intron retenzió (intron retention)
Ez a rugalmasság létfontosságú a sejttípus-specifikus és fejlesztés során megjelenő fehérjekészletek kialakításához.
Szabályozás — mi határozza meg, hogy melyik splice variáns készül?
A splicing pontos szabályozása különféle fehérjékkel és RNS-elemekkel történik:
- SR-fehérjék (szerin-arginin gazdag): általában serkentik az exonok felismerését és beépülését.
- hnRNP-ek (heterogén nukleáris RNP): sokszor gátolják egyes splice helyek használatát.
- Transzkripciós sebesség, kromatinállapot és mRNS-modifikációk (például metilációk) szintén befolyásolják a splicinget; sok splicing esemény co-transzkripcionálisan, a transzkripcióval párhuzamosan zajlik.
Speciális esetek és kivételek
- Minor spliceoszóma: bizonyos ritkább intronokat a kis (U12-típusú) spliceoszóma dolgoz fel, más snRNS-ekkel (pl. U11, U12, U4atac, U6atac).
- Önsplicing intronok: egyes mikrobákban és mitokondriális RNS-ekben előfordulnak olyan intronok (Group I és II), amelyek önmagukban ribozimként képesek kivágódni; a Group II intronok mechanizmusa hasonlít a spliceoszóma által végzett lariat-képzésre.
Klinikai jelentőség
A hibás splicing számos betegség alapja lehet. Példák:
- Spinalis izomatrófia (SMA): az SMN1/SMN2 gének alternatív splicingja kritikus szerepű.
- Beta-thalassaemia: splice site mutációk vezethetnek funkcióvesztéshez.
- Ráktípusok: spliceoszóma komponenseit érintő mutációk (pl. SF3B1, U2AF1) megváltoztathatják a splicinget és hozzájárulhatnak daganatok kialakulásához.
Hogyan vizsgáljuk a splicinget?
Gyakori módszerek: RT–PCR, Northern blot, RNA-seq (transzkriptomikai vizsgálatok), valamint in vitro splicing-assayek és spliceoszóma-rekonstrukciók biokémiai vizsgálatokhoz.
Összefoglalva: az RNS-splicing alapvető és kifinomult folyamat, amely a pre-mRNS-ből készít működőképes hírvivő RNS-t azáltal, hogy eltávolítja az intronokat és összekapcsolja az exonokat. A splicing szabályozása és variábilitása kulcsfontosságú a sejtbiológiai sokféleség és számos betegség megértése szempontjából.