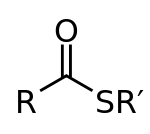
A tioészter olyan molekula, amelynek C-S-CO-C csoportja van. Olyanok, mint az észterek, de oxigén helyett egy kénatomot tartalmaznak. Formálisan a tioészter általános képlete R–C(=O)–S–R′, vagyis egy acilegység (R–C=O) kötődik közvetlenül a kénhez. Az észterekhez hasonlóan karbonsavakból is előállíthatók, de a gyakorlatban gyakran aktivált karbonsav-derivátumokat (például savkloridokat vagy anhidrideket) vagy kondenzációs szereket alkalmaznak, mert a közvetlen kondenzáció a alkohol helyett használt tiol és a karbonsav között nehezebb lehet.
Kémiai tulajdonságok és reaktivitás
A tioészterek jellegzetes tulajdonsága, hogy a kén miatt gyengébb a konjugáció az acil- és a heteroatom között, mint az oxigénes észtereknél. Emiatt a karbonil-szén elektrofílibb, azaz könnyebben támadható nukleofilek által, ezért általában reaktívabbak, mint az észterek és az amidok. Ennek következménye, hogy a tioészterek jó akil- és acilátátvivők, és gyakran szolgálnak acilátátadásra kémiai és biokémiai reakciókban.
A tioészterekre jellemző reakciók közé tartoznak:
- acilátadás (transzacilezés)—szerves szintézisben és enzimek által katalizált folyamatokban;
- Claisen- és aldol-szerű kondenzációk (biokémiai analógokkal, pl. malonil-észterek kondenzációi);
- nukleofil szubsztitúció a karbonilon (hidrolízis vagy aminolízis);\u00a0
- enolizáció és enol- vagy enolátreakciók — az alfa-hidrogének savasabbak, mint sok észter esetében.
Előállítás
Laboratóriumban tioésztereket többféle úton készítenek: aktivált karbonsav-derivátumok (savkloridok, anhidridek) és tiolok reakciójával, vagy karbonsav + tiol párosítását katalizátorral és vízeltávolítással végzik, illetve kondenzációs reagensekkel (például DCC típusú aktiválással). Biokémiai rendszerekben a tioészterkötést általában koenzim A (CoA) vagy acil-kötő fehérjék (pl. ACP) tiolcsoportja hozza létre, és ezek enzimatikus akceptálással/szintézissel jönnek létre.
Szerep a biokémiában
A tioészterek kiemelkedően fontosak a biokémiában. A sejtekben az acilcsoportokat gyakran tioészter formájában (például acil‑CoA‑ként vagy acil‑ACP‑ként) tárolják és továbbítják. Néhány konkrét példa és szerep:
- Acetil‑CoA: központi metabolit, amely acilátadóként részt vesz a citrátkörben, zsírsav‑szintézisben és sok bioszintetikus folyamatban;
- Zsírsav‑szintézis és β‑oxidáció: az acil‑szénláncok aktiválása és szállítása tioészter formában történik (acil‑CoA, acil‑ACP);
- Poliketid és nemriboszomális peptid bioszintézis: a tioészterköztesek fontosak a lánchosszabbító kondenzációk során;
- Subsztrát-szintű foszforiláció: például a szukcinil‑CoA → szukcinát átalakulás során a szukcinil‑CoA tioésztere közvetlenül hozzájárulhat GTP/ATP képződéséhez (szubsztrát‑szintű foszforiláció);
- Adenozin‑triphosphát (ATP) kapcsolódása: bár a tioészterek maguk nem „termelik” közvetlenül az ATP-t minden esetben, az acil‑CoA‑k és a tioészterköztesek központi szerepet játszanak az anyagcsere útvonalakban, amelyek végső soron az energiatermeléshez (ATP‑hoz) vezetnek.
Biokémiai enzimek és szabályozás
Számos enzim képes tioészterképzésre és -bomlásra: acil‑CoA‑szintetázok, aciltranszferázok, tioészterázok és mások. A tioészterköztesek redox‑független módon gyors acilátviteleket tesznek lehetővé, ami hatékony mechanizmust ad a metabolikus útvonalak szabályozásához és energiaátviteléhez.
Alkalmazások és példák a szintetikus kémiában
A tioésztereket a szerves kémiai szintézisben is széles körben használják acilátadóként, poláris reakciók kiindulóanyagaként és átvezető egységként komplex molekulák előállításához. Speciális reakciókban (pl. Fukuyama‑coupling vagy különféle acilációs eljárások) a tioészterek előnyösek lehetnek reaktivitásuk és kényelmes előállíthatóságuk miatt.
Összefoglalva, a tioészterek strukturálisan az észterek kénváltozatai, kémiailag reaktívabbak, és biokémiai: acilátvitelben, metabolizmusban és bioszintézisben kulcsfontosságú köztesek. A pontos laboratóriumi vagy enzimatikus előállítási módok és a reakcióban betöltött szerep mindig az adott rendszer és célfüggő.