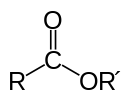
Az észter egy karbonilcsoportot (C=O) tartalmazó szerves vegyület, amelynél a karbonil-szénhez egy alkoxi (–OR) csoport kapcsolódik. A szerkezetet gyakran rövidítve COOR formában írjuk. Általános képlete R–COOR′, ahol R és R′ alkil vagy aromás csoport lehet. Karbonsav és alkohol reakciójával, általában savkatalízissel (például amin vagy ásványi sav jelenlétében) jön létre az észteresítés; ezt a reakciót gyakran egyszerűen a savval történő reakció megfogalmazással is említjük.
Szerkezet és elektronikus jellemzők
Az észter karbonil-szénje sp2 hibridizált, a C=O kötés és a hozzátartozó alkoxi-oxigén között delokalizáció (rezonancia) figyelhető meg, ami befolyásolja a kötés polaritását és a reakciókészséget. Az alkoxi rész (–OR) könnyen cserélhető nukleofil reakciók során (transzeszterifikáció), ezért az észterek ilyen típusú reakciókban viszonylag rugalmasak.
Előállítási módszerek
- Fischer-észterezés: Karbonsav + alkohol savkatalizátor mellett, víz eltávolításával (egyszerű, gyakran alkalmazott módszer).
- Aktivált származékok (sav-klorid, anhidrid): sav-klorid vagy savanhidrid + alkohol gyors és hatékony észterezést ad.
- Transzeszterifikáció: egy észter alkoholcseréje másik alkohollal (gyakori gyakorlatolajok, biodízel gyártásánál).
- Steglich-észterezés és kondenzációs módszerek: karbonsavak aktiválása vegyületekkel (például DCC/DMAP) finom szerves szintézisekben hasznos.
- Enzimatikus módszerek: lipázokkal végzett katalízis (pl. élelmiszeripari vagy zöld kémiai alkalmazások).
Fizikai tulajdonságok
- Az észterek általában polárisabbak, mint a szénhidrogének, de kevésbé képesek hidrogénkötést adni, mint a karbonsavak; emiatt forráspontjuk a hozzájuk hasonló moláris tömegű karbonsavaknál alacsonyabb.
- Kis molekulatömegű észterek (például metil- vagy etil-észterek) vízben részben vagy jól oldódnak; a nagyobb láncú észterek apolárisabbak és zsíroldó tulajdonságúak.
- Sok észternek jellegzetes, gyakran kellemes illata van, ezért fontosak az aroma- és parfümök előállításában.
- Az észtercsoportban található poliészterek (poliészterek a) nagy ipari jelentőségű műanyagok (pl. PET).
Kémiai reakciók és reaktivitás
Az észterekre jellemző, hogy a karbonil-szén nukleofil addícióval és nukleofil akilelvonással reagálhat:
- Hidrolízis: savas körülmények között megfordítható (észteresítés fordítottja), bázisos körülmények között viszont gyakran irreverzibilis szoaponifikáció történik (só és alkohol keletkezik).
- Transzeszterifikáció: az alkoxi rész kicserélhető más alkohollal; fontos például a biodízel előállításánál (zsírsav-metilészterek).
- Redukció: erős redukáló szerekkel, például LiAlH4-gyel az észtereket két alkoholra lehet redukálni; a gyengébb redukálószerek (pl. NaBH4) általában nem hatékonyak redukálni az észtert.
- Átalakulás ketonokká, alkoholokká: bizonyos körülmények között lehetséges az észterek átalakítása ketonra vagy alkoholra történő átalakítással (pl. Claisen-átalakítások, redukciók).
- Amidképzés: az észterekből megfelelő aktiválás után karbonsavszármazékokhoz hasonlóan amidot lehet előállítani.
- C-alkilek kondenzációja: a klaisen- és egyéb kondenzációs reakciók fontos szerepet játszanak szén–szén kötés kialakításában.
Azonosítás spektroszkópiával
Számos analitikai módszer alkalmas az észtercsoport felismerésére:
- Infravörös spektroszkópia: az észterekre jellemző a C=O szigetelt absorpciója általában ~1735–1750 cm⁻¹ körül (konjugáció vagy ringi hatások ezt le vagy fel tolhatják). Emellett erős C–O nyúlási sávok is megjelennek ~1050–1300 cm⁻¹ tartományban.
- Szén-NMR (13C): a karbonil-szén eltolódása tipikusan ~160–185 ppm között található, ami segít megkülönböztetni az észtereket más karbonilvegyületektől.
- 1H NMR: az alkoxi oldalon lévő protonok (R′–O–CH2, R′–O–CH3 stb.) jellegzetes kémiai eltolódással jelennek meg, és a karbonilhoz közeli alfa-protonok is desztilódhatnak.
- MS (tömegspektrometria): tipikus fragmmentációk (például alkoxi cationok) segítik azonosítani a lánchosszakat és az alkoxi részt.
Gyakorlati alkalmazások és előfordulás
Az észterek mindennapi életben és iparban számos helyen előfordulnak: fontos alkotórészei a zsíroknak és olajoknak (trigliceridek), oldószerként (pl. etil-acetát), illat- és aromaanyagként (parfümök, élelmiszer- aroma), továbbá polimerizációval létrehozott poliészterek a textil- és csomagolóipar alapanyagai. Biodízelként a zsírsav-metilészterek hasznos tüzelőanyagok.
Összefoglalva: az észterek sokoldalú, könnyen átalakuló funkciós csoportok, amelyek kémiai viselkedésük, fizikai tulajdonságaik és kellemes illatuk miatt jelentősek mind a természetben, mind az iparban.