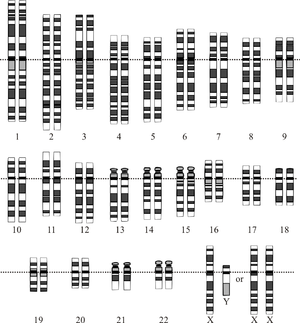
Az emberi genom 23 kromoszómapáron tárolódik a sejtmagban és a kis mitokondriális DNS-ben. Ma már nagyon sokat tudunk a kromoszómáinkon található DNS-szekvenciákról. Azt, hogy a DNS valójában mit csinál, már részben tudjuk. Ennek a tudásnak a gyakorlati alkalmazása még csak most kezdődik.
A Humán Genom Projekt (HGP) olyan referenciaszekvenciát hozott létre, amelyet világszerte használnak a biológiában és az orvostudományban. A Nature közölte a közpénzekből finanszírozott projekt jelentését, a Science pedig a Celera tanulmányát. Ezek a cikkek leírták, hogyan készült a szekvencia tervezete, és elemzést adtak a szekvenciáról. 2003-ban és 2005-ben továbbfejlesztett tervezeteket jelentettek be, amelyek a szekvencia ≈92%-át kitöltötték.
A legújabb ENCODE projekt a gének irányításának módját vizsgálja.
Szerkezet és alapvető jellemzők
Az emberi genom haploid (egyes példány) mérete körülbelül 3,1–3,2 milliárd bázispár. Diploid sejtekben — amelyekben minden kromoszóma párban van — ennek nagyjából a duplája található meg. A teljes nukleáris genom mindössze ≈1–2%-át teszi ki a protein-kódoló exonok összessége; a többi rész nagyrészt intronokból, szabályozó elemekből, ismétlődő szekvenciákból és egyéb nem-kódoló régiókból áll.
- Gének száma: a jelenlegi becslések szerint körülbelül 19–21 ezer fehérjét kódoló gént ismerünk; ehhez jönnek még a sok ezer nem-kódoló RNS-t kódoló egységek.
- Ismétlődő elemek: az emberi genom majdnem fele ismétlődő szekvenciából áll (LINE-ek, SINE-ek — például Alu —, LTR elemek, műsorszóró (satellite) DNS). Ezek nehezítik a teljes összeállítást és a funkciók értelmezését.
- Telomerek és centromerek: a kromoszóma-végeken található telomer-szakaszok (humánban a ismétlődő motívum a TTAGGG) és a centromerek speciális, ismétlődő szerkezetű régiók, amelyek kulcsfontosságúak a kromoszómaszegregációban.
- Alternatív splicing: egy gén többféle mRNS-t és így többféle fehérjét is eredményezhet, ez nagy mértékben növeli a proteom változatosságát.
Mitokondriális DNS
A mitokondriális DNS-ben található genom kicsi, körkörös molekula (emberben ≈16 569 bp), és tipikusan maternálisan öröklődik. A mitokondriális genom körülbelül 37 gént tartalmaz: 13 fehérje-kódoló gént (elsősorban a légzési lánc komponenseihez), 22 tRNS-t és 2 rRNS-t. Több példány is lehet belőle egyetlen sejtben, és mutációi különböző öröklődő vagy szövet-specifikus betegségekhez vezethetnek.
A Humán Genom Projekt és utókövetkezményei
A HGP (1990 környékén indult) célja egy jó minőségű, nyilvános humán referencia-szekvencia összeállítása volt. Az első „munkavázlat” publikálása 2001-ben nagy nemzetközi és tudományos visszhangot kapott (Nature, Science és a Celera tanulmányai). 2003–2005 körül a referencia egyre pontosabbá vált (a szekvencia nagy részét lefedve), de az ismétlődő, heterokromatin- és centromer-területek miatt még maradtak hiányok.
Az elmúlt évtizedben újabb összerakó és szekvenálási technológiák (hosszú olvasatú rendszerek, optikai térképezés, Hi-C és más módszerek) lehetővé tették a korábban kitakart régiók feltárását. A Telomere-to-Telomere (T2T) konszorcjum 2021–2022 folyamán jelentős előrelépést tett a gap-mentes összeállítások felé (például a CHM13 teljes, telomér–telomérhez illesztett emberi genom projekt), és napjainkban egyre nagyobb hangsúlyt kap a pangenom megközelítés, amely sokféle egyén genomját egyaránt figyelembe veszi, hogy a referencia reprezentatívabb legyen a földrajzi és népességbeli variabilitásra.
ENCODE és a funkcionális genomika
A ENCODE projekt célja a genom funkcionális elemeinek feltérképezése: mely régiók aktívak transzkripcióban, hol találhatók promóterek, enhancer-ek, szigetelések és egyéb szabályozó elemek, továbbá hogyan változik a kromatin állapota különböző sejttípusokban. Az ENCODE eredményei megmutatták, hogy a genom sokkal „élettelibb”, mint azt korábban gondoltuk: nagyszámú nem-kódoló RNS, széleskörű transzkripció és számos szabályozó interakció fedezhető fel, bár az, hogy minden biokémiai aktivitás valódi biológiai funkciót jelent-e, még vita tárgya.
Technológiák és módszerek
- Szintén fontos technológiák: Sanger-szekvenálás (korai időkben), rövid olvasatú NGS rendszerek (pl. Illumina), hosszú olvasatú rendszerek (PacBio, Oxford Nanopore), kromatin-konformációs módszerek (Hi-C), és optikai térképezés — mindegyik hozzájárult a genom pontosabb összeállításához és az összetett régiók feltárásához.
- Analitikai módszerek: populációgenetikai elemzések, GWAS (genome-wide association studies), funkcionális annotációk, gépi tanulás a variánsok hatásának előrejelzésére.
Orvosi alkalmazások és etikai kérdések
A genomikai ismeretek gyakorlati haszna egyre növekszik: ritka betegség-diagnosztika (exom- és genom-szekvenálás), onkológia (tumorsekvenálás a célzott terápiákhoz), farmakogenomika (gyógyszerválasz előrejelzése), valamint prediktív és preventív medicina. Ugyanakkor fontos etikai, jogi és társadalmi kérdések is felmerülnek: adatvédelem, genetikai diszkrimináció elleni védelem, informált beleegyezés, és a populációk közötti egyenlő hozzáférés biztosítása a hasznosítás során.
Záró megjegyzések
Az emberi genom feltérképezése egy mérföldkő volt a biológia és az orvostudomány történetében, de a genom működésének megértése folyamatos folyamat. A referencia-szekvenciák, az ENCODE és a pangenom-projektek, valamint az egyre fejlettebb szekvenálási módszerek együttesen teszik lehetővé, hogy egyre pontosabban megfejtsük, hogyan szabályozódnak a gének, hogyan járulnak hozzá a genomvariánsok a betegségekhez, és hogyan lehet ezeket az ismereteket felelősen alkalmazni a gyógyításban és a közegészségügyben.