Az irányított evolúció (DE) egy kísérleti módszer, amelyet ipari és orvosi célú enzimek és egyéb biomolekulák fejlesztésére alkalmaznak. A cél olyan variánsok előállítása, amelyek jobb katalitikus hatékonysággal, stabilitással vagy új funkcióval rendelkeznek az eredeti természetes változathoz képest.
A módszer a fehérjemérnökség eszköztárába tartozik, és laboratóriumi körülmények között a természetes szelekciót utánozza: ismételt mutációs és szelekciós (vagy szűrési) körökkel javítja a kívánt tulajdonságokat.
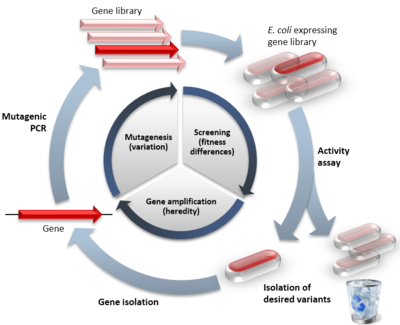
Az alapötlet az, hogy egy gént ismételt mutációs köröknek vetnek alá, és így egy nagy variánskönyvtár jön létre. A megfelelő szelekció vagy szűrés izolálja a kívánt funkcióval rendelkező variánsokat. Ezek képezik a következő forduló sabllonját.
Az irányított evolúciót lehet végezni in vivo — élő baktérium- vagy élesztősejtekben — illetve in vitro — sejtek nélküli, cellafree rendszerekben vagy mikrocseppekben. Az in vivo megközelítésnél a variánsokkal töltött plazmiddal transzformálnak sejtek ezreit vagy millióit, úgy, hogy a sejtek között csak a kívánt gén különbözik, míg az összes többi genetikai háttér azonos marad.
A sejtek a fehérjét vagy a citoplazmájukban vagy a felszínükön expresszálják, ahol a fehérje működése vizsgálható. Ennek az az előnye, hogy a kiválasztás a valós sejtkörnyezetben történik, ami különösen fontos, ha a fejlesztett fehérjét vagy RNS-t élő szervezetekben kívánják használni.
A sejtek nélkül végzett DE in vitro transzkripciós transzlációval állít elő fehérjéket vagy RNS-t oldatban vagy mesterséges mikrocseppekben. Ennek előnye, hogy a környezet (például hőmérséklet, oldószerek) és a kísérleti feltételek szélesebb skálája tesztelhető, továbbá olyan fehérjéket is kifejezhetnek, amelyek a sejtek számára mérgezők lennének. Továbbá az in vitro evolúciós kísérletek sokkal nagyobb (akár 1015) könyvtárakat is létrehozhatnak, mivel a könyvtár DNS-ét nem kell a sejtekbe beilleszteni. Ez gyakran korlátozza az in vivo megközelítéseket.
Módszerek (mutáció és variánskészítés)
- Erroneous PCR (hibás PCR): magas hibaarányú PCR-rel véletlenszerű pontmutációkat vezetnek be a génbe.
- Site-saturation és célzott mutagenezis: egy vagy több aminosavat célzottan telítenek variábilis nukleotidokkal, ha ismert pozíciók fontosak a funkcióért.
- DNA shuffling (rekombináció): kompatibilis szülői gének darabjait rekombinálva hoznak létre új kombinációkat.
- Mutátor törzsek: olyan mikroorganizmusokat használnak, amelyekben a DNS-javító mechanizmusok gyengébbek, így gyorsabb mutációs ráta érhető el.
- Komputációs tervezés és kombinált megközelítések: in silico predikciókkal célzott változtatásokat alkalmaznak, majd ezekből könyvtárakat hoznak létre.
Szelekciós és szűrési stratégiák
Az irányított evolúció két alapvető megközelítése a szelekció és a szűrés. A szelekció automatikusan elszaporítja azokat a variánsokat, amelyek egy adott feltételnek megfelelnek (például túlélés antibiotikum jelenlétében, vagy katalízis következtében keletkező jel), míg a szűrés minden egyes variánst egyenként tesztel, például mikrotiterlemezes assay-ekkel vagy áramlási citometriával (FACS).
Speciális platformok és technikák:
- Fág-displaylist, riboszóma- és mRNS-displaylist — a kötő- vagy katalitikus képességet közvetlenül a DNS/RNS és a termék kapcsolatára fordítják.
- Sejtfelszíni display — fehérjék a sejtfelszínen jelennek meg, így könnyen válogathatók.
- Mikrocseppes mikrofluidika — egyedi reakciók ultranagy számú párhuzamos vizsgálatát teszi lehetővé, kifejezetten nagy könyvtárak kezelésére.
- Kompartimentalizált önreplikáció (CSR) — olyan rendszerek, ahol a katalitikus aktivitás a saját genetikai anyag szaporodását segíti elő.
Alkalmazások
- Ipari enzimek: magasabb hőstabilitás, szerves oldószerekkel való kompatibilitás, jobb szubsztrátspecificitás (pl. mosószeripar, élelmiszeripar, vegyipar).
- Gyógyszerfejlesztés: biokatalizátorok és terapeutikus fehérjék optimalizálása, antitest fragments javítása.
- Diagnosztika és bioszenzorok: érzékenység és szelektivitás növelése.
- Környezeti alkalmazások: szennyezők lebontását segítő enzimek fejlesztése.
- Alapkutatás: fehérje-mechanizmusok feltárása és új biokémiai aktivitások felfedezése.
Előnyök és korlátok
Előnyök: nincs szükség teljesen előre meghatározott tervezésre — természetes evolúciós elveket használva gyakran olyan megoldások születnek, amelyeket tervezéssel nem könnyű előre látni. Az in vitro rendszerek nagy könyvtárméreteket és veszélyes/toxikus fehérjék vizsgálatát is lehetővé teszik.
Korlátok: a megfelelő szelekciós rendszer kialakítása gyakran nehéz és időigényes; egyes tulajdonságok több gén vagy komplex sejtkörnyezet függvényei, ami megnehezíti a közvetlen szelekciót. Az in vivo módszereknél a DNS beillesztése, az expresszió és a sejtti toxicitás korlátozó tényezők lehetnek.
Példák és eredmények
Számos sikeres példa bizonyítja a DE erejét: enzimaktivítások jelentős növelése, új katalitikus aktivitások megjelenése, illetve olyan változatok létrehozása, amelyek extrém hőmérsékleten vagy szerves oldószerekben is funkcionálnak. A módszert Nobel-díjjal is elismerték a fehérjék fejlesztésében elért áttörések miatt.
Etika és biztonság
Az irányított evolúció laboratóriumi alkalmazása során fontos a biológiai biztonság és a felelős kutatás betartása: a létrehozott variánsok potenciális kockázatainak értékelése, megfelelő biokontroll és engedélyezési eljárások betartása elengedhetetlen.
Összefoglalás
Az irányított evolúció rugalmas és hatékony eszköz a fehérjemérnökségben: kombinálva a mutációs módszereket, nagy könyvtárakat és jól megtervezett szelekciós stratégiákat, lehetővé teszi új vagy jobb funkciójú biológiai molekulák gyors kifejlesztését. A módszer fejlődése — különösen a mikrofluidikai és cellafree technológiák terén — tovább növeli alkalmazhatóságát és a vizsgálható könyvtárak méretét.