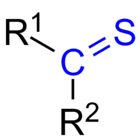
A tioketon (vagy tiion) bármely molekula, amelynek R csoportja2 C=S. Olyan, mint egy keton, amelynek oxigénatomját kénatomra cserélték: a kénatom kettős kötést alkot a szénatomhoz, és két magányos párt is megtart. A tioketontól származó analóg, amikor az egyik R csoport hidrogén, az az aldehid kénes változata, amelyet thialnak neveznek; ezek általában még a tioketonoknál is nagyobb reakciókészséget mutatnak.
Szerkezet és fizikai tulajdonságok
A C=S kötés elektronikailag és geometriailag hasonlít a C=O kötéshez, de fontos különbségek vannak: a kén elektronegativitása kisebb, ám polárizálhatósága nagyobb, ezért a C=S pályák energiája és a HOMO–LUMO rés között eltérő. Ennek következménye, hogy sok tioketon intenzív színt ad (például piros vagy vörös árnyalatok), és a molekulák gyakran erőteljes elektronikus abszorpciót mutatnak.
Kémiai reaktivitás
A tioketonok általában nagyon reaktív vegyületek: jó elektrofilek, így könnyen reagálnak nukleofilekkel (pl. aminokkal, tiolokkal), és hajlamosak addíciós reakciókra. Sok tioketon instabil, hajlamos polimerizálódni vagy oligomerizálódni, illetve Gyűrűket kialakítani. Gyakori reakciók:
- Cikloaddíciók: a tioketonok jó cikloaddíciós partnerek — például hasonlóan a Diels-Alder reakcióhoz alkalmazhatók dienofilekként dienekkel való reakciókban, új heterociklusok képzésére.
- Adíció nukleofilekkel: aminok, alkoholok vagy tiolok addíciója hemithioketalokhoz vagy dithioacetalokhoz vezethet (a tioketalak fontos védelmi egységek lehetnek kénvegyületek előállításában).
- Redox- és átalakító reakciók: thionálással előállított tioketonok könnyen visszaalakulhatnak ketonná oxidálással, illetve különböző redukciókkal átalakíthatók.
Előállítás
A legegyszerűbb és leggyakrabban alkalmazott módszer a ketonok oksigénének kénre cserélése, az ún. thionálás. Tipikus reagensek:
- P4S10 (foszfor-pentaszulfid) — általános thionálószer, sok keton és aldehid átalakítására alkalmas.
- Lawesson-reagens — kíméletesebb, széles körben használt thionálószer szerves szintézisben.
Egyes speciális tioketonokat aromás konjugáció vagy nagy sterikus gátlás segítségével is elő lehet állítani, mert ezek a faktorok növelik a termék stabilitását.
Stabilitás és befolyásoló tényezők
Sok tioketon instabil vagy nagyon reaktív; a stabilitást befolyásolják:
- Elektronikus tényezők: konjugáció (pl. aromás gyűrűkkel) csökkentheti a reaktivitást és stabilizálhatja a tioketont.
- Sterikus védelem: nagy, térkitöltő R-csoportok megakadályozzák a dimerizációt vagy cikloaddíciókat, és így stabilabbá teszik a molekulát (például a thiobenzophenone — diphenylthioketone — ismert, viszonylag stabil példa).
Spektroszkópia és azonosítás
A tioketonok azonosítása spektroszkópiai módszerekkel történik: infravörös (IR) spektrometriában a C=S kötés jellegzetes rezgéseket ad, amelyek általában alacsonyabb energián jelennek meg a C=O-hoz képest; elektronikus (UV–Vis) spektroszkópiában sok tioketon erős látható vagy UV abszorpciót mutat. NMR-ben a tiokarbonil-szén jele magasabb tértértékekkel jelenhet meg, és a környező protonok kémiai eltolódása is jellegzetes lehet.
Példák és alkalmazások
Példák közé tartoznak a kis alkil- és aril-tioketonok, valamint a különleges, stabilizált típusok, mint a thiobenzophenone. Alkalmazási területek:
- szerves szintézis: tioketonok hasznos intermediátok heterociklusok és kénmentes vegyületek előállításában,
- cikloaddíciós reakciók és fotokémiai átalakulások vizsgálata,
- védőcsoportokként dithioacetalok képzése kén-kémiai transzformációkhoz.
Összefoglalás
A tioketonok a ketonok kénanalógjai, jellemzően nagyobb reaktivitást és különleges elektronikus tulajdonságokat mutatnak a C=S kötés miatt. Sok képviselőjük instabil, hajlamos cikloaddíciókhoz és addíciós reakciókhoz, ugyanakkor megfelelő szubsztituensekkel és előkészítéssel stabil, jól használható vegyületek is előállíthatók. A thialok (thialnak nevezett kénes aldehidek) különösen reakcióképesek és ritkán izoláltak alapesetben.