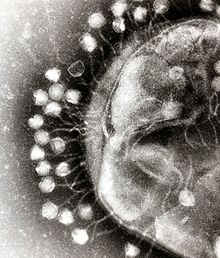
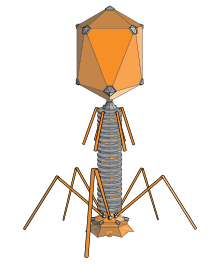
A bakteriofág olyan vírus, amely baktériumokat fertőz. A kifejezést általában fágra rövidítik. A fágok rendkívül változatosak: vannak egyszerű, kapszidszerű részecskék és összetett, farokkal rendelkező formák is. A fágok szinte mindig kizárólagos gazdaspecifikussággal rendelkeznek, azaz gyakran csak egy vagy néhány baktériumtörzset képesek megfertőzni.
Szerkezet és genom
A bakteriofágok a bioszféra leggyakoribb és legváltozatosabb egyedei közé tartoznak. Az eukariótákat (növények, állatok és gombák) megfertőző vírusokhoz hasonlóan a fágok szerkezete és funkciói is sokfélék. Sok baktériumfág külső vázát fehérjeszerkezetek alkotják, egyes nagyobb fágoknak fej–nyak–farok felépítésük van, mások egyszerű kapsziddal rendelkeznek.
A fágok jellemzően egy külső fehérjehéjból állnak, amelynek belsejében genetikai anyag található. A genetikai anyag lehet egyszálú (ssRNS vagy ssDNS) vagy kétszálú (dsRNS vagy dsDNS). Hossza 5 és 500 kilobázispár között lehet, körkörös vagy lineáris elrendezésben. A bakteriofágok mérete általában 20 és 200 nanométer között van.
A fág genomok akár négy gént is kódolhatnak, de akár több száz gént is. A genomokból kódolt fehérjék közé tartoznak a kapszidalkotó fehérjék, farokfehérjék, replikációs enzimek és a gazdasejt falát lebontó enzimek (pl. endolizin). A fágok befecskendezik genomjukat a baktériumba, és a baktériumban szaporodnak.
Életciklusok és kölcsönhatások a baktériumokkal
A fágok életciklusa jellemzően lítikus vagy lizogén útvonalon zajlik. A lítikus ciklusban a fág replikálódik, majd a gazdasejtet felrobbantva (lizálva) új virionokat szabadít fel. A lizogén ciklusban a fág genomja beépül a baktérium kromoszómájába (profágként), és osztódáskor együtt öröklődik; később különböző környezeti jelre aktiválódhat és lítikussá válhat. Sok baktérium védekezik fágok ellen CRISPR rendszerekkel és egyéb abortusz mechanizmusokkal, miközben a fágok ellenfelek evolúciós nyomást gyakorolnak a baktériumok adaptációjára.
A fágok specifikussága és a gazdaspektrum szűkössége miatt a gazdag fajdiverzitás lehetővé teszi, hogy egy ökoszisztémán belül sok különböző fág–gazda páros létezzen párhuzamosan. Ugyanakkor a fágok hozzájárulnak a horizontális géntranszferhez (transzdukció), ami a baktériumok evolúciójában és a antibiotikumoknak ellenálló tulajdonságok terjedésében is szerepet játszhat.
Ökológiai szerep
A fágok mindenütt jelen vannak, ahol baktériumok vannak, például a talajban vagy az állatok beleiben. Nagyon gyakoriak a tengervízben: a felszíni mikrobiális szőnyegekben milliliterenként akár 9×108 viriont is találtak, és a tengeri baktériumok akár 70%-a is fágokkal fertőzött lehet. A fágok kulcsszereplők a mikrobiális ökoszisztémákban: befolyásolják a baktériumpopulációk dinamikáját, hozzájárulnak az organikus anyagok lebontásához és az ún. "vírális shunt" révén szabályozzák a tápanyagáramlást az óceánokban.
A fágok emellett szerepet játszanak a mikrobiomok szabályozásában — például az emberi, állati vagy növényi bélflora egyensúlyában — és befolyásolhatják a patogén baktériumok elterjedését vagy visszaszorítását. Egyes fágok fág-encoded toxinokat vagy más virulencia-faktorokat hordozhatnak, így hozzájárulhatnak gazdáik patogenitásához.
Fágok és biofilmek
Számos baktérium antibiotikumoknak ellenálló törzse ellen lehetséges terápiát jelentenek. Másrészt egyes fágok megnehezítik a tüdőgyulladásban és a cisztás fibrózisban szerepet játszó biofilmeket. Megvédik a baktériumokat a gyógyszerektől, és így meghosszabbítják a fertőzést. Ugyanakkor sok fág, vagy fágból származó enzim (pl. depolimerázok, endolizinok) képes elbontani a biofilm mátrixot, megkönnyítve a baktériumok elpusztítását és az antibiotikumok hozzáférését. A fág–biofilm kölcsönhatás ezért komplex: egyes fágok hozzájárulhatnak a biofilm stabilizálásához (pl. lizogén integrációval vagy biofilm-alkotó génátvitellel), míg mások biofilm-rongáló hatásúak lehetnek.
Terápiás szerep és alkalmazások
Több mint 90 éve használják az antibiotikumok alternatívájaként a volt Szovjetunióban és Közép-Európában, valamint Franciaországban. A fágok valódi természetét azonban csak akkor állapították meg, amikor Helmut Ruska 1939-ben elektronmikroszkóp alatt megfigyelte az első fágot. A fágterápia története korábbra nyúlik vissza: Félix d'Hérelle és mások a 20. század elején már alkalmaztak fágakat fertőzések kezelésére.
A fágterápia előnyei közé tartozik a célzott hatás (kisebb mellékhatás a normál mikrobiomra), a saját szaporodás a fertőzés helyén és az a lehetőség, hogy kombinációs (koktél) kezelésekkel a rezisztencia kialakulását csökkentsék. Jelenleg több módszert vizsgálnak: természetes fágkoktélok, genetikai módszerekkel módosított fágak (pl. szűkebb specifitás, jobb baktericid hatás), valamint fág-eredetű enzimek (endolizinok) alkalmazása.
Fontos történelmi és intézményi helyszín az Eliava Intézet Grúziában, ahol a fágterápiát folyamatosan fejlesztették; a hidegháború idején és azt követően Kelet-Európában szélesebb körben alkalmazták, mint a nyugaton. Az utóbbi években az antimikrobiális rezisztencia növekedése miatt a fágterápia iránti érdeklődés világszerte megnőtt: vannak klinikai kísérletek és esetsorozatok, valamint néhány engedélyezett alkalmazás és egyre több engedélyezési vita a szabályozásról.
Előnyök, kihívások és biztonság
- Előnyök: magas specifitás (kis hatás a hasznos baktériumokra), lehetőség rezisztens törzsek célzására, önszaporodás a fertőzési gócban, fág-enzimek alkalmazhatósága.
- Kihívások: keskeny gazdaspektrum miatt pontos izolátum-azonosítás szükséges; a baktériumok kialakíthatnak fág-rezisztenciát; potenciális transzdukciós génátadás (antibiotikum-rezisztencia vagy toksinátvitel) lizogén fágok esetén; immunszervrendszeri semlegesítés; gyártási, tisztítási és szabályozási nehézségek.
- Biztonság: a lítikus fágok általában biztonságosabbnak tekinthetők terápiás célra, mint a lizogén fágok, mert kevésbé valószínű, hogy horizontális géntranszfert közvetítenek. A terápiás készítményeket endotoxin-mentesítéssel és alapos tisztítással kell előállítani, és klinikai vizsgálatok szükségesek a hatékonyság és a biztonság igazolására.
Alkalmazások a gyógyászaton és iparban
A fágokat vizsgálják és alkalmazzák:
- a bakteriális fertőzések kezelése (helyi és szisztémás alkalmazás, például sebek, égési sérülések, légúti és húgyúti fertőzések esetén);
- élelmiszer-biztonság: fágkészítményekkel csökkentik bizonyos patogének (pl. Salmonella, Listeria) előfordulását;
- diagnosztika: fágakat lehet használni baktériumok gyors kimutatására;
- mikrobiológiai kutatás és biotechnológia: fágdisplay rendszerek fehérje- és antitestkutatásra, valamint génszállítási módszerek fejlesztése;
- fág-enzimek (endolizinok, depolimerázok) mint új antibakteriális hatóanyagok.
Jövőbeli irányok
A kutatás jelenleg a következő területekre fókuszál: fágkoktélok optimalizálása, fágak genetikai módosítása hatékonyság és biztonság növelésére, kombinált kezelések antibiotikumokkal vagy immunkomodulánsokkal, valamint a gyártási és szabályozási keretek kidolgozása. Emellett alapkutatások folynak a fág–gazda kölcsönhatások, a CRISPR és egyéb védekező rendszerek, valamint a fágok ökológiai szerepének mélyebb megértésére.
Összefoglalva: a bakteriofágok sokszínű, ökológiailag és orvosilag is jelentős csoportot alkotnak. Előnyeik és lehetőségeik mellett fontos a kockázatok, az ellenállás kialakulásának és a génátvitelnek a kezelése; a jövőben interdiszciplináris kutatás és nemzetközi szabályozás segítheti a fág-alapú terápiák biztonságos és hatékony alkalmazását.