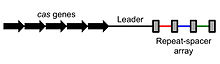
A CRISPR a mikrobiológiában használt kifejezés: a Clustered Regularly Interspaced Short Palindromic Repeats rövidítése. Ezek rövid palindromikus ismétlődések és közéjük ékelt ún. spacer-szekvenciák egyaránt — a DNS egy természetes részei, amelyeket főleg a prokariótákban (tehát sok baktériumban és archaea) találtak meg. A CRISPR-szekvenciák mellett gyakran vannak jelen a cas (CRISPR-associated) gének is, amelyek a rendszer működéséhez szükséges fehérjéket kódolják.
Miért fontosak a CRISPR-ek?
A CRISPR-ek a prokarióták adaptív immunrendszerének részét képezik: a baktériumok és archaeák ezek segítségével „emlékeznek” a korábban megtámadó vírusokra (például bakteriofágokra) és képesek célzottan megtámadni az idegen genetikai anyagot. Amikor egy vírus megtámad egy sejtet, a prokarióta egyes vírus-DNS darabokat beépít spacer-ként a CRISPR-kelyhek közé; később ez a spacer információként szolgál a felismeréshez.
Hogyan működik a CRISPR-Cas rendszer?
- Adaptáció (spacer-acquisition): a rendszer beépít rövid DNS-morzsákat a CRISPR-láncba, amelyek később felismerik ugyanazt a vírust.
- Expresszió és feldolgozás: a CRISPR-láncról először pre-crRNA készül, amelyet feldolgoznak és rövid crRNA-kra vágnak; a crRNA-k a Cas-fehérjékkel együtt működnek.
- Interferencia: a crRNA irányítja a Cas-fehérjét (például a legismertebb Cas9-ot) olyan cél-DNS-hez, amely komplementer a spacerhez, és amely mellett a megfelelő protospacer adjacent motif (PAM) is jelen van. A Cas-fehérje ezután hasítja a cél-DNS-t.
A génszerkesztésben a természetes rendszert úgy használják, hogy a crRNA és tracrRNA szerepét egyetlen vezető (guide) RNS-re (gRNA) egyszerűsítik, mely a kívánt helyre vezeti a Cas-fehérjét.
Hogyan alkalmazzák genomszerkesztésre?
A CRISPR-Cas rendszert mesterségesen úgy alkalmazzák, hogy egy célzott gRNA és egy Cas-nukleáz (pl. Cas9) együtt beviszik a sejtekbe. Amikor a Cas9 kettős szálú törést (double-strand break, DSB) hoz létre a célpontnál, a sejtek saját javítófolyamatai reagálnak:
- NHEJ (nem homogén végű összekapcsolás): gyors, hibajavító mechanizmus, ami gyakran törléseket vagy behelyezéseket (indel) okoz — ezáltal kikapcsolható a gén.
- HDR (homológ rekombináció): pontosabb javítás, amely külső mintát (donor DNS) használva célzott módosításokat tesz lehetővé; viszont csak bizonyos sejttípusokban és fázisokban hatékony.
A CRISPR-technológiából számos változat alakult ki: nickase fehérjék (egyszálú hasítás), katalitikusan inaktív dCas9 (génregulációhoz, célzott szerkesztés nélküli kötődéshez), valamint fejlettebb módszerek, mint a base editing és a prime editing, amelyek pontos bázismódosításokat tesznek lehetővé kisebb kártétellel.
Alkalmazások
- Tudományos kutatás: génfunkciók gyors vizsgálata, knockout/knockin vonalak létrehozása modellorganizmokban és sejtvonalakban.
- Orvosi terápia: ex vivo és in vivo génterápiák — például vérképző őssejtek szerkesztése sarlósejtes vérszegénység vagy béta-talasszémia kezelésére; retina betegségek, rák immunterápiák fejlesztése. Számos klinikai vizsgálat folyamatban van.
- Mezőgazdaság: növények és állatok célzott nemesítése betegség-ellenállóság, hozam vagy tápérték javítására.
- Diagnosztika: CRISPR-alapú érzékelők (pl. SHERLOCK, DETECTR) gyors, érzékeny kórokozó-diagnosztikához.
- Antivirális és antimikrobiális megoldások: kutatások folynak arra, hogyan használhatók CRISPR-alapú módszerek vírusok vagy antibiotikum-rezisztensen terjedő gének célzására.
Korlátok, kockázatok és etikai kérdések
Bár a CRISPR forradalmasította a géntechnikát, több fontos probléma is fennáll:
- Off-target hatások: a nem kívánt helyeken bekövetkező szerkesztések kockázata, ami kiszűrhető és csökkenthető, de nem teljesen kiküszöbölhető.
- Szállítási nehézségek: hogyan juttassuk be biztonságosan és hatékonyan a szerkesztő rendszert a megfelelő sejtekbe — vírusvektorok, lipidnanorészecskék, elektroporáció és egyéb módszerek használatosak.
- Immunválasz: a Cas-fehérjéket hordozó szervezetek immunreakciót válthatnak ki.
- Germline vs. soma: az ivarsejtek és embriók szerkesztése öröklődő változásokat hozna létre, ami súlyos etikai és társadalmi kérdéseket vet fel (a He Jiankui-eset figyelmeztető példa volt).
- Szabályozás és jogi keretek: a technológia gyors fejlődése megköveteli a nemzetközi és nemzeti szabályozások folyamatos frissítését.
Kitekintés
A CRISPR alapú eszközök rendkívül sokféle irányban fejlődnek: pontosabb szerkesztők, jobb célzás, kevesebb mellék-hatás, és biztonságosabb szállítási módszerek fejlesztése folyik. A technológia már ma is forradalmi hatással van a kutatásra, mezőgazdaságra és az orvostudományra, de felelős alkalmazásához gondos tudományos, etikai és jogi megfontolások szükségesek.
Fontos megjegyezni: a CRISPR rendszerek természetes eredetű védekezési mechanizmusokból származnak, és ugyanazok az alapelvek (ismétlődő szekvenciák, spacer-ek, cas gének) állnak mögöttük, amelyekről korábban írtunk a genetikai kód, a baktérium és a archaea kontextusában. A technológia lehetővé teszi a precíz génmódosítást — a génmódosítás egyik legfontosabb eszközévé vált — ugyanakkor óvatosságot és alapos ellenőrzést igényel.