A kémiában a van der Waals-erők a molekulák közötti erők egyik csoportját alkotják. Ezek olyan viszonylag gyenge erők, amelyek a molekulákat és atomokat közel tartják egymáshoz. Nevüket Johannes Diderik van der Waals holland tudósról kapják. Bár egyes esetekben gyengébbek a kovalens kötéseknél, a van der Waals-erők döntő szerepet játszanak sok szerkezet és folyamat kialakulásában.
Többféle komponens — milyen típusok léteznek?
- London-féle diszperziós erők (indukált dipól–indukált dipól): minden atomra és molekulára hatnak, különösen fontosak apoláris részecskék és nemesgázok esetén. Ezek a gyorsan változó elektroneloszlásokból erednek, és általában az összes van der Waals-kölcsönhatás legerősebb komponensei nagy, könnyen polarizálható részecskék között.
- Dipól–dipól kölcsönhatások (Keesom): állandó dipólusú molekulák (például HCl) közt fellépő elektroosztatikus vonzás, amely a molekulák orientációjától függ.
- Dipól–indukált dipól kölcsönhatások (Debye): egy állandó dipólusú molekula polarizációt indukál egy apoláris részecskében, és így jön létre vonzás.
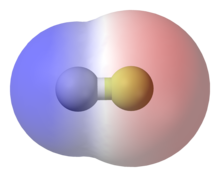
- Hidrogénkötés: bár formálisan erősebb és részben külön kategória, gyakran említik a van der Waals-erők környezetében, mert irányított, részben elektroosztatikus jellegű kölcsönhatás (például víz, aminosavak, nukleinsavak között). A cikk elején látható
is jól illusztrálja a dipólusokat és a hidrogénkötődést képző rendszereket.
Mechanizmus és távolságfüggés
A van der Waals-erők forrása az elektronok eloszlásának időleges vagy állandó egyenetlenségeiben keresendő. Az elektronok a molekula egyik végétől a másikig kellemetlen egyenletességgel keringenek, amit az anyagok körüli részleges töltések (δ− és δ+) hoznak létre; ezekre az effektekre utal a következő szöveg: az elektronok a molekula egyik végétől a másikig kissé eltérő töltéseket hoznak létre. Ezeket az enyhe különbségeket részleges töltéseknak nevezzük, mint δ- vagy δ+.
Matematikailag a diszperziós és dipólus-alapú komponensek gyakran r−6 távolságfüggést mutatnak (r a részecskék közötti távolság). A gyakorlatban a részecskék rövidtávolságú taszítása miatt a Lennard–Jones-potenciált használják gyakran, amely egy vonzó r−6 és egy erősen taszító ≈r−12 tag kombinációja.
Erősség, polarizálhatóság és van der Waals-sugár
- A kölcsönhatás erősségét befolyásolja a részecske polarizálhatósága: minél nagyobb a részecske elektronfelhője és minél könnyebben torzul, annál erősebbek a diszperziós erők.
- A van der Waals-sugár azt a távolságot jelzi, amelynél két atom egymáshoz érve még nem lép be kovalens kötésbe, és gyakran használják az atomok "méretének" becslésére.
- Makroszkopikus testekre vonatkozóan a Hamaker-állandóval írják le a van der Waals-energiát és -erőt, ami fontos például porok összetapadásában vagy felületi jelenségekben.
Szerep a kémiában, biológiában és anyagtudományban
A Van der Waals-erők — bár gyengék egyenként — összeadódva jelentős makroszkopikus hatásokat eredményeznek. Példák és hatások:
- Folyadékok és szilárd anyagok képződése: a nemesgázok kondenzációját és az apoláris molekulák forráspontjainak növekedését a diszperziós erők határozzák.
- Szupermolekuláris kémia: molekuláris összegződések és önszerveződő alakzatok stabilizálásában kulcsfontosságúak.
- Enzimekben és fehérjékben: a komplex térszerkezeteket és a molekuláris felismerést részben a van der Waals-kölcsönhatások határozzák meg (pl. ligandum kötődése az aktív helyhez).
- Polimerek tudományában a láncok közti kölcsönhatások befolyásolják a mechanikai tulajdonságokat és oldhatóságot.
- Nanotechnológia és felülettudomány: nanoszerkezetek, rétegezett anyagok (pl. grafénalapú heteroszerkezetek) stabilitása és a tapadás nagyban függ tőlük.
- Kondenzált anyag fizikában a molekuláris kristályok, amorf anyagok és felületi jelenségek leírásánál fontos komponensek.
- Szerves vegyületek fizikai tulajdonságai — például oldhatóságuk, olvadás- és forráspontjuk — gyakran a van der Waals-erők és hidrofób hatások együttese alapján alakulnak.
Mérések és modellezés
A van der Waals-erők mérésére és modellezésére különböző módszerek állnak rendelkezésre: spektroszkópia, röntgen- és neutrondiffrakció, atomfunkciós kölcsönhatások vizsgálata, illetve számítógépes módszerek (kvantumkémia, molekuladinamika). A gyakorlatban a Lennard–Jones-potenciál és a kvantumkémiai korrekciók (pl. dispersziós korrekciók a DFT-ben) segítenek a kölcsönhatások leírásában.
Összefoglalás
A van der Waals-kölcsönhatások a molekulák és anyagok közötti gyenge, de sokszor döntő fontosságú vonzó erők összességét jelentik. Három fő komponens (diszperziós, dipól–dipól és dipól–indukált dipól) különíthető el, és ezen felül a hidrogénkötés speciális, erősebb esete is szorosan kapcsolódik a témához. Ezek az erők alapvetőek a mindennapi anyagok szerkezetének és tulajdonságainak megértéséhez, a biológiai molekulák működésétől kezdve az anyagtudomány és nanotechnológia alkalmazásaiig.

