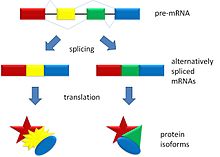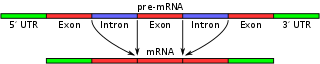
Alternatív splicing során egy génről származó pre-messenger RNS különböző módon vágódik és összeáll, így ugyanabból a DNS-szakaszból többféle érett hírvivő RNS (mRNS) és ezáltal többféle fehérje-izoforma jöhet létre. A folyamat lényege, hogy a pre-mRNS exonjai és intronjai különböző kombinációkban kapcsolódnak össze az RNS-splicing során, így változik az mRNS exon-összetétele.
Hogyan működik a splicing (alapok)
A splicingot a sejtben a spliceoszóma végzi: egy nagy RNS–fehérje komplex, amely kis nukleáris RNS-ekből (snRNS-ekből, például U1, U2, U4/U6, U5) és számos fehérjéből épül fel. A spliceoszóma felismeri a pre-mRNS-en található cis-elemeket (például az 5' splicing-helyet, a branch pointot és a 3' splicing-helyet), és katalizálja az intronok kivágását és az exonok összekapcsolását.
A splicing-helyek konszenzus szekvenciái (például az 5' GU és a 3' AG) fontosak a helyes vágáshoz, de a döntést finomhangolják transz-regulátor fehérjék:
- SR-fehérjék (serin/arginin-gazdag): általában splicing-aktivátorok, elősegítik bizonyos exonok beillesztését.
- hnRNP-ek (heterogén nukleáris RNP-ek): gyakran represszorok, gátolják egy-egy hely használatát.
Típusai
A legismertebb alternatív splicing-módok:
- Exon kihagyás (exon skipping) – egy exon kimarad a kész mRNS-ből (a leggyakoribb forma az eukariótákban).
- Mutuálisan kizáró exonnok – két (vagy több) exon közül csak az egyik kerül be az mRNS-be.
- Alternatív 5' vagy 3' splicing-helyek – az exon kezdete vagy vége eltérő helyen metsződik, így rövidebb vagy hosszabb exonok keletkeznek.
- Intron-retenció – egy intron nem vágódik ki, és benne marad az mRNS-ben.
- Alternatív promóterek és alternatív poliadeniláció – bár ezek nem klasszikus splicing-esetek, ugyancsak eltérő mRNS-változatokat eredményezhetnek.
Szabályozás
Az alternatív splicing szabályozása több szinten történik:
- Tissue-specifikus és fejlődési szabályozás: bizonyos izoformák csak adott szövetekben vagy fejlődési stádiumokban készülnek.
- Jelátviteli utak befolyásolják a splicing-faktort foszforilációval vagy más módosítással, így külső jelekre reagál a splicing.
- Az RNS-szekvencia finom különbségei (cis-elemek) meghatározzák, hogy egy adott helyet mennyire használnak.
Fiziológiai jelentőség és következmények
Az alternatív splicing nagyban növeli a genom által kódolható fehérjék sokféleségét: az emberben a multiexonikus gének körülbelül 95%-a alternatív splicinget mutat. Az izoformák különböző tulajdonságúak lehetnek:
- eltérő domének — más funkció vagy kötőpartner;
- veszteség vagy nyereség sejtszintű lokalizációs jelekből (pl. lokálisizációs szignál);
- differenciált szabályozás — különböző stabilitás, fordítási hatékonyság;
- egyes alternatív splicing-eredetű mRNS-ekhez nonsense-mediated decay (NMD) kapcsolódhat, azaz a hibás/korai stop-kodon miatt lebontódnak.
Alternatív splicing és betegségek
A splicing hibái számos betegség oka lehetnek. Példák:
- Gerincvelői izomsorvadás (SMA) — az SMN1/SMN2 gén alternatív splicingje kritikus szerepet játszik a betegségben; az SMN2 rosszabbul splicingelődik, így kevesebb működő SMN fehérje készül.
- β-talasszémia — bizonyos pontmutációk splicing-hibát okoznak a β-globin génben, csökkent hemoglobin-termelést eredményezve.
- Rák — onkogén vagy tumorszupresszor gének alternatív splicingje megváltozhat, ami hozzájárulhat a daganatok kialakulásához és progressziójához.
Több humán genetikai rendellenesség splicing-variánsokra vezethető vissza. A nem működő splicing-termékeket a sejtek poszt-transzkripciós minőség-ellenőrző mechanizmusai kezelik: például különböző enzimek és RNS-lebontó útvonalak (mint az exoszóma vagy az NMD) feldarabolják és eliminálják a hibás RNS-eket.
Diagnosztika és terápiás lehetőségek
Az alternatív splicing vizsgálata ma már rutin laboratóriumi módszerekkel történik: RT–PCR, RNA-seq és bioinformatikai elemzések mutatják meg az izoformák jelenlétét és relatív mennyiségét. Kutatásban minigének, mutagenezis és CRISPR-alapú megközelítések használatosak a splicing-mechanizmusok feltárására.
Terápiás beavatkozások:
- antiszensz oligonukleotidok (ASO) — specifikus mRNS-szakaszokhoz kötődve módosítják a splicinget (példa: Spinraza a SMA kezelésében);
- exon-skipping terápia — bizonyos exonok kihagyásával helyreállítható a fehérje részműködése (példa: bizonyos Duchenne-féle izomdystrophia terápiák);
- kis molekulás gyógyszerek, amelyek befolyásolják splicing-faktorok aktivitását (néhányat rákterápiában és SMA kezelésben vizsgálnak).
Összefoglalás
Az alternatív splicing egy dinamikus, szabályozott mechanizmus, amely lehetővé teszi, hogy egy gén többféle fehérjét adjon. Kritikus szerepet játszik a sejtbiológiában, a fejlődésben és az alkalmazkodásban, ugyanakkor hibái súlyos betegségekhez vezethetnek. A modern molekuláris biológiai és terápiás módszerek folyamatosan bővítik lehetőségeinket a splicing megértésére és célzott korrekciójára.