A kémiában és a fizikában az atomelmélet magyarázza, hogyan változott az atomról alkotott képünk az idők során. Az atomokat egykor az anyag legkisebb darabjainak tartották. Ma már azonban tudjuk, hogy az atomok protonokból, neutronokból és elektronokból állnak. Ezek a szubatomi részecskék kvarkokból állnak. Az atomra vonatkozó első elképzelés a görög filozófustól, Démokritosztól származik. A modern elmélet sok ötlete John Daltontól, egy brit kémikustól és fizikustól származik.
Az elmélet szilárd, folyékony és gáz halmazállapotú anyagokra alkalmazható, de a plazmákra és a neutroncsillagokra nem alkalmazható analóg módon.
Történeti áttekintés
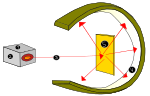
Az atom fogalma hosszú fejlődés eredménye. A görög gondolkodók (például Démokritosz) már az ókorban feltételeztek megoszthatatlan részecskéket, de a tudományos bizonyítékok csak a 19–20. század fordulóján jelentek meg. John Dalton a kémiai reakciók és arányok alapján visszaállította az atomok jelentőségét a kémiai elméletben. A kísérleti bizonyítékok — például a katódsugár-kísérletek — vezettek az elektron felfedezéséhez (J. J. Thomson, 1897), majd a mag szerkezetének feltárásához (Ernest Rutherford aranyfólia-kísérlete, 1909). A neutront James Chadwick fedezte fel 1932-ben.
Az atom szerkezete röviden
- Atommag: A magban találhatók a protonok és neutronok. A protonok száma határozza meg az elem rendszámát, a neutronok és protonok együttese adja az atom tömegét (tömegszám).
- Elektronfelhő: Az elektronok a mag körül, változó tartózkodási valószínűséggel helyezkednek el; a kvantummechanika szerint pályák helyett elektronpályákhoz (orbitálokhoz) és kvantumszámokhoz kötött eloszlást használunk.
- Izotópok: Ugyanannak az elemnek különböző neutronszámú változatai léteznek — ezek az izotópok, amelyek kémiai tulajdonságaikban hasonlóak, de tömegük és nukleáris tulajdonságaik eltérhetnek.
Szubatomi részecskék és kvarkok
A protonok és neutronok nem elemi részecskék: belső szerkezetük kvarkokra vezethető vissza. A proton két "up" és egy "down" kvarkból, a neutron egy "up" és két "down" kvarkból áll. Ezeket a kvarkokat a gluonok kötik össze a kvantum-színdinamika (QCD) elmélete szerint. Az elektron viszont elemi részecske, lepton, amelynek nem ismert belső szerkezete.
Az atommodellek fejlődése
- Dalton-modell: Az atom kémiai részecskeként jelent meg, meghatározott tömegekkel és arányokkal.
- Thomson-modell: "Mazsolás pogácsa" kép, ahol az elektronok elszórtan helyezkednek el pozitív közegben.
- Rutherford-modell: A kísérletek alapján kis, sűrű, töltött mag és körülötte keringenek az elektronok.
- Bohr-modell: Állítható pályák és kvantált energiaszintek bevezetése a hidrogénspektrum magyarázatára.
- Modern kvantummechanikai modell: Schrödinger és Heisenberg munkái után az elektronok eloszlását hullámfüggvényekkel írjuk le, amely pályák helyett valószínűségi felhőt ad meg.
Kémiai és fizikai következmények
Az atomok elektroneloszlása határozza meg az anyag kémiai viselkedését: a vegyértékelektronok határozzák meg a kötéseket és a reakcióképességet. Az atomok ionizálhatók (elektron leadásával vagy felvételével), így ionok keletkeznek. Az elemek rendszere — a periódusos rendszer — az elektronkonfigurációk és a rendszám alapján rendezett, ezért előre jelezhetők a kémiai tulajdonságok.
Energia és kötés
Az atommagban lévő nukleáris kötések energiái sokkal nagyobbak, mint a kémiai kötések energiái. A nukleáris reakciók (hasadás, fúzió) jelentős mennyiségű energiát szabadítanak fel a tömeg és energia viszonyát leíró E=mc² alapján. A kötési energia, azaz az atommag tömegdefektusa, fontos fogalom a nukleáris fizikában.
Megfigyelési módszerek és bizonyítékok
- Spektroszkópia: az atomok sugárzása és elnyelése diszkrét vonalakat ad, amelyeket kvantumelmélettel lehet magyarázni.
- Szórás- és részecskegyorsító-kísérletek: ezekkel feltárhatók a mag és a kvarkok szerkezeti részletei.
- Radioaktivitás és nukleáris kísérletek: információt adnak a magok stabilitásáról és bomlási folyamatairól.
Korlátok és különleges állapotok
A cikk elején említett megjegyzés arra utal, hogy az atomelmélet hagyományos formájában nehezen alkalmazható olyan szélsőséges körülményekre, mint a plazma vagy a neutroncsillagok anyaga. Ennek oka:
- Plazma: Itt az atomok jelentős része ionizált állapotban van, az elektronok és ionok kollektiv módon viselkednek, tehát plasmaphysikára és elektromágneses kölcsönhatások kollektív leírására van szükség.
- Neutroncsillagok: Rendkívül nagy nyomáson az anyag degnerált, a protonok és elektronok összepréselődhetnek neutronokká, illetve nukleonális és kvantumdegenerált anyagok jönnek létre. Itt a nukleáris fizika és általános relativitás együttes alkalmazása szükséges; az egyszerű atomos kép nem elegendő.
Összefoglalás
Az atomelmélet folyamatosan fejlődött a filozófiai feltételezésektől a modern kvantum- és részecskefizikáig. Ma már részletes képpel rendelkezünk az atomok és szubatomi részecskék szerkezetéről, miközben tudjuk, hogy bizonyos körülmények között — például erősen ionizált plazmákban vagy ultra-sűrű csillagok belsejében — további, speciális elméletekre van szükség a pontos leíráshoz.