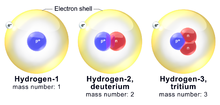
Egy kémiai elem atomjai különböző típusokban létezhetnek — ezeket nevezzük izotópoknak. Az izotópok ugyanannyi proton (és elektron) tartalmaznak, de eltérő számú neutron van bennük, ezért különböző a tömegük. A tömeg azt jelenti, hogy mennyi anyag van egy testben; az izotópok esetében a tömegkülönbség a nukleonok (protonok és neutronok) számának különbségéből adódik. Mivel a neutronok száma eltérő, ugyanazon elem különböző izotópjai különböző tömegszámúak és különböző fizikai tulajdonságokkal rendelkezhetnek.
Tömegszám és jelölés
Az izotópok azonos elem különböző változatai, ezért az atomszámuk — vagyis a protonok száma — megegyezik. Az atomszámot a protonok száma határozza meg, míg az izotópok megkülönböztetésére szolgáló fontos jellemző a tömegszám, amely a protonok és neutronok összegét adja. Az izotópok tömegszámáról gyakran az A betűvel beszélünk: A = Z + N (Z = protonok, N = neutronok).
Az izotópokat a vegyjel elé vagy fölé tett tömegszámmal jelöljük, például 12C vagy 12C a szén stabil izotópjára, illetve a hidrogén izotópjai: 1H (protium), 2H (deutérium) és 3H (trícium). A természetes elem relatív atomtömege pedig az adott izotópok bőségének súlyozott átlagából adódik.
Típusok, stabilitás és előfordulás
Az izotópok lehetnek stabilak vagy radioaktívak (radioizotópok). A radioaktív izotópok instabil maggal rendelkeznek, amely idővel bomlik, és közben sugárzást bocsát ki (alfa-, béta- vagy gamma-sugárzás). Például a szén-14 (14C) radioaktív izotópja a szén-dátumozás (radiokarbon módszer) alapja, mert felezési ideje körülbelül 5730 év. Másik példa: a trícium (3H) radioaktív, felezési ideje ~12,3 év. A deutérium (2H) viszont stabil.
Az egyes elemek több izotóppal rendelkezhetnek, amelyek természetes bőségükben nagyon eltérőek lehetnek. Néhány elemnek csak egy stabil izotópja van, másoknak több tucat stabil és/vagy radioaktív izotópja lehet.
Kémiai hatások és tömeghatás
Egy semleges atomban az elektronok száma megegyezik a protonok számával. Ugyanazon elem izotópjainak elektronszáma és elektronszerkezete is megegyezik, ezért a kémiai kötődésük és az alapvető kémiai tulajdonságaik szinte azonosak. Az atom kémiai viselkedését elsősorban az elektronok határozzák meg, így az izotópok általában ugyanazon reakciókban vesznek részt.
Ugyanakkor létezik a tömeghatás (kinetikai izotóphatás): a nehezebb izotópok reakciósebessége gyakran lassabb a könnyebb izotópokéhoz képest, mert nagyobb a tehetetlenségük és eltérő a kötési rezgésük. Ez a hatás különösen jól látható a protium (1H) és a deutérium (2H) közötti különbségnél, mivel a deutérium tömege gyakorlatilag kétszerese a protiumének. Nehézebb elemek esetén az izotópok közötti relatív tömegbeli különbség kisebb, így a tömeghatás általában kicsi, sokszor elhanyagolható.
Alkalmazások és példák
- Izotópjelölés és tracer-kutatás: stabil vagy radioaktív izotópokat használnak nyomjelzésre biológiában, kémiai mechanizmusok vizsgálatára és környezeti kutatásokra.
- Orvosi alkalmazások: bizonyos radioizotópokat diagnosztikára (pl. PET-vizsgálat, ahol gyakori az 18F), illetve sugárterápiára használnak.
- Éghajlat- és kormeghatározás: a szén-14 és más radioizotópok segítségével meghatározzák régészeti és geológiai minták korát.
- Energia és ipar: izotópokat használnak neutron-forrásként, illetve nukleáris energiatermelésben és anyagvizsgálatokban.
Összefoglalva: az izotópok ugyanannak a kémiai elemnek azok a változatai, amelyek azonos protonszámmal, de eltérő neutronszámmal rendelkeznek. Ez a különbség határozza meg a tömegszámukat, a nukleáris stabilitásukat és bizonyos fizikai tulajdonságaikat, miközben kémiai viselkedésük általában nagyon hasonló marad.