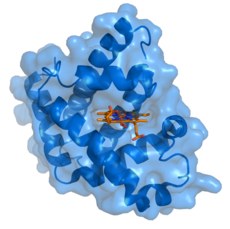
A ligandum egy biokémiai anyag. Feladata, hogy egy biológiai molekulához kötődjön, és a molekulát rávegye egy funkció betöltésére. A ligand megkötése megváltoztatja a receptorfehérje alakját. Ez megváltoztatja a fehérje viselkedését.
Szűkebb értelemben ez egy jelkiváltó molekula, amely egy célfehérje egy helyéhez kötődik.
A kötés molekulák közötti erők, például ionos kötések, hidrogénkötések és van der Waals-erők révén történik. A dokkolás (asszociáció) általában reverzibilis (disszociáció).
A ligandumok közé tartoznak a szubsztrátok, inhibitorok, aktivátorok és neurotranszmitterek. A kötődés hajlamát vagy erősségét affinitásnak nevezzük.
Kötés mechanizmusa és jellemzői
A ligand és a receptormolekula közötti kölcsönhatásokat többféle gyenge kötés tartja össze: elektrosztatikus (ionos) kölcsönhatások, hidrogénkötések, van der Waals-erők és hidrofób interakciók. Ezek együtt határozzák meg a kötés pontosságát és erősségét. A kölcsönhatás lehet ortoszterikus (a ligandum a hatóhelyen kötődik) vagy alloszterikus (más helyen kötődik, és a fehérje konformációját változtatja meg).
Az interakciók leírására fontos fogalmak:
- Affinitás: a ligand és a receptor közötti kötés erőssége; gyakran a disszociációs konstanssal (Kd) jellemzik — minél kisebb a Kd, annál nagyobb az affinitás.
- Kinetika: az asszociációs (kon) és disszociációs (koff) sebességek határozzák meg, milyen gyorsan kötődik és szabadul fel a ligandum.
- Szelektivitás és specifitás: egy ligandum mennyire preferál egy adott célpontot a többi hasonló molekulával szemben.
- Aviditás: multivalens (többkötésű) kölcsönhatások összhatása — különösen fontos pl. antitestek és több kötőhellyel rendelkező ligandumok esetén.
Típusok és példák
Ligandum lehet:
- Szubsztrát: az enzim által átalakított molekula.
- Agonista: receptorhoz kötődve aktiválja annak jelátviteli funkcióját (például sok neurotranszmitter, hormonok agonistái).
- Antagonista/inhibitor: kötődik a helyhez, de nem aktiválja a receptort; megakadályozza az agonista hatását (gyakori gyógyszerhatás).
- Alloszterikus modulátorok: a fő hatóhelytől eltérő helyen kötődnek, módosítva a receptor válaszát.
- Kofaktorok és koenzimek: enzimek működéséhez szükséges kisebb molekulák.
Farmakológiai és biológiai jelentőség
A ligandum-receptor interakciók alapvetőek a sejtek közötti kommunikációban és a fiziológiás szabályozásban. A gyógyszertervezésnél cél, hogy olyan ligandumokat alkossunk, amelyek optimális affinitással és szelektivitással rendelkeznek a kívánt célponthoz, miközben minimalizálják az off-target hatásokat. A strukturális biológia és a számítógépes dokkolás (docking) módszerei segítik a hatékony ligandumok tervezését.
Mérések és elemzési módszerek
Ligandum–receptor kölcsönhatásokat különböző módszerekkel vizsgálják:
- Radioligand kötés: radioaktív jelölésű ligandumot használnak a kötőhelyek számának és affinitásának mérésére.
- Surface plasmon resonance (SPR): valós időben követi a kötődés és leválás kinetikáját.
- Isotermikus titrálási kalorimetria (ITC): a kötés termodinamikai paramétereit (ΔG, ΔH, ΔS) méri.
- Enzimkinetika: a Km és Vmax értékekből következtetnek a szubsztrát affinitására és hatékonyságára.
Speciális jelenségek
Induced fit és lock-and-key: a klasszikus „kulcs-zár” modell mellett sok esetben a receptor konformációja a ligand kötődésekor változik (induced fit). Több kötőhelyes rendszerekben előfordulhat kooperativitás, amikor egy ligandum kötődése megkönnyíti vagy megnehezíti a következő kötődést.
Összefoglalva: a ligandumok széles körű szerepet játszanak a biokémiában és farmakológiában — a kötődési erősség (affinitás), kinetika, szelektivitás és a kötés helye mind fontosak a biológiai hatás meghatározásában és a gyógyászati alkalmazások tervezésében.