A sejtbiológiában a receptorok olyan speciális struktúrák, amelyek a sejtmembránokban találhatók. Ezek fehérjemolekulákból, például glikoproteinekből állnak. A receptorok speciális molekulákhoz kötődnek (kapcsolódnak). Ha a receptor rendelkezik ezzel a molekulával, akkor aktiválódik, ha viszont nem, akkor deaktiválódik. Állapotától függően változás történik a sejten belül.
A sejtfelszíni receptorok (membránreceptorok, transzmembrán receptorok) részt vesznek a sejt és a külvilág közötti kommunikációban. A sejteken kívüli jelzőmolekulák (általában hormonok, neurotranszmitterek, citokinek, növekedési faktorok vagy sejtfelismerő molekulák) kapcsolódnak a receptorhoz. Ez változásokat vált ki a sejt működésében. A folyamatot jelátvitelnek nevezzük: A kötődés kémiai változást indít el a membrán belsejében.
Röviden, a receptorok úgy működnek, mint a zárak és a kulcsok. A kulccsal a zárat be lehet zárni vagy ki lehet nyitni. Ha ki van nyitva, a hozzá tartozó ajtó kinyitható.
Receptorok szerkezete és felépítése
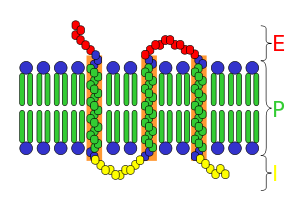
A membránreceptorok szerkezete általában három fő részből áll:
- Extracelluláris ligandumkötő domén: ez az a része a receptorfehérjének, amely konkrétan felismeri és megköti a külső jelzőmolekulát. Gyakran glikoprotein formában van, vagyis cukormolekulák kapcsolódnak hozzá (glikoziláció), ami befolyásolja a stabilitást és a felismerést.
- Transzmembrán szegmens(ek): hidrofób aminosavak alkotta rész, amely a lipidmembránba illeszkedik; egyes receptorok több átmenettel rendelkeznek a membránon.
- Intracelluláris effektor- vagy jelátviteli domén: a sejten belüli jelet továbbító rész, amely lehet enzimes aktivitás (például tirozin-kináz), vagy olyan oldalsó láncokkal ellátott terület, amely adapter fehérjéket toboroz.
Fő típusok és példák
- Ioncsatorna összekapcsolt receptorok (ligand-activated ion channels): a ligand kötődése nyitja vagy zárja az ioncsatornát, ami gyors elektromos választ eredményez. Példa: a nikotinos acetilkolin-receptor (gyors neuromuszkuláris jelátvitel).
- G-fehérjéhez kapcsolt receptorok (GPCR-ek): nagy család, amely a ligand kötődése után G-fehérjét aktivál, és ez más effektorokat (adenilát-cikláz, foszfolipáz C stb.) indít el. Példa: β-adrenerg receptorok.
- Enzimatikusan aktív receptorok (receptor tirozin-kinázok, RTK-k): a ligand kötődése dimerizációt és autofoszforilációt vált ki, ami további jelátviteli kaszkádokat indít. Példa: inzulinreceptor, növekedési faktor receptorok.
- Citokinreceptorok és immunreceptorok: nem mindig rendelkeznek beépített enzimes aktivitással, de adaptorfehérjéket toboroznak, amelyek elindítják a jelátvitelt (pl. JAK–STAT út).
Jelátviteli mechanizmusok — hogyan továbbítódik a jel?
A ligand kötődése konformációs változást okoz a receptorban, amely a sejt belsejében különböző mechanizmusokat indíthat el:
- Ionfluxus: ioncsatornák megnyílása változtatja a membránpotenciált és az elektromos jelet (gyors válasz ideg- vagy izomsejtekben).
- G-fehérje-mediált útvonalak: Gα vagy Gβγ alegységek befolyásolják az adenilát-ciklázot (cAMP képződés), a foszfolipáz C-t (IP3 és DAG keletkezése, Ca2+ felszabadulás), vagy ioncsatornákat.
- Kináz-kaszkádok: receptor tirozin-kinázok aktiválása foszforilálási láncot indít (pl. MAP-kináz út), ami génexpressziót, anyagcsere-változást vagy sejtosztódást szabályozhat.
- Second messengerek: kis molekulák (pl. cAMP, cGMP, IP3, DAG, Ca2+) közvetítik és felerősítik a jelet belső hatásokig.
Affinitás, specificitás és jel amplifikáció
A receptoroknak jellemzői közé tartozik a ligand iránti affinitásuk (milyen erősen kötődnek) és specificitásuk (mennyire szelektíven ismernek fel egy molekulát). Egyetlen ligandum-receptor kötődés is nagy belső választ indíthat el: a jelátviteli folyamatokban gyakori a felerősítés (amplifikáció), amikor egy aktivált receptor több G-fehérjét vagy enzimet képes aktiválni egymás után.
Szabályozás, deszenzitizáció és jel leállítása
A jelátvitelt pontosan szabályozni kell. Főbb mechanizmusok:
- Deszenzitizáció: tartós stimuláció hatására a receptorok érzéketlenebbé válhatnak (pl. foszforiláció és β-arrestin kötődés GPCR-eknél).
- Internalizáció: receptorok endocitózissal a sejt belsejébe kerülhetnek, ahol lebomlanak vagy újrahasznosulnak.
- Ligand lebontása vagy eltávolítása: az extracelluláris jel molekulák inaktiválása (enzimek, reuptake) megszünteti a stimulust.
- Negatív feedback: a jelátviteli kaszkádok gyakran aktiválnak olyan elemeket, amelyek gátolják a folyamatot (pl. foszfatázok, gátló fehérjék).
Farmakológiai fogalmak és orvosi jelentőség
A receptorok fontos gyógyszercélpontok. Néhány alapfogalom:
- Agonista: olyan molekula, amely aktiválja a receptort és hasonló választ vált ki, mint az endogén ligand.
- Antagonista: kötődik a receptorhoz, de nem aktiválja; gátolja az endogén ligand hatását.
- Parciális agonista, inverz agonista: változó mértékű aktivációt vagy a receptor konstitutív aktivitásának csökkentését eredményezik.
Receptorok hibája vagy mutációja számos betegséghez vezethet (pl. inzulinreceptor rezisztencia, öröklődő receptordefektusok), ezért a receptorok megértése kulcsfontosságú a terápiás fejlesztésben.
Gyakorlati példák
- Nikotinos acetilkolin-receptor: gyors ioncsatorna, szerepe az izomösszehúzódásban és a szinaptikus jelátvitelben.
- β-adrenerg receptorok: GPCR-ek, amelyek a szívfrekvenciát és a légutak simaizmait szabályozzák; béta-blokkolók és béta-agonisták céltípusai.
- Inzulinreceptor: dimerként működő tirozin-kináz receptor, fontos a glükózanyagcserében és a sejtnövekedés szabályozásában.
Összefoglalva: a sejtfelszíni receptorok alapvető szereplők a sejt-környezet közötti kommunikációban. A ligandkötés által indukált konformációs változások komplex jelátviteli hálózatokat aktiválnak, amelyek szabályozzák a sejt anyagcseréjét, génkifejeződését, mozgását és túlélését. A receptorok molekuláris megértése és farmakológiai célzása alapvető a modern biokémia és orvostudomány számára.