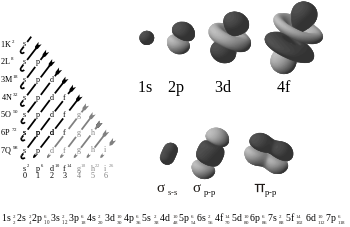
A kémiában a pi-kötések (π-kötések) olyan kovalens kémiai kötések, ahol az egyik elektron pályája keresztezi (átfedésben van) egy másik elektron pályájával. Pontosabban: a π-kötés oldalsó (side‑to‑side) átfedés eredménye, amely két, egymással párhuzamos vagy közel párhuzamos p‑orbitál között jön létre. Ennek következtében a kötéstér két, az internukleáris tengely fölött és alatt elhelyezkedő töltéssűrűség‑lob képviseli, míg a kötés tengelyére merőleges sík csomóponti síkként viselkedik. A pálya csomóponti síkjai közül csak az egyik halad át mindkét érintett magon, ezért a π‑kötésben lévő elektronok sűrűsége nem a kötéstengelyen, hanem annak környezetében koncentrálódik.
Szerkezet és kialakulás
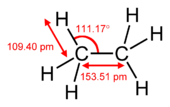
A nevükben szereplő görög π betű a p‑orbitálisokra utal, mert a π‑kötés tipikusan p‑orbitálok közötti oldalirányú átfedésből jön létre. A π‑kötés orbitális szimmetriája a kötés tengelye mentén úgy néz ki, mint a p‑orbitális: a hullámfüggvény előjelei az egyik lobban megegyeznek, a másikban ellentétesek. Gyakran előfordul, hogy egyszeresen kapcsolódó atomok között a belső σ‑kötés (szigma) alakul ki, míg kettős kötés esetén egy σ és egy π, hármas kötésnél egy σ és két π‑kötés található. Az sp2‑hibridizáció például az alkénekre jellemző: a három hibridizált orbitál síkban helyezkedik el, míg a megmaradó p‑orbitál függőleges, és ez vesz részt a π‑kötésben.
Bár a d‑orbitálokról is gyakran beszélnek π‑típusú kötések kapcsán, a d‑orbitálok valódi szerepe vegyes: átmenetifém‑komplexeknél fontos a d→π* és π→d kölcsönhatás (például π‑visszadónás), míg a főcsoportos elemeknél a d‑orbitálok bevonása a kötésbe vitatott kérdés a hipervalencia kontextusában.
Kötésenergia, geometria és forgás
A π‑kötések általában gyengébbek, mint a szigma kötések. A kvantummechanika szerint ez azért van, mert az oldalirányú p–p átfedés kisebb, mint a tengelyirányú σ‑átfedés, tehát a kötésenergia alacsonyabb és a kötéshossz általában nagyobb. Emiatt a π‑kötések gyakran reaktívabbak is a σ‑kötéseknél.
Fontos következmény, hogy a π‑kötéssel összekapcsolt molekuladarabok nem tudnak szabadon elfordulni a kötés körül anélkül, hogy a π‑kötés megszakadna. A forgás ugyanis tönkretenné a két p‑orbitális párhuzamos illeszkedését, így a kettős kötés körüli rotáció jelentős energiaigényű folyamat.
Kémiai tulajdonságok és reakciók
- Pi‑elektronok: A π‑kötésben lévő elektronokat gyakran pi‑elektronoknak nevezik. Ezek a rendszerek képesek delokalizálódni (konjugáció), ami stabilizációhoz és jellegzetes fizikai tulajdonságokhoz (például UV–vis abszorpció) vezet.
- Reaktivitás: A π‑kötések elektromilag sűrűbb zónái miatt gyakran nukleofil/elektrofílszerű viselkedést mutatnak: például az alkeneknél tipikus az elektrofíliás addíció, aromás rendszereknél pedig a delokalizált π‑rendszer sajátos szubstitúciós reakciókat ad.
- Konjugáció és aromásság: Szomszédos π‑kötések közötti átfedés következtében kialakulhat konjugált rendszer, amely csökkenti a HOMO–LUMO energiakülönbséget és növeli a stabilitást. Aromás vegyületeknél (Hückel‑szabály: 4n+2 π‑elektron) a π‑elektronok delokalizációja különleges stabilitást eredményez.
- Antikötő π* pályák: A π‑rendszer rendelkezik kötő (π) és antikötő (π*) orbitálokkal; elektronbefogadás vagy visszadónás során a π* elfoglalódása gyengítheti a π‑kötést.
- Koordinációs kémia: A π‑kötések és a π‑elektronok fontos szerepet játszanak átmenetifém‑komplexekben (pl. olefin‑komplexek, karbonilok), ahol π‑donor és π‑backbonding kölcsönhatások alakítják a kötési jelleget.
Gyakorlati példák
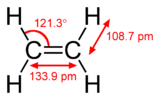
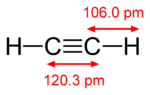
Példákra: az etén (etilén) C=C kötése egy σ és egy π‑komponensből áll; az etin (acetilén) C≡C kötés pedig egy σ és két ortogonális π‑kötést tartalmaz. Aromás példákban, mint a benzol, a hat π‑elektron delokalizált rendszerben oszlik el, ami a molekula speciális kémiai tulajdonságait adja.
Összefoglalva: a π‑kötések speciális, oldalirányú atomi pályák átfedéséből adódó kötések, amelyek gyengébbek, de reakcióképesek és kulcsfontosságúak a molekulák szerkezetében, elektroneloszlásában és számos kémiai reakció mechanizmusában.