A termodinamika második törvénye azt mondja ki röviden, hogy egy zárt (elszigetelt) rendszerben az entrópia általában nem csökken; a természet irányultsága szerint az energia és az anyag a lehető legjobban elterjed a rendelkezésre álló tereken és állapotokon. Gyakorlatilag ez azt jelenti, hogy amikor az energia egyik formából egy másikba alakul át, vagy az anyag szabadon mozog, a rendszer rendezetlensége (entrópiája) nő, és spontán folyamatok általában a rendezetlenség növelése felé haladnak.
A hőmérséklet, a nyomás és a sűrűség különbségei egy idő után kiegyenlítődnek, amennyiben nincs külső beavatkozás; vízszintes irányban (szabad mozgás esetén) általában teljes kiegyenlítődés következik be. A gravitáció miatt azonban a sűrűség és a nyomás függőlegesen nem feltétlenül egyenlítődik ki teljesen: lefelé, az alul lévő rétegekben a nyomás és a sűrűség rendszerint nagyobb, mint felül.
Az entrópia a rendszerben lévő energia és anyag eloszlásának, illetve a mikroszkopikus állapotok számának mérőszáma: minél többféleképpen rendeződhetnek az összetevők (minél több mikrosztátusz áll rendelkezésre), annál nagyobb az entrópia. Röviden: az entrópia az anyag és az energia „szétszóródásának” mértéke.
Clausius és Kelvin megfogalmazásai
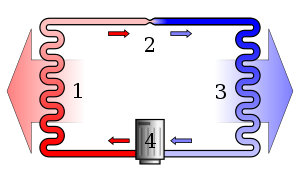
A termodinamika második törvényének legismertebb klasszikus megfogalmazásai közül az egyik Rudolf Clausius nevéhez fűződik. A hétköznapi értelemben ezt úgy szoktuk mondani, hogy minden megpróbálja ugyanazt a hőmérsékletet fenntartani az idő múlásával: a hő spontán módon csak a melegebb testből a hidegebb felé folyik.
A hő önmagában nem tud átmenni egy hidegebb testből egy melegebb testbe.
Lord Kelvin egy ekvivalens, gépekre (hőerőgépekre) fókuszáló megfogalmazást adott:
Lehetetlen olyan átalakítás, amelynek egyetlen végeredménye az állandó hőmérsékletű forrásból kivont hő munkává alakítása.
Mindkét állítás ugyanannak az alapelvnek a kétféle leírása: nem létezik olyan gép, amely kizárólag hőt vesz fel egyetlen hőforrásból és azt maradéktalanul munkává alakítja (Kelvin–Planck-formuláció), illetve a hő soha nem áramlik magától hidegebb testből melegebbe (Clausius-formuláció). A kettő matematikailag és logikailag egyenértékű.
Matematikai megfogalmazás és reverzibilitás
Formálisan egy izolált rendszer entrópiaváltozása soha nem lesz negatív:
ΔS_total ≥ 0
Reverzibilis (ideális) folyamat esetén ΔS_total = 0; irreverzibilis folyamatnál ΔS_total > 0. A hőátadás reverzibilis eseteiben az entrópia-változásra gyakran használjuk a következő összefüggést:
ΔS = ∫ (dQ_rev / T),
ahol dQ_rev a reverzibilis közben felvett (vagy leadott) hő mennyisége, T pedig az abszolút hőmérséklet.
Statisztikus értelmezés (Boltzmann)
Statisztikus mechanikai nézőpontból Boltzmann híres egyenlete köti össze az entrópiát a mikroszkopikus állapotok számával:
S = k_B ln W,
ahol S az entrópia, k_B a Boltzmann-állandó (k_B ≈ 1,380649·10^−23 J·K^−1), W pedig a rendszer által felvehető mikrosztátuszok száma. Ez az összefüggés megmagyarázza, miért tekinthető az entrópianövekedés valószínűségi jelenségnek: a „rendezett” makróállapotokhoz kevesebb mikrosztátusz tartozik, míg a „rendezetlenekhez” jóval több.
Példák és következmények
- Hőáramlás: két érintkező test közül a melegebb lead hőt a hidegebb felé, amíg hőmérsékletük egyenlő nem lesz — ez az entrópia növekedésével jár.
- Szabad expanzió: egy gáz szabad térbe való kitágulása reverzibilis munkavégzés nélkül növeli a rendszer entrópiáját.
- Keveredés: két különböző gáz összekeveredése növeli az entrópiát; ennek visszafordítása (hatékony szétválasztás) munkát igényel.
- Hőerőgépek: a Carnot-hőerőgép maximális hatásfoka két hőmérséklet között η ≤ 1 − T_c/T_h, ami közvetlen következménye a második törvénynek.
Korlátok, kivételek és finomítások
A második törvény statisztikus természetű: nagyon kis rendszereknél és rövid idők alatt felléphetnek ingadozások, amelyek során lokálisan az entrópia rövid időre csökkenhet. Az ilyen fluktuációk azonban a nagyszámú részecske és hosszú időskálák esetén elenyészően valószínűek, ezért makroszkopikus rendszerekben a törvény rendkívül megbízható.
Továbbá fontos megjegyezni, hogy a második törvény egy zárt vagy izolált rendszerre vonatkozik. Nyitott rendszerekben az entrópia lokálisan csökkenhet (például egy hűtőszekrényben), de ilyenkor a környezet entrópiájában bekövetkező növekedés összességében nagyobb lesz, így a teljes (rendszer + környezet) entrópia növekedése megmarad.
Összefoglalás
A termodinamika második törvénye alapvető korlátot szab meg az energiaátalakulások irányára és hatékonyságára: spontán folyamatok rendre az entrópia növelése felé mutatnak, a reverzibilis (ideális) folyamatok esetében az entrópia állandó. Ez a törvény összekapcsolja a makroszkopikus megfigyeléseket a mikroszkopikus valószínűségeken alapuló magyarázattal, és számos gyakorlati következménnyel jár a hőerőgépek, hűtők és általános energiaátalakítások terén.