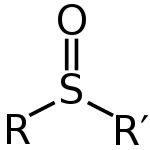
A szulfoxid olyan molekula, amelyben egy kénatom két szénatomhoz és egy oxigénatomhoz kapcsolódik. A tioéterek oxidációjából származik, anélkül, hogy egészen a szulfonig menne. Mint sok kéntartalmú molekula, a szulfoxid is néha nagyon büdös lehet — például a dimetil-szulfoxid (DMSO) enyhén kénszagú, más szulfoxidok pedig intenzívebb, fokhagymára emlékeztető illatot adhatnak.
Szerkezet és sztereokémia
A szulfoxidok általános képlete R–S(=O)–R'. A kénnek az oxigénnel formálódó közel dupla kötése és a két szénnel létesített egyszerű kötések mellett egy magányos pár elektronja is van, ezért a kén környezete tetraéderes geometriájúnak tekinthető. Ennek következtében a kén lehet királis központ abban az esetben, ha R és R' különböző csoportok; sok szulfoxid tehát enánsziomerként előállítható és izolálható, ami fontos az aszimmetrikus szintézisben és katalízisben.
A S=O kötéssel kapcsolatban érdemes megjegyezni a polaritást: a kötés erősen polarizált, a kén részlegesen pozitív (Sδ+) míg az oxigén részlegesen negatív (Oδ–). Ez a polaritás befolyásolja a fizikai és kémiai tulajdonságokat, valamint a koordinációs viselkedést átmeneti fémekhez.
Fizikai tulajdonságok (példa: DMSO)
- Dimetil-szulfoxid (DMSO): (CH3)2S=O — színtelen, higroszkópos folyadék.
- Olvadáspont: körülbelül +18,5 °C — ezért hűvösebb helyen megszilárdulhat.
- Forráspont: kb. 189 °C — magas forráspontú, ezért hőstabil oldószer.
- Sűrűség: ~1,10 g·cm–3 (20–25 °C körül).
- Permittivitás (dielektromos állandó): viszonylag nagy (DMSO ≈ 47), ezért erősen poláris, aprotikus oldószer.
- Keverhetőség: vízzel és sok szerves oldószerrel jól keveredik.
Kémiai tulajdonságok és reaktivitás
A szulfoxidok általában stabilabbak a tioétereknél, de oxidálhatók tovább szulfonokká (R–S(=O)2–R') erős oxidálószerekkel. Fordítva, redukcióval visszaalakulhatnak tioéterekké. A szelektív oxidáció fontos részfeladat a szulfoxidok előállításában — gyakori reagensek például mCPBA, hidrogén-peroxid katalizátorral vagy más enyhébb oxidálószerek.
Néhány jellegzetes reakció és felhasználás:
- Swern-oxidáció: DMSO mint reagens szerepel olyan eljárásokban, amelyek elsődleges vagy másodlagos alkoholokat alakítanak át aldehidekké vagy ketonokká (oxalil-kloriddal és bázissal kombinálva).
- Pummerer-átalakítás: szulfoxidok aktiválása után alfa-helyzetben történő funkcióbevezetésre használható reakciók.
- Ligandumként való viselkedés: a szulfoxidok koordinálhatnak átmeneti fémekhez, leggyakrabban a kén atomon keresztül, de okszigenkötésű koordináció is előfordulhat, ami fontos homogene katalízisben.
- Aszimmetrikus szintézis: chiralitásuk és stabil enánsziomereik miatt szulfoxidokat aszimmetrikus segédanyagként vagy katalizátorkomponensként használnak.
Alkalmazások
- Oldószer: DMSO és más szulfoxidok kiváló poláris aprotikus oldószerek, gyakoriak szerves és biokémiai laboratóriumi reakciókban, különösen ahol ionos reaktánsok stabilizálása vagy nagy polaritás szükséges.
- Kryoprotektáns: DMSO-t gyakran alkalmaznak sejtvédőként krioprezerválásnál (például 10% DMSO a fagyasztó közegben), mert csökkenti a jégkristályok okozta sejtkárosodást.
- Orvosi/biológiai felhasználás: DMSO helyi gyulladáscsökkentőként és fájdalomcsillapító hatású szerekkel kombinálva szerepel egyes terápiákban (például intersticiális cisztitis kezelésében engedélyezett készítmények). Erősen ható transzdermális hordozóként is ismert: képes átvinni más molekulákat a bőrön keresztül.
- Ipari alkalmazások: oldószerként, reakcióközegként és olyan helyzetekben, ahol magas hőstabilitás és polaritás szükséges.
Biztonság és környezet
Bár a DMSO viszonylag alacsony akut toxicitású, különleges óvintézkedéseket igényel:
- DMSO jól felszívódik a bőrön át, és képes más vegyületeket is magával vinni a szervezetbe — ezért laboratóriumi munka során mindig viseljen védőkesztyűt, és kerülje a bőrrel való érintkezést, különösen ha a folyadék nem tiszta.
- Topikális alkalmazáskor előfordulhat bőrirritáció, vörösödés, valamint jellegzetes, enyhe fokhagymára emlékeztető szag a leheletben vagy a bőrön.
- Súlyos mérgezési esetek ritkák, de a nagy dózisú vagy szennyezett anyaggal történő expozíció káros lehet — gondoskodjon megfelelő szellőzésről és hulladékkezelésről.
Példák és fontos megjegyzések
- A dimetil-szulfoxid (DMSO) a legismertebb és leggyakrabban használt szulfoxid: egyszerű szerkezetű, olcsó és sokoldalú oldószer.
- Sok szulfoxid jellegzetes szagú; a szag és a bőrön való felszívódás miatt különös elővigyázatosság szükséges, ha szennyeződések, oldószermaradékok vagy gyógyszerhatóanyagok jelen lehetnek.
- Szulfoxidok és derivátumaik (például sulfoximinek) fontosak a gyógyszerkutatásban, anyagtudományban és katalízisben.
Összefoglalva: a szulfoxidok (R–S(=O)–R') fontos, sokoldalú kéntartalmú vegyületek, melyek jellegzetes szerkezete és polaritása miatt értékesek a szerves szintézisben, az analitikai kémiai alkalmazásokban, valamint az ipari és orvosi felhasználásokban. Különös figyelmet igényelnek a megfelelő kezelés és a transzdermális felszívódás kockázatainak ismerete miatt.