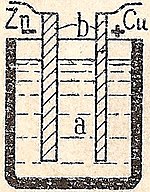
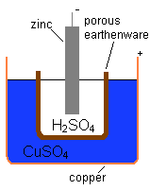
A kémiai cella a kémiai energiát elektromos energiává alakítja. A legtöbb akkumulátor kémiai cella. Az akkumulátorban kémiai reakció megy végbe, amely elektromos áramot indít el.
Az akkumulátoroknak két fő típusa van: az újratölthető és a nem újratölthető akkumulátorok.
A nem újratölthető akkumulátor addig ad áramot, amíg a benne lévő vegyi anyagok el nem fogynak. Ezután már nem használható. Joggal nevezhető "használd és dobd el".
Az újratölthető akkumulátort úgy lehet újratölteni, hogy az elektromos áramot visszafelé vezetjük át az akkumulátoron; ezután újra fel lehet használni, hogy több villamos energiát termeljen. Gaston Planté francia tudós volt az, aki 1859-ben feltalálta ezeket az újratölthető akkumulátorokat.
Az akkumulátoroknak sokféle formája és mérete van, a játékokban és fényképezőgépekben használt nagyon kicsiktől kezdve az autókban használtakig, vagy akár a nagyobbakig. A tengeralattjárókhoz nagyon nagy méretű akkumulátorok szükségesek.
Működési elv — röviden
A kémiai cella alapvetően három fő részből áll: az anód (negatív elektróda), a katód (pozitív elektróda) és az elektrolit. Töltéskor és kisütéskor redoxireakciók (elektronátadás) zajlanak az elektródák felületén. Ezek a reakciók hozzák létre az elektronáramlást a külső áramkörben, amit mi elektromos áramként használunk.
Főbb elméleti fogalmak
- Üzemi feszültség: egy cella névleges feszültsége (pl. alkáli ≈ 1,5 V; NiMH/NiCd ≈ 1,2 V; lítiumion ≈ 3,6–3,7 V; ólomsavas cella ≈ 2,0 V).
- Kapacitás: amperóra (Ah) vagy milliamperóra (mAh) egységben mérik, megmutatja, mennyi töltést képes leadni a cella.
- Belső ellenállás: minél kisebb, annál hatékonyabban tud nagy áramot adni az akkumulátor; növekedése csökkenti a leadható teljesítményt.
- Önkisülés: az az jelenség, amikor az akkumulátor tárolt energiája kémiai folyamatok miatt idővel csökken, még terhelés nélkül is.
- Töltési ciklusok és élettartam: az újratölthető cellákhoz ciklusszám társul (hányszor tölthetők/üríthetők), amely függ a kémiai rendszertől és a használati körülményektől.
Főbb típusok és jellemzőik
- Nem újratölthető (primer) cellák:
- Zinc–karbon (egyszerű, olcsó)
- Alkáli mangán-dioxid (gyakoribb, nagyobb kapacitás, 1,5 V)
- Lítium (magas energiasűrűség, hosszú élettartam, gyakori kis fogyasztó eszközökben)
- Újratölthető (szekunder) cellák:
- Ólomsavas (lead-acid) – autóindító akkumulátorokban gyakori; cellafeszültség ≈ 2,0 V, 12 V-os akkumulátor 6 cellából áll.
- NiCd (nikkel–kadmium) – robosztus, jól bír nagy áramot, de memóriahatás és mérgező kadmium miatt visszaszorulóban.
- NiMH (nikkel–fémhidrid) – jobb energiasűrűség, kevesebb memóriahatás.
- Lítium-ion és lítium-polimer – magas energiasűrűség, alacsony önkisülés, széles körben használják mobiltelefonokban, laptopokban és elektromos járművekben.
Gyakorlati tudnivalók
- Sorba és párhuzamosan kapcsolás: sorba kötéskor a cellák feszültsége adódik össze, párhuzamos kapcsoláskor a kapacitás növekszik. Pontosan egyező kapacitású és állapotú cellákat érdemes kombinálni a hosszú élettartamért.
- Töltés és töltésvezérlés: különböző cellatípusokhoz eltérő töltési algoritmus szükséges (például ólom-sav: „bulk–absorption–float”, Li-ion: CC-CV). Rossz töltés csökkentheti az élettartamot vagy veszélyes helyzetet teremthet.
- Biztonság: ne rövidre zárjuk, ne szúrjuk ki vagy melegítsük túl az akkumulátort. Különösen a Li-ion celláknál fennáll a „thermal runaway” (hőfutás) kockázata túlterhelés vagy sérülés esetén.
- Környezetvédelem és újrahasznosítás: sok akkumulátort (különösen az ólomsavasakat és bizonyos lítium- és nikkel alapúakat) érdemes és törvényileg is szükséges visszavinni gyűjtőhelyre vagy újrahasznosítóhoz a veszélyes anyagok miatt.
Alkalmazások
Az akkumulátorokat kisebb hordozható eszközöktől (távirányítók, elemlámpák) kezdve a fogyasztói elektronikán át (telefonok, laptopok) egészen a közlekedésig (hibrid és tisztán elektromos autók, indítóakkumulátorok) és ipari méretű energiatárolókig használják. Nagy rendszerek, például tengeralattjárók vagy energiatároló farmok különösen nagy kapacitású és speciális cellákat igényelnek.
Összefoglalás
Az akkumulátor/kémiai cella a mindennapi élet fontos részét képezi: energia tárolására szolgál kémiai úton, majd ezt elektromosság formájában leadja. Különböző kémiai rendszerek léteznek, melyek eltérő feszültséget, kapacitást, élettartamot és biztonsági jellemzőket kínálnak. A megfelelő típus kiválasztása, helyes töltés és a környezetbarát ártalmatlanítás mind hozzájárul az eszköz hatékony és biztonságos használatához.