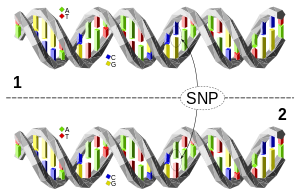
Az egynukleotid-polimorfizmus (SNP, ejtsd: snip; többes számban snip) egy populációban előforduló DNS-szekvencia-változás. Az SNP egyetlen nukleotid különbség a genomban.
Például a két emberből származó szekvenált DNS-darabok, az AAGCCTA és az AAGCTTA között egyetlen nukleotidban különbözik. Ebben az esetben azt mondjuk, hogy két allél van. Szinte minden gyakori SNP-nek csak két allélja van. Az SNP-k leggyakrabban a DNS olyan régióiban fordulnak elő, amelyek nem befolyásolják a szervezet túlélését: különben a természetes szelekció kiszűrné őket. Más tényezők, például a genetikai rekombináció és a mutációs ráta szintén befolyásolhatják az SNP-sűrűséget. Az emberi populációk között is vannak eltérések, így az egyik földrajzi vagy etnikai csoportban gyakori SNP-allél egy másikban sokkal ritkább lehet.
Ezeket az egyének közötti genetikai eltéréseket (különösen a genom nem kódoló részeiben) néha kihasználják a DNS-ujjlenyomatok készítésénél, amelyet a törvényszéki tudományban használnak. Ezek a genetikai eltérések a betegségekre való fogékonyságunkban is különbséget okoznak. A betegségek súlyossága és az, ahogyan szervezetünk a kezelésekre reagál, szintén a genetikai eltérések megnyilvánulásai. Például az APOE (apolipoprotein E) gén egyetlen bázisú mutációja az Alzheimer-kór magasabb kockázatával jár.
Típusok és hatásuk a génekre
Az SNP-k különféle helyeken és módon fordulhatnak elő, és ennek megfelelően eltérő lehet a hatásuk:
- Exonikus (kódoló) SNP-k – megváltoztathatják a fehérje aminosavsorrendjét. Ezek lehetnek szinonim (nem változtatják az aminosavat) vagy nem szinonim (megváltoztatják az aminosavat), illetve ritkábban stop-kodon létrehozásához vagy megszüntetéséhez vezethetnek.
- Intrónikus és nem kódoló régiókban lévő SNP-k – befolyásolhatják az alternatív hasítást, az RNS-stabilitást vagy a génszabályozást, például promoter- vagy enhancerrégiókban.
- Regulációs SNP-k – hatással lehetnek arra, hogy egy gén mikor és mennyire expresszálódik (pl. transzkripciós faktor kötőhelyeket érintve).
Gyakoriság és terminológia
Az SNP elnevezés általában olyan egynukleotidos változatokra vonatkozik, amelyek a populációban viszonylag gyakoriak; gyakran az a küszöb, hogy a ritkább allél gyakorisága >1% (ez a határ nem szigorúan kötött). A ritkább egynukleotid-változatokat általában nem SNP-nek, hanem ritka mutációnak vagy variánsnak nevezik. A kisebb gyakoriságú allél gyakoriságát MAF-nek (minor allele frequency) hívjuk.
Haplotípusok és linkáltsági egyensúly
Több SNP egymás melletti kombinációja kialakít haplotípusokat; a különböző SNP-ek közti kapcsolatot (hogy együttesen milyen gyakran öröklődnek) linkáltsági egyensúlynak (linkage disequilibrium, LD) nevezzük. Ezek fontosak a populációgenetikai elemzésekben és a betegség-asszociációs kutatásokban (pl. GWAS), mert gyakran nem maga a vizsgált SNP okozza a hatást, hanem egy vele LD-ben lévő funkcionális variáns.
Vizsgálati módszerek
Sokféle módszer létezik SNP-k detektálására és genotípus meghatározására:
- SNP-mikrotömbök (SNP-arrayek) – nagy mennyiségű ismert SNP gyors és olcsó genotipizálására alkalmasak.
- Teljes-genom szekvenálás (WGS) és exom-szekvenálás – ritka és új variánsok feltárására.
- Célzott PCR-alapú módszerek, Sanger-szekvenálás – kis számú SNP megerősítésére.
- Next-generation sequencing alapú genotipizálás – nagy átviteli sebesség és részletesség.
Orvosi és klinikai jelentőség
SNP-k közvetlenül vagy közvetetten befolyásolhatják a betegségek kialakulását, a kórlefolyást és a gyógyszerreakciót. Fontos területek:
- Betegségkockázat – sok komplex betegségre (pl. cukorbetegség, szív-érrendszeri betegségek, autizmus, különböző daganatok) vonatkozó genetikai rizikót vizsgáló tanulmányok SNP-eket azonosítanak, amelyek statisztikailag növelik a kockázatot. Ezek gyakran kismértékű hatásúak, és sok SNP kombinációja határozza meg a tényleges rizikót.
- Farmakogenetika – SNP-k befolyásolhatják, hogyan reagál valaki egy gyógyszerre (hatékonyság, mellékhatások). Példák: a CYP2C9 és VKORC1 variánsok a warfarin adagolását befolyásolhatják, bizonyos CYP allélek pedig a számos gyógyszer metabolizmusát módosítják.
- Monogénes betegségekkel kapcsolatos változatok – egyes egynukleotid-változások egyértelműen betegséget okozhatnak (pl. bizonyos véralvadási rendellenességekhez kapcsolódó pontmutációk).)
- Diagnosztika és predikció – SNP-k segítik a genetikai kockázatbecslést és a személyre szabott orvoslás felé vezető döntéseket, bár értelmezésük gyakran bonyolult és mindig klinikai kontextust igényel.
Gyakorlati példák
- APOE ε4 allél — növeli az Alzheimer-kór kockázatát (már szerepelt a bevezetőben).
- Factor V Leiden (G1691A) — egy egynukleotid-csere, amely fokozott vérrögképződési hajlamhoz kapcsolódik.
- MTHFR C677T — hatással lehet a homocisztein-anyagcserére; egyes tanulmányok kapcsolták különböző klinikai állapotokhoz, bár a hatás mértéke és klinikai jelentősége vitatott.
Korlátok, etikai és értelmezési kérdések
Fontos megérteni, hogy:
- Sok SNP hatása kicsi, és környezeti tényezők, életmód vagy más genetikai variánsok befolyásolják a végső kockázatot.
- Az asszociáció nem bizonyít okozati összefüggést; gyakran további funkcionális vizsgálatok szükségesek a mechanizmus megértéséhez.
- Genetikai eredmények visszajelzése etikai és pszichológiai kérdéseket vet fel (pl. diszkrimináció, biztosítás, életminőségre gyakorolt hatás), ezért a klinikai genetikai tanácsadás fontos része az eredmények kezelésének.
Források és adatbázisok
Sok ismert SNP és populációs gyakoriság megtalálható nemzetközi adatbázisokban (például dbSNP, 1000 Genomes, gnomAD), amelyek a kutatók és klinikusok számára fontos forrást jelentenek.
Összefoglalva: az SNP-k egyszerű, de igen elterjedt genetikai változatok, amelyek kulcsszerepet játszanak a populációgenetikában, a betegségek kockázatának megértésében, a farmakogenetikában és a forenzikában. Az értelmezésük sokszor összetett, és mindig a genetikai, környezeti és klinikai adatok együttes vizsgálatát igényli.